Al2(SO4)3 (Aluminium sulfate) (Tính chất hóa học, vật lí, nhận biết, điều chế, ứng dụng)
Bài viết về tính chất hóa học của Al2(SO4)3 (Aluminium sulfate) gồm đầy đủ thông tin cơ bản về Al2(SO4)3 trong bảng tuần hoàn, tính chất hóa học, tính chất vật lí, cách điều chế và ứng dụng.
Al2(SO4)3 (Aluminium sulfate) (Tính chất hóa học, vật lí, nhận biết, điều chế, ứng dụng)
I. Định nghĩa Aluminium sulfate
- Aluminium sulfate là một hợp chất hóa học của nhôm với công thức Al2(SO4)3.Nó hòa tan trong nước và chủ yếu được sử dụng như một chất kết tủa (khiến các hạt ô nhiễm co cụm lại thành các hạt lớn hơn, dễ dàng bị mắc kẹt) trong lọc nước uốngvà các nhà máy xử lý nước thải, và trong sản xuất giấy.
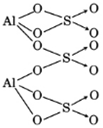
- Công thức phân tử: Al2(SO4)3
II. Tính chất vật lí của Aluminium sulfate & nhận biết
- Tính chất vật lí : Là chất rắn, có màu trắng, dễ hút ẩm.
- Nhận biết: Cho dung dịch Aluminium chloride tác dụng với dung dịch BaCl2, thấy xuất hiện kết tủa trắng:
Al2(SO4)3 + 3BaCl2 → 3BaSO4↓ + 2AlCl3
III. Tính chất hóa học của Aluminium sulfate
- Mang đầy đủ tính chất hóa học của muối
- Tác dụng với dung dịch bazo:
Al2(SO4)3 + 6KOH(vừa đủ) → 3K2SO4 + 2Al(OH)3
- Tác dụng với dung dịch muối khác:
Al2(SO4)3 + Ba(NO3)2 → 3BaSO4↓ + 2Al(NO3)3
- Phản ứng với kim loại mạnh hơn:
3Mg + Al2(SO4)3 → 3MgSO4 + 2Al
IV. Điều chế Aluminium sulfate
- Cho hiđroxit nhôm, Al(OH)3 tác dụng với axit sunfuric:
2Al(OH)3 + 3H2SO4 → Al2(SO4)3 +6H2O
- Cho kim loại nhôm trong dung dịch axit sunfuric:
2Al+ 3H2SO4 → Al2(SO4)3 + 3H2
V. Ứng dụng của Aluminium sulfate
- Aluminium sulfate được sử dụng trong lọc nước và như là một gắn màu trong dệt nhuộm và in ấn. Trong lọc nước, nó khiến các tạp chất keo lại thành các hạt lớn hơn và sau đó lắng xuống đáy của bình nước (hoặc được lọc ra) dễ dàng hơn.
- Nhôm sulfate đôi khi được dùng để giảm độ pH của đất vườn, vì nó thủy phân để tạo thành chất kết tủa hydroxit nhôm và một dung dịch axit sunfuric loãng.
- Trong ngành công nghiệp xây dựng, nó được sử dụng như chống thấm và tác nhân tăng tốc trong bê tông.
- Là một chất tạo bọt trong bọt chữa cháy.
Xem thêm tính chất hóa học của các chất khác:
- Tính chất của Al (Aluminium)
- Tính chất của Al2O3 (Aluminium oxide)
- Tính chất của Al(OH)3 (Aluminum hydroxide)
- Tính chất của AlCl3 (Aluminium chloride)
- Tính chất của AlH3 (Aluminium hydride)
- Tính chất của AlN (Aluminium nitride)
- Tính chất của Al4C3 (Aluminium carbide)
- Tính chất của Al2S3 (Aluminium sulfide)
- Tính chất của NaAlO2 (Sodium aluminate)
- Tính chất của Na3AlF6 (Cryolite)
- Tính chất của Phèn chua (K2SO4.Al2(SO4)3.24H2O hay KAl(SO4)2.12H2O)
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Loạt bài Wiki tính chất hóa học trình bày toàn bộ tính chất hóa học, vật lí, nhận biết, điều chế và ứng dụng của tất cả các đơn chất, hợp chất hóa học đã học trong chương trình Hóa học cấp 2, 3.
Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Đề thi lớp 1 (các môn học)
- Đề thi lớp 2 (các môn học)
- Đề thi lớp 3 (các môn học)
- Đề thi lớp 4 (các môn học)
- Đề thi lớp 5 (các môn học)
- Đề thi lớp 6 (các môn học)
- Đề thi lớp 7 (các môn học)
- Đề thi lớp 8 (các môn học)
- Đề thi lớp 9 (các môn học)
- Đề thi lớp 10 (các môn học)
- Đề thi lớp 11 (các môn học)
- Đề thi lớp 12 (các môn học)
- Giáo án lớp 1 (các môn học)
- Giáo án lớp 2 (các môn học)
- Giáo án lớp 3 (các môn học)
- Giáo án lớp 4 (các môn học)
- Giáo án lớp 5 (các môn học)
- Giáo án lớp 6 (các môn học)
- Giáo án lớp 7 (các môn học)
- Giáo án lớp 8 (các môn học)
- Giáo án lớp 9 (các môn học)
- Giáo án lớp 10 (các môn học)
- Giáo án lớp 11 (các môn học)
- Giáo án lớp 12 (các môn học)






 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

