Top 8 Đề kiểm tra Hóa học 9 Chương 3 có đáp án, cực hay
Top 8 Đề kiểm tra Hóa học 9 Chương 3 có đáp án, cực hay
Để học tốt Hóa học lớp 9, dưới đây là danh sách Top 8 Đề kiểm tra Hóa học 9 Chương 3 có đáp án, cực hay gồm các đề kiểm tra 15 phút, 45 phút (1 tiết). Hi vọng bộ đề thi này sẽ giúp bạn ôn luyện & đạt điểm cao trong các bài thi Hóa học 9.
Đề kiểm tra 15 phút
Đề kiểm tra 1 tiết
Đề thi Học kì I
>Đề kiểm tra 15 phút Hóa học 9 Chương 3
Phần tự luận
Câu 1: (3 điểm) Bằng phương pháp hóa học hãy phân biệt 2 khí Cl2 và SO2 được chứa trong 2 bình riêng biệt.
Câu 2: (4 điểm) Một hợp chất có thành phần theo khối lượng: SiO2 75%, CaO 12%, Na2O 13%. Xác định công thức hóa học của các hợp chất ở dạng oxit (Ca=40, O=16, Na=23, Si=28).
Câu 3: (3 điểm) Nhiệt phân 80g đá vôi, toàn bộ khí sinh ra được sục vào dung dịch nước vôi trong dư, thu được 60g kết tủa CaCO3. Giả thiết các phản ứng xảy ra hoàn toàn. Tính độ tinh khiết của loại đá vôi trên (Ca=40, O=16, C=12, Na=23, Si=28).
Đáp án và hướng dẫn giải
Câu 1:
Trích khí ở mỗi bình lần lượt cho qua dung dịch nước vôi trong, khí làm đục dung dịch Ca(OH)2 là SO2.
Ca(OH)2 + SO2 → CaSO3↓ + H2O
2Ca(OH)2 + 2Cl2 → CaCl2 + Ca(ClO)2 + 2H2O
Khí Cl2 không tạo kết tủa.
Câu 2:
Gọi công thức hợp chất: xCaO.yNa2O.zSiO2
Tỉ lệ x: y: z = 12/56:13/62:75/60 = 0,21: 0,21: 1,25 = 1: 1: 6
Công thức hóa học ở dạng oxit của chất đó: CaO.Na2O.6SiO2
Câu 3:
CaCO3 to→ CaO + CO2
CO2 + Ca(OH)2 → CaCO3 + H2O
mCaCO3 tạo ra = mCaCO3 ban đầu = 60 gam
Độ tinh khiết của loại đá vôi trên là:
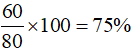
Đề kiểm tra 1 tiết Hóa học 9 Chương 3
Phần trắc nghiệm
Câu 1: (1 điểm)
| Công thức phân tử | Ca(HCO3)2 | NaHCO3 | NaClO | KMnO4 |
| Gọi tên | Canxi cacbonat | Natri hidrocacbonat | Natri hipoclorat | Kali pemanganat |
| (1) | (2) | (3) | (4) |
Các chất gọi đúng tên là
A. (1), (2), (3)
B. (1), (2), (4)
C. (1), (3), (4)
D. (2), (4)
Câu 2: (1 điểm) Cho sơ đồ:
CO2 NaOH (1)→ NaHCO3 H2CO3 (2)→ Na2CO3 dd HCl (3)→ NaHCO3
Trong 3 vị trí trên, chất phản ứng ở vị trí nào sai?
A. (2) B. (3) C. (1) D. (1) và (2)
Câu 3: (2 điểm) Phản ứng nào sau đây thể hiện tính chất của NaHCO3?
NaHCO3 + NaOH → Na2CO3 + H2O
2NaHCO3 to→ Na2CO3 + CO2 + H2O
2NaHCO3 + Ca(OH)2 → Na2CO3 + CaCO3 +2H2O
2NaHCO3 + CaCl2 → Ca(HCO3)2 + 2NaCl
A. (2), (3), (4)
B. (1), (3), (4)
C. (1), (2), (4)
D. (1), (2), (3)
Câu 4: (1 điểm) Có các chất bột màu trắng: Na2CO3, CaCO3, NaHCO3, NaCl. Có thể dùng hóa chất nào sau đây để nhận biết từng chất?
A. nước, dung dịch HCl
B. nước, dung dịch CaCl2, dung dịch HCl
C. dung dịch HCl, dung dịch CaCl2
D. dung dịch Ca(OH)2
Câu 5: (1 điểm) Cho các phương trình hóa học
CO2 + H2O ⇌ H2CO3 (1)
CaCO3 + 2HCl → CaCl2 + CO2 + H2O (2)
Các phát biểu sau, phát biểu nào đúng?
A. phương trình (1) chứng tỏ axit H2CO3 là axit không bền. Phương trình (2) chứng tỏ axit H2CO3 có tính axit yếu hơn axit HCl
B. phương trình (1) nói lên axit H2CO3 là axit 2 nấc
C. phương trình (2) nói lên CaCO3 là muối tan được trong nước
D. phương trình (2) có thể xảy ra theo chiều ngược lại
Câu 6: (1 điểm) CO2 và SiO2 có điểm giống nhau là cùng
A. tác dụng với kiềm và oxit bazo
B. tác dụng với nước
C. tác dụng với dung dịch muối
D. được dùng để chữa cháy
Câu 7: (1 điểm) Phương trình hóa học nào sau đây không dùng để sản xuất thủy tinh?
A. CaCO3 to→ CaO + CO2
B. CaO + SiO2 to→ CaSiO3
C. Na2CO3 + SiO2 to→ Na2SiO3 + CO2
D. Si + O2 to→ SiO2
Câu 8: (2 điểm) Khối lượng KHCO3 thu được khí sục 6,72 lít khí CO2 (đktc) vào 400ml dung dịch KOH 1M là (K=39, O=16, C=12, H=1)
A. 20g B. 10g C. 30g D. 40g
Đáp án và hướng dẫn giải
| Câu | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| Đáp án | D | A | D | B | A | A | D | A |
Câu 1:D
Ca(HCO3)2: canxi hidrocacbonat. NaClO: natri hipoclorit
Câu 2:A
Vị trí (2): là nhiệt phân hay tác dụng với NaOH.
Câu 3:D
Phản ứng (4) 2NaHCO3 + CaCl2 → Ca(HCO3)2 + 2NaCl
Không xảy ra vì Ca(HCO3)2 và NaCl đều là những chất tan được trong nước.
Câu 4:B
Chất không tan trong nước là CaCO3.
Dung dịch CaCl2 nhận ra Na2CO3 do tạo kết tủa CaCO3.
Na2CO3 + CaCl2 → CaCO3↓ + 2NaCl
Dùng dung dịch HCl nhận ra được NaHCO3 do có hiện tượng sủi bọt
NaHCO3 + HCl → NaCl + CO2↑ + H2O
Còn lại là NaCl.
Câu 5:A
CO2 + H2O ⇌ H2CO3 (1)
Nghĩa là có sự phân hủy H2CO3.
CaCO3 + 2HCl → CaCl2 + CO2 + H2O (2)
Axit H2CO3 bị axit HCl đẩy ra khỏi muối CaCO3.
Câu 6:A
SiO2 không tác dụng với nước, không tác dụng với dung dịch muối, không dùng để chữa cháy.
Câu 7:D
Si + O2 to→ SiO2 không dùng trong sản xuất thủy tinh
Câu 8:A
nCO2 = 6,72/22,4 = 0,3 mol
nKOH = 0,4 mol => 1 < nKOH/nCO2 < 2
Nên phản ứng tạo ra 2 muối: CO2 + KOH → KHCO3
CO2 + 2KOH → K2CO3 + H2O
Gọi x, y lần lượt là số mol của KHCO3, K2CO3.
Thì nCO2 = x + y = 0,3 và nKOH = x + 2y = 0,4.
Giải ta được y = 0,1 mol, x = 0,2 mol => mKHCO3 = 0,2 x 100 = 20 gam.
Xem thêm các đề kiểm tra, đề thi Hóa Học lớp 9 chọn lọc, có đáp án hay khác:
Loạt bài Đề thi Hóa lớp 9 năm 2025 học kì 1 và học kì 2 được biên soạn bám sát cấu trúc ra đề thi mới Tự luận và Trắc nghiệm giúp bạn giành được điểm cao trong các bài thi Hóa học lớp 9.
Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Giáo án lớp 9 (các môn học)
- Giáo án điện tử lớp 9 (các môn học)
- Giáo án Toán 9
- Giáo án Ngữ văn 9
- Giáo án Tiếng Anh 9
- Giáo án Khoa học tự nhiên 9
- Giáo án Vật Lí 9
- Giáo án Hóa học 9
- Giáo án Sinh học 9
- Giáo án Địa Lí 9
- Giáo án Lịch Sử 9
- Giáo án GDCD 9
- Giáo án Tin học 9
- Giáo án Công nghệ 9
- Đề thi lớp 9 (các môn học)
- Đề thi Ngữ Văn 9 (có đáp án)
- Đề thi Toán 9 (có đáp án)
- Đề thi Tiếng Anh 9 mới (có đáp án)
- Đề thi Tiếng Anh 9 (có đáp án)
- Đề thi Khoa học tự nhiên 9 (có đáp án)
- Đề thi Lịch Sử và Địa Lí 9 (có đáp án)
- Đề thi GDCD 9 (có đáp án)
- Đề thi Tin học 9 (có đáp án)
- Đề thi Công nghệ 9 (có đáp án)




 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp



