NaOH + Cl2 → NaCl + NaClO + H2O | NaOH ra NaCl | NaOH ra NaClO | Cl2 ra NaCl | Cl2 ra NaClO
Phản ứng NaOH + Cl2 hay NaOH ra NaCl hoặc NaOH ra NaClO hoặc Cl2 ra NaCl hoặc Cl2 ra NaClO thuộc loại phản ứng oxi hóa khử đã được cân bằng chính xác và chi tiết nhất. Bên cạnh đó là một số bài tập có liên quan về NaOH có lời giải, mời các bạn đón xem:
2NaOH + Cl2 → NaCl + NaClO + H2O
1. Phương trình hoá học của phản ứng Cl2 tác dụng với NaOH
Cl2 + 2NaOH → NaCl + NaClO + H2O
Cách lập phương trình hoá học:
Bước 1: Xác định các nguyên tử có sự thay đổi số oxi hoá, từ đó xác định chất oxi hoá – chất khử:
Chất khử và chất oxi hoá đều là: Cl2.
Bước 2: Biểu diễn quá trình oxi hoá, quá trình khử
- Quá trình oxi hoá:
- Quá trình khử:
Bước 3: Tìm hệ số thích hợp cho chất khử và chất oxi hoá
Bước 4: Điền hệ số của các chất có mặt trong phương trình hoá học. Kiểm tra sự cân bằng số nguyên tử của các nguyên tố ở hai vế.
Cl2 + 2NaOH → NaCl + NaClO + H2O
2. Điều kiện để Cl2 tác dụng với NaOH
Phản ứng giữa Cl2 và NaOH diễn ra ngay điều kiện thường.
3. Cách tiến hành thí nghiệm
Dẫn khí clo vào ống nghiệm đã để sẵn dung dịch NaOH và mẩu giấy quỳ tím.
4. Hiện tượng phản ứng
Ban đầu mẩu quỳ có màu xanh, sau khi phản ứng xảy ra màu quỳ bị mất.
- Nguyên tử clo có độ âm điện lớn (3,16) chỉ sau F (3,98) và O (3,44). Vì vậy trong các hợp chất với các nguyên tố này clo có số oxi hóa dương (+1; +3; +5; +7), còn trong các trường hợp khác clo có số oxi hóa âm (-1).
- Khi tham gia phản ứng hóa học clo dễ dàng nhận thêm 1 electron:
Cl + 1e → Cl-
⇒ Tính chất hóa học cơ bản của clo là tính oxi hóa mạnh.
5.1. Tác dụng với kim loại
- Khí clo oxi hóa trực tiếp được hầu hết các kim loại tạo thành muối clorua. Phản ứng xảy ra ở nhiệt độ thường hoặc không cao lắm, phản ứng xảy ra nhanh, tỏa nhiều nhiệt.
- Ví dụ:
2Na + Cl2 2NaCl
2Fe + 3Cl2 2FeCl3
Cu + Cl2 CuCl2
- Trong phản ứng với kim loại clo thể hiện tính oxi hóa.
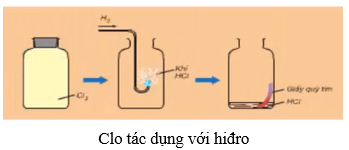
5.2. Tác dụng với hiđro
- Ở nhiệt độ thường và trong bóng tối, khí clo hầu như không phản ứng với khí hiđro.
- Khi chiếu sáng hỗn hợp bởi ánh sáng mặt trời hoặc ánh sáng của magie cháy, phản ứng xảy ra và có thể nổ. Hỗn hợp nổ mạnh nhất khi tỉ lệ số mol giữa hiđro và clo là 1 :
- Phương trình hóa học:
H2 + Cl2 2HCl
- Trong phản ứng với H2, clo thể hiện tính oxi hóa.
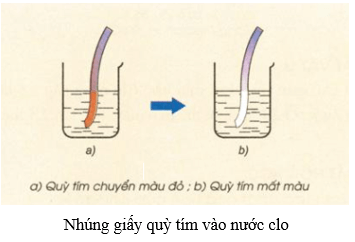
5.3. Tác dụng với nước
- Khi tan trong nước, một phần khí clo tác dụng với nước tạo ra hỗn hợp hydrochloric acid và axit hipoclozơ.
- Phương trình hóa học:
Trong phản ứng trên clo vừa là chất oxi hóa vừa là chất khử.
- Phản ứng trên là phản ứng thuận nghịch do HClO là chất oxi hóa mạnh, có thể oxi hóa HCl thành Cl2 và H2O. Cũng do HClO có tính oxi hóa mạnh nên nước clo có tính tẩy màu.
- Chú ý: Thành phần của nước clo gồm: Cl2; HCl; HClO; H2O
Mở rộng:
Ngoài ra, clo có thể tham gia một số phản ứng hóa học khác như:
- Tác dụng với dung dịch bazơ:
Cl2 + 2NaOH → NaCl + NaClO + H2O
3Cl2 + 6KOH KClO3 + 5KCl + 3H2O
- Tác dụng với muối của các halogen khác
Cl2 + 2NaBr → 2NaCl + Br2
Cl2 + 2FeCl2 → 2FeCl3
- Tác dụng với chất khử khác
3Cl2 + 2NH3 → N2 + 6HCl
Cl2 + SO2 + 2H2O → H2SO4 + 2HCl
6. Bài tập vận dụng liên quan
Câu 1: Cho 13,44 lít khí clo (đktc) đi qua 2,5 lít dung dịch KOH ở 1000C. Sau khi phản ứng xảy ra hoàn toàn, thu được 37,25 gam KCl. Dung dịch KOH trên có nồng độ là
A. 0,24M
B. 0,20M
C. 0,40M
D. 0,48M
Hướng dẫn giải:
Đáp án A
Vì Cl2 dư, KOH phản ứng hết
→ Tính số mol KOH theo KCl
→ nKOH = 0,6 mol
→ CM(KOH) = 0,24M
Câu 2: Cho V lít Cl2 tác dụng với dung dịch NaOH vừa đủ ở điều kiện thường, cô cạn dung dịch thu được m1 gam muối khan. Cũng lấy V lít Cl2 cho tác dụng với dung dịch NaOH vừa đủ, đun nóng ở 80oC, cô cạn dung dịch thu được m2 gam muối. Thể tích khí Cl2 đo ở cùng điều kiện. Tỉ lệ m1:m2 là
A. 1:2
B. 1:1,5.
C. 1:1
D. 2:1.
Hướng dẫn giải:
Đáp án C
Bảo toàn khối lượng cho phương trình (1)
(*)
Bảo toàn khối lượng cho phương trình (2)
(**)
Theo phương trình:
Từ (*) và (**) → m1 = m2
→ m1 : m2 = 1:1
Câu 3: Thể tích khí Cl2 (đktc) thu được khi cho 3,95 gam KMnO4 phản ứng hết với dung dịch HCl (lấy dư) là
A. 1,4000 lít
B. 1,4560 lít
C. 1,3440 lít
D. 0,0625 lít
Hướng dẫn giải:
Đáp án A
Bảo toàn electron:
lít
Câu 4: Cho 1 lít H2 (đktc) tác dụng với 0,672 lít Cl2 (đktc) rồi hòa tan sản phẩm vào nước để được 20 gam dung dịch A. Lấy 5 gam A tác dụng với dung dịch AgNO3 dư thu được 1,435 gam kết tủa. Tính hiệu suất phản ứng giữa H2 và Cl2 (giả sử Cl2 và H2 không tan trong nước)
A. 50%
B. 33,33%
C. 60%
D. 66,67%
Hướng dẫn giải:
Đáp án D
H2 + Cl2 → 2HCl
Vì hiệu suất phản ứng tính theo Cl2
AgNO3 + HCl → AgCl ↓ + HNO3
→ nHCl (5g A) = nAgCl = 0,01 mol
→ nHCl (20g A) = 0,01.4 = 0,04 mol
Theo phương trình:
Câu 5: Trong phản ứng: Cl2 + H2O HCl + HClO clo đóng vai trò
A. Là chất khử
B. Vừa là chất oxi hóa, vừa là chất khử
C. Là chất oxi hóa
D. Không là chất oxi hóa, không là chất khử
Hướng dẫn giải:
Đáp án B
Xét sự thay đổi số oxi hóa của Cl:
+ Tăng từ 0 lên +1 (trong HClO)
+ Giảm từ 0 xuống -1 (trong HCl)
⇒ Clo vừa là chất khử vừa là chất oxi hóa
Câu 6: Nước clo có màu:
A. vàng lục
B. vàng da cam
C. vàng đậm
D. vàng nhạt
Hướng dẫn giải:
Đáp án A
Dung dịch nước clo là dung dịch hỗn hợp giữa Cl2, HCl và HClO nên có màu vàng lục, mùi hắc của clo.
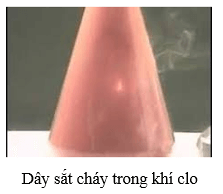
Câu 7: Hiện tượng xảy ra khi cho dây sắt nóng đỏ vào bình đựng khí clo là:
A. Có khói trắng
B. Có khói nâu
C. Có khói đen
D. Có khói tím
Hướng dẫn giải:
Đáp án B
2Fe + 3Cl2 → 2FeCl3 (có màu nâu)
Câu 8. Cho sơ đồ chuyển hóa sau: Cl2 → X → Y → Z → X → Cl2. Trong đó X, Y, Z là các chất rắn; Y và Z đều chứa natri. X, Y, Z là
A. NaCl, NaBr, Na2CO3
B. NaBr, NaOH, Na2CO3
C. NaCl, Na2CO3, NaOH
D. NaCl, NaOH, Na2CO3
Hướng dẫn giải:
Đáp án D
Cl2 → NaCl → NaOH → Na2CO3 → NaCl → Cl2.
2Na + Cl2 → 2NaCl
2NaCl +2H2O 2NaOH + H2 + Cl2
2NaOH + CO2 → Na2CO3 + H2O
Na2CO3 + 2HCl → 2NaCl + H2O + CO2
2NaCl +2H2O2NaOH + H2 + Cl2
Câu 9. Đốt cháy hết 13,6g hỗn hợp Mg, Fe trong bình kín chứa khí clo dư, sau phản ứng thì lượng clo trong bình giảm tương ứng 0,4 mol. Khối lượng muối clorua khan thu được là.
A. 65,0 g. B. 38,0 g. C. 50,8 g. D. 42,0 g.
Hướng dẫn giải
Đáp án D
mmuối = mKL
Câu 10. Nước Gia-ven là hỗn hợp các chất nào sau đây?
A. HCl, HClO, H2O. B.NaCl, NaClO, H2O.
C. NaCl, NaClO3, H2O. D. NaCl, NaClO4, H2O.
Hướng dẫn giải
Đáp án B
Cho khí clo tác dụng với dung dịch NaOH loãng ở nhiệt độ thường ta thu được nước Gia-Ven theo PTHH sau: 2NaOH + Cl2 → NaCl + NaClO + H2O.
Xem thêm các phương trình hóa học hay khác:
- 2NaOH + CO2 → Na2CO3 + H2O
- NaOH + CO2 → NaHCO3
- 2NaOH + SO2 → Na2SO3 + H2O
- NaOH + SO2 → NaHSO3
- NaOH + HCl → NaCl + H2O
- NaOH + HNO3 → NaNO3 + H2O
- 2NaOH + H2SO4 → Na2SO4+ 2H2O
- 2NaOH + CuSO4 → Na2SO4+ Cu(OH)2 ↓
- 2NaOH + FeSO4 → Na2SO4 + Fe(OH)2 ↓
- 3NaOH + FeCl3 → 3NaCl+ Fe(OH)3 ↓
- 2NaOH + Mg(NO3)2 → 2NaNO3 + Mg(OH)2 ↓
- NaOH + Al(OH)3 → NaAlO2+ 2H2O
- NaOH + Cr(OH)3 → NaCrO2+ 2H2O
- 2NaOH + Zn(OH)2 ↓ → Na2ZnO2 (dd)+ 2H2O
- NaOH + NaHCO3 → Na2CO3 + H2O
- NaOH + NaHSO3 → Na2SO3 + H2O
- 2NaOH + Ba(HSO3)2 → Na2SO3 + BaSO3 ↓ + 2H2O
- 2NaOH + Ba(HCO3)2 → Na2CO3 + BaCO3 ↓ + 2H2O
- 2NaOH + Ca(HCO3)2 → Na2CO3 + CaCO3 ↓ + 2H2O
- 2NaOH + Ca(HSO3)2 → Na2SO3 + CaSO3 ↓ + 2H2O
- 6NaOH + 3Cl2 -90oC→ 5NaCl + NaClO3 + 3H2O
- 2NaOH + Al2O3 → 2NaAlO2 + H2O
- 2NaOH + ZnO → Na2ZnO2 + H2O
- 2NaOH + H2S → Na2S + 2H2O
- NaOH + H2S → NaHS + H2O
- NaOH + CH3COOH → CH3COONa + H2O
- NaOH + NH4Cl -to→ NaCl+ NH3 ↑ + H2O
- NaOH + NH4NO3 -to→ NaNO3+ NH3 ↑ + H2O
- 2NaOH + (NH4)2SO4 -to→ Na2SO4+ 2NH3 ↑ + 2H2O
- CH3COOCH3 + NaOH -H2O,to→ CH3COONa + CH3OH
- CH3COOC2H5 + NaOH -H2O,to→ CH3COONa + C2H5OH
- C2H5Cl + NaOH -to→ NaCl + C2H5OH
- C2H5Br + NaOH -to→ NaBr + C2H5OH
- C2H5Br + NaOH -toC2H5OH→ NaBr + C2H4 ↑ + H2O
- C2H5Cl + NaOH -toC2H5OH→ NaCl + C2H4 ↑ + H2O
- C6H5OH + NaOH → C6H5ONa + H2O
- 2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2 ↑
- Zn + 2NaOH -to→ Na2ZnO2 + H2 ↑
- NaOH + NaHS → Na2S + H2O
- 2NaOH + 2KHS → K2S + Na2S + 2H2O
- 2NaOH + 2KHSO3 → K2SO3 + Na2SO3 + 2H2O
- 2NaOH + 2KHCO3 → K2CO3 + Na2CO3 + 2H2O
- CH3COONa + NaOH -CaO,to→ CH4 ↑ + Na2CO3
- H2N-CH2-COOH + NaOH → H2N-CH2-COONa + H2O
- AlCl3 + 3NaOH → Al(OH)3 ↓ + 3NaCl
- ZnCl2 + 2NaOH → Zn(OH)2 ↓ + 2NaCl
- Si + 2NaOH + H2O → Na2SiO3 + 2H2 ↑
- SiO2 + 2NaOH -to→ Na2SiO3 + H2O
Sách VietJack thi THPT quốc gia 2025 cho học sinh 2k7:
- Đề thi lớp 1 (các môn học)
- Đề thi lớp 2 (các môn học)
- Đề thi lớp 3 (các môn học)
- Đề thi lớp 4 (các môn học)
- Đề thi lớp 5 (các môn học)
- Đề thi lớp 6 (các môn học)
- Đề thi lớp 7 (các môn học)
- Đề thi lớp 8 (các môn học)
- Đề thi lớp 9 (các môn học)
- Đề thi lớp 10 (các môn học)
- Đề thi lớp 11 (các môn học)
- Đề thi lớp 12 (các môn học)
- Giáo án lớp 1 (các môn học)
- Giáo án lớp 2 (các môn học)
- Giáo án lớp 3 (các môn học)
- Giáo án lớp 4 (các môn học)
- Giáo án lớp 5 (các môn học)
- Giáo án lớp 6 (các môn học)
- Giáo án lớp 7 (các môn học)
- Giáo án lớp 8 (các môn học)
- Giáo án lớp 9 (các môn học)
- Giáo án lớp 10 (các môn học)
- Giáo án lớp 11 (các môn học)
- Giáo án lớp 12 (các môn học)








 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp



