Giáo án Hóa 12 Kết nối tri thức Bài 27: Đại cương về kim loại chuyển tiếp dãy thứ nhất
Giáo án Hóa 12 Kết nối tri thức Bài 27: Đại cương về kim loại chuyển tiếp dãy thứ nhất
Chỉ từ 200k mua trọn bộ Kế hoạch bài dạy (KHBD) hay Giáo án Hóa học 12 Kết nối tri thức (cả năm) bản word chuẩn kiến thức, trình bày đẹp mắt, dễ dàng chỉnh sửa:
- B1: Gửi phí vào tk:
1133836868- CT TNHH DAU TU VA DV GD VIETJACK - Ngân hàng MB (QR) - B2: Nhắn tin tới Zalo VietJack Official - nhấn vào đây để thông báo và nhận giáo án
I. MỤC TIÊU
1. Kiến thức
- Nêu được đặc điểm cấu hình electron của nguyên tử kim loại chuyển tiếp dãy thứ nhất (từ Sc đến Cu).
- Trình bày được một số tính chất vật lí của kim loại chuyển tiếp (nhiệt độ nóng chảy, khối lượng riêng, độ dẫn điện và dẫn nhiệt, độ cứng) và ứng dụng của kim loại chuyển tiếp từ các tính chất đó.
- Nêu được sự khác biệt các số liệu về nhiệt độ nóng chảy, khối lượng riêng, độ dẫn điện, độ cứng,... giữa một số kim loại chuyển tiếp so với kim loại họ s.
- Nêu được xu hướng có nhiều số oxi hoá của nguyên tố chuyển tiếp.
- Nêu được các trạng thái oxi hoá phổ biến, cấu hình electron, đặc tính có màu của một số ion kim loại chuyển tiếp dãy thứ nhất.
2. Về năng lực
- Thực hiện được (hoặc quan sát video) thí nghiệm xác định hàm lượng muối Fe(II) bằng dung dịch thuốc tím.
- Thực hiện được thí nghiệm kiểm tra sự có mặt từng ion riêng biệt: Cu2+, Fe3+.
3. Về phẩm chất
- Sử dụng hợp lí, hiệu quả các kim loại phục vụ đời sống.
- Khơi dậy ý thức sử dụng tiết kiệm tài nguyên; thu gom, phân loại các đồ vật bằng kim loại sau khi hết hạn sử dụng để tái chế, bảo vệ môi trường.
II. THIẾT BỊ DẠY HỌC VÀ HỌC LIỆU
- Hình ảnh, video về ứng dụng của các kim loại chuyển tiếp dãy thứ nhất; màu sắc của các đơn chất và hợp chất.
- Video về thao tác chuẩn độ thuốc tím.
- Dụng cụ, hoá chất thí nghiệm theo hướng dẫn trong SGK.
III. TIẾN TRÌNH DẠY HỌC
1. Hoạt động 1: Mở đầu
1.1. Mục tiêu
- Huy động được vốn hiểu biết, kĩ năng có sẵn của học sinh về cấu tạo nguyên tử, cấu hình electron, phân loại nguyên tố, nguyên tắc sắp xếp trong bảng tuần hoàn để tìm hiểu về kim loại chuyển tiếp dãy thứ nhất.
- Kích thích sự tò mò, khơi dậy hứng thú của học sinh về chủ đề sẽ học; tạo không khí lớp học sôi nổi, chờ đợi, thích thú.
- Học sinh trải nghiệm qua tình huống có vấn đề, trong đó chứa đựng những nội dung kiến thức, những kĩ năng để phát triển phẩm chất, năng lực mới.
1.2. Nội dung
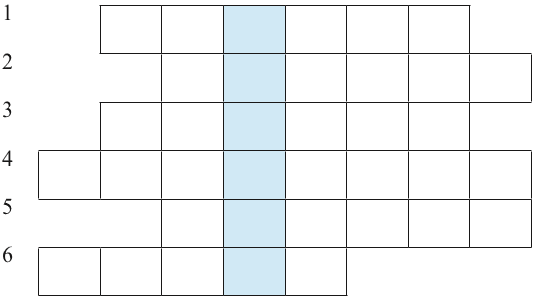
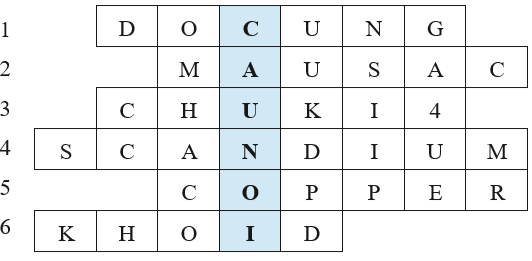
Giáo viên tổ chức cho học sinh trả lời câu hỏi để tìm các từ hàng ngang, cuối cùng xác định từ chìa khoá.
Câu 1: Do sở hữu tính chất vật lí nổi bật nào mà kim loại chromium được sử dụng để chế tạo hợp kim có độ bền cơ học cao?
Câu 2: Thuộc tính nào của cả vật thể và ánh sáng mà con người nhận biết được bằng mắt thường?
Câu 3: Các nguyên tố mà nguyên tử đều có 4 lớp electron được xếp ở chu kì nào trong bảng tuần hoàn?
Câu 4: Electron bắt đầu được điền vào phân lớp 3d ở lớp vỏ nguyên tử của nguyên tố nào?
Câu 5: Kim loại nào được dùng làm dây dẫn điện do có tính dẫn điện đứng thứ hai trong các kim loại?
Câu 6: Các nguyên tố mà nguyên tử có electron cuối cùng điền vào phân lớp d được xếp vào khối nào?
1.3. Sản phẩm
Kim loại chuyển tiếp là kim loại đóng vai trò trung gian, cầu nối giữa kim loại khối s (bên trái) và khối p (bên phải) trong bảng tuần hoàn.
1.4. Tổ chức thực hiện
- Giáo viên thiết kế các câu hỏi dạng trò chơi Quizizz, Rung chuông vàng,… để khởi động buổi học.
2. Hoạt động 2: Đơn chất kim loại chuyển tiếp dãy thứ nhất
2.1. Mục tiêu
- Nêu được đặc điểm cấu hình electron của nguyên tử kim loại chuyển tiếp dãy thứ nhất (từ Sc đến Cu).
- Trình bày được một số tính chất vật lí của kim loại chuyển tiếp (nhiệt độ nóng chảy, khối lượng riêng, độ dẫn điện và dẫn nhiệt, độ cứng) và ứng dụng của kim loại chuyển tiếp ứng từ các tính chất đó.
- Nêu được sự khác biệt các số liệu về nhiệt độ nóng chảy, khối lượng riêng, độ dẫn điện, độ cứng,... giữa một số kim loại chuyển tiếp so với kim loại họ s.
2.2. Nội dung
Nhiệm vụ 2.1: Viết cấu hình electron
Nguyên tố scandium, Sc (Z = 21) nằm ngay sau calcium và mở đầu cho các kim loại chuyển tiếp dãy thứ nhất.
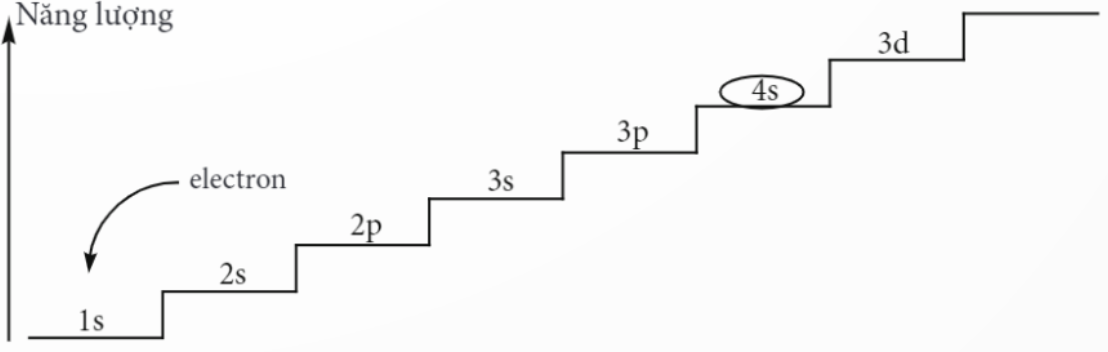
1. Điền electron của nguyên tử Sc vào các phân lớp theo thứ tự năng lượng sau:
Electron cuối cùng của nguyên tử Sc điền vào phân lớp nào? Nguyên tố Sc thuộc khối s, p, d hay f?
2. Sắp xếp lại các phân lớp sao cho thứ tự lớp tăng dần từ trái sang phải để thu được cấu hình electron của nguyên tử Sc ở dạng đầy đủ và dạng thu gọn.
3. Từ cấu hình electron thu gọn của Sc, hãy dự đoán cấu hình electron của nguyên tử Ti (Z = 22).
Nhiệm vụ 2.2: Đặc điểm cấu hình electron nguyên tử
Dựa vào thông tin ở Bảng 27.1 (SGK trang 129), thực hiện các yêu cầu sau:
1. Kim loại chuyển tiếp dãy thứ nhất gồm các kim loại nào? Chúng được xếp ở khối nào trong bảng tuần hoàn?
2. Nhận xét chung về cấu hình electron của nguyên tử kim loại chuyển tiếp dãy thứ nhất về:
a) Đặc điểm giống nhau và khác nhau trong cấu hình electron nguyên tử.
b) Sự biến đổi số electron trên phân lớp 3d và 4s.
Nhiệm vụ 2.3: Tính chất vật lí
1. Dựa vào số liệu ở Bảng 27.2 (SGK trang 130) để liệt kê các kim loại tương ứng vào chỗ trống trong bảng sau.
|
Kim loại dễ nóng chảy hơn Be ...................................................................... |
Kim loại khó nóng chảy hơn Be ...................................................................... |
|
Kim loại nhẹ ...................................................................... |
Kim loại nặng ...................................................................... |
|
Kim loại dẫn điện kém nhất ...................................................................... |
Kim loại dẫn điện tốt nhất ...................................................................... |
|
Kim loại dẫn nhiệt kém nhất ...................................................................... |
Kim loại dẫn nhiệt tốt nhất ...................................................................... |
|
Kim loại có độ cứng thấp nhất ...................................................................... |
Kim loại có độ cứng cao nhất ...................................................................... |
................................
................................
................................
(Nguồn: NXB Giáo dục)
Trên đây tóm tắt một số nội dung miễn phí trong bộ Kế hoạch bài dạy (KHBD) hay Giáo án Hóa học 12 Kết nối tri thức năm 2026 mới nhất, để mua tài liệu đầy đủ, Thầy/Cô vui lòng xem thử:
Xem thêm các bài soạn Giáo án Hóa học lớp 12 Kết nối tri thức chuẩn khác:
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Giáo án lớp 12 (các môn học)
- Giáo án điện tử lớp 12 (các môn học)
- Giáo án Toán 12
- Giáo án Ngữ văn 12
- Giáo án Vật Lí 12
- Giáo án Hóa học 12
- Giáo án Sinh học 12
- Giáo án Địa Lí 12
- Giáo án Lịch Sử 12
- Giáo án Lịch Sử 12 mới
- Giáo án GDCD 12
- Giáo án Kinh tế Pháp luật 12
- Giáo án Tin học 12
- Giáo án Công nghệ 12
- Giáo án GDQP 12
- Đề thi lớp 12 (các môn học)
- Đề thi Ngữ văn 12
- Đề thi Toán 12
- Đề thi Tiếng Anh 12 mới
- Đề thi Tiếng Anh 12
- Đề thi Vật Lí 12
- Đề thi Hóa học 12
- Đề thi Sinh học 12
- Đề thi Địa Lí 12
- Đề thi Lịch Sử 12
- Đề thi Giáo dục Kinh tế Pháp luật 12
- Đề thi Giáo dục quốc phòng 12
- Đề thi Tin học 12
- Đề thi Công nghệ 12






 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

