SO2 + O2 → SO3 | SO2 ra SO3
Phản ứng SO2 + O2 ra SO3 thuộc loại phản ứng oxi hóa khử đã được cân bằng chính xác và chi tiết nhất. Bên cạnh đó là một số bài tập có liên quan về SO2 có lời giải, mời các bạn đón xem:
2SO2 + O2 2SO3
1. Phương trình hóa học của phản ứng SO2 tác dụng với O2
2SO2 + O2 2SO3
2. Điều kiện để SO2 tác dụng với O2
Oxi hóa SO2 bằng khí oxi hoặc không khí dư ở nhiệt độ 450 - 500oC, chất xúc tác vanađi (V) oxit V2O5.
3. Mở rộng kiến thức về SO2
3.1. Tính chất vật lí
- Là không màu, mùi hắc, nặng hơn không khí (d = )
- Tan nhiều trong nước (ở 20oC, một thể tích nước có thể hòa tan được 40 thể tích SO2).
- Hóa lỏng ở -10oC.
- Là khí độc, hít thở phải không khí có khí này sẽ gây viêm đường hô hấp.
3.2. Tính chất hóa học
a. Lưu huỳnh đioxit là acidic oxide
- SO2 tan trong nước tạo thành axit yếu và không bền:
SO2 + H2O ⇆ H2SO3
- SO2 tác dụng với dd bazơ tạo nên 2 loại muối: muối axit HSO3-, muối trung hòa SO32-.
SO2 + NaOH →NaHSO3(1)
SO2 + 2NaOH→ Na2SO3 + H2O (2)
+ Nếu : chỉ xảy ra phản ứng (1)
+ Nếu 1 < < 2: xảy ra cả phản ứng (1) và (2)
+ Nếu : chỉ xảy ra phản ứng (2)
b. Lưu huỳnh đioxit là chất khử và là chất oxi hóa
(*)SO2 là chất khử
Khi gặp chất oxi hóa mạnh như O2 , Cl2 , Br2 : khí SO2 đóng vai trò là chất khử:
SO2 + Br2 + 2H2O → 2HBr + H2SO4
5SO2 + 2KMnO4 + 2H2O → K2SO4 + 2MnSO4 + 2H2SO4
(*) SO2 là chất oxi hoákhi tác dụng chất khử mạnh:
SO2 + 2H2S → 2H2O + 3S
3.3. Ứng dụng và điều chế sulfur dioxide
a. Ứng dụng
- Sản xuất axit sunfuric trong công nghiệp
- Tấy trắng giấy, bột giấy.
- Chống nấm mốc cho lương thực, thực phẩm …
b. Điều chế
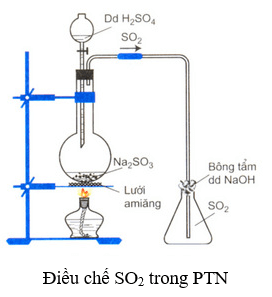
- Trong phòng thí nghiệm:Đun nóng dd H2SO4 với muối Na2SO3, sau đó thu SO2 bằng cách đẩy không khí. Phương trình hóa học:
Na2SO3 + H2SO4 → Na2SO4 + H2O + SO2
- Trong công nghiệp
Đốt cháy S hoặc đốt cháy quặng pirit sắt:
4FeS2 + 11O2 2Fe2O3 + 8SO2
4. Mở rộng kiến thức về sulfur trioxide (SO3)
a. Tính chất
- Ở điều kiện thường, SO3 là chất lỏng không màu, tan vô hạn trong nước và trong axit H2SO4, tnc=17oC, tsôi = 45oC.
- sulfur trioxide là một acidic oxide:
+ Tác dụng với H2O tạo axit sunfuric: SO3 + H2O → H2SO4
+ Tác dụng với bazơ, basic oxidetạo muối sunfat:
SO3 + 2NaOH → Na2SO4 + H2O
SO3 + Na2O → Na2SO4
b. Ứng dụng và sản xuất
- Trong thực tiễn, SO3 có ít ứng dụng nhưng nó là sản phẩm trung gian để sản xuất axit H2SO4.
- Trong công nghiệp, người ta sản xuất SO3 bằng cách oxi hóa SO2 ở nhiệt độ cao 450o – 500oC, xúc tác V2O5
2SO2 + O2 2SO3
5. Bài tập vận dụng liên quan
Câu 1:Hòa tan 8,36g oleum vào nước được dung dịch Y, để trung hòa dung dịch Y cần 200 ml dung dịch NaOH 1M. Công thức phân tử của oleum:
A. H2SO4. nSO3
B. H2SO4.3SO3
C. H2SO4. 5SO3
D. H2SO4. 4SO3
Hướng dẫn giải:
Đáp án D
Gọi công thức phân tử của oleum là: H2SO4.nSO3
H2SO4.nSO3 + nH2O → (n+1) H2SO4 (1)
← 0,1 mol
Dung dịch Y là dung dịch H2SO4
H2SO4 + 2 NaOH → Na2SO4 + 2H2O (2)
0,1 mol ← 0,2 mol
→ n = 4 → CTPT của oleum: H2SO4.4SO3
Câu 2:SO2 luôn thể hiện tính khử trong các phản ứng với
A. H2S, nước Br2, O2
B. dung dịch NaOH, O2, dung dịch KMnO4
C. dung dịch KOH, CaO, nước Br2
D. O2, nước Br2, dung dịch KMnO4
Hướng dẫn giải:
Đáp án D
A loại H2S vì H2S là chất có tính khử nên khi phản ứng với H2S thì SO2 thể hiện tính oxi hóa.
B loại NaOH vì phản ứng giữa SO2 và NaOH không phải là phản ứng oxi hóa khử
C loại KOH vì phản ứng giữa SO2 và KOH không phải là phản ứng oxi hóa khử
D đúng
Các phản ứng là:
2SO2 + O2 2SO3
SO2 + Br2 + 2H2O → 2HBr + H2SO4
5SO2 + 2KMnO4 + 2H2O → K2SO4 + 2MnSO4 + 2H2SO4
Câu 3:Hấp thụ hoàn toàn 2,24 lít khí SO2 (đkc) vào 100 ml dung dịch NaOH 1,5M. Muối thu được gồm:
A. Na2SO4
B. NaHSO3
C. Na2SO3
D. NaHSO3 và Na2SO3
Hướng dẫn giải:
Đáp án D
Ta có:
Nên muối thu được gồm: NaHSO3 và Na2SO3
Câu 4:Thể tích dung dịch NaOH 2M tối thiểu để hấp thụ hết 5,6 lít khí SO2 (đkc) là:
A. 250 ml
B. 500 ml
C. 125 ml
D. 175 ml
Hướng dẫn giải:
Đáp án C
Vì NaOH tối thiểu cần dùng nên chỉ xảy ra phản ứng tạo NaHSO3 (tỉ lệ NaOH : SO2 =1:1)
NaOH + SO2 → NaHSO3
Vdd NaOH = 0,125 (lít) = 125 (ml)
Câu 5: Đốt cháy hoàn toàn 4,8 gam lưu huỳnh rồi cho sản phẩm cháy hấp thụ hoàn toàn vào 200 ml dung dịch Ba(OH)2 0,5M. Khối lượng kết tủa thu được là:
A. 10,85 gam
B. 16,725 gam
C. 21,7 gam
D. 32,55 gam
Hướng dẫn giải:
Đáp án A
nS = 0,15 (mol)
S + O2 SO2
Theo PTHH:
Ta có tỉ lệ:
→ Thu được 2 muối: BaSO3 và Ba(HSO3)2
SO2 + Ba(OH)2 → BaSO3 + H2O
x →x→x (mol)
2SO2 + Ba(OH)2 → Ba(HSO3)2
2y→y→ y (mol)
Ta có hệ phương trình:
Giải hệ phương trình
Vậy
Câu 6:Cho sản phẩm khí thu được khi đốt cháy 17,92 lít khí H2S (đktc) sục vào 200 ml dung dịch NaOH 25% (d = 1,28g/ml). Tính nồng độ phần trăm muối trong dung dịch ?
A. 32,81%
B. 23,81%
C. 18,23%
D. 18,32%
Hướng dẫn giải:
Đáp án A
BTNT “S”:
m dd NaOH = 200.1,28 = 256 gam
→ mNaOH = 256.25% = 64 gam
→ nNaOH = 1,6 mol
→ Muối sinh ra là Na2SO3
2NaOH + SO2 → Na2SO3 + H2O
Theo PTHH:
Khối lượng dung dịch sau phản ứng :
m dd sau pư = 256 + 0,8.64 = 307,2 gam
Vậy
Câu 7: Dẫn V lít khí SO2 vào dung dịch nước Br2 dư thu được dung dịch X. Cho thêm dung dịch BaCl2 cho đến khi kết tủa đạt cực đại thì dừng lại. Lọc kết tủa và sấy khô thu được 1,165 gam chất rắn. V có giá trị là:
A. 0,112 lít.
B. 0,224 lít.
C. 0,336 lít.
D. 0,448 lít.
Hướng dẫn giải:
Đáp án A
Chất rắn sau khi sấy khô là BaSO4:
SO2 + Br2 +2H2O → H2SO4 + 2HBr
BaCl2 + H2SO4 → BaSO4 ↓ + 2HCl
Mà
lít
Câu 8: Hấp thụ hoàn toàn 3,36 lít SO2 (đktc) vào 125 ml Ba(OH)2 1M thì thu được dung dịch X (coi thể tích dung dịch không đổi). Tính nồng độ chất tan trong dung dịch X
A. 0,4M
B. 0,2M.
C.0,6M
D. 0,8M
Hướng dẫn giải:
Đáp án B
sinh ra hỗn hợp muối BaSO3 và Ba(HSO3)2
Gọi số mol BaSO3 và Ba(HSO3)2 lần lượt là x,y
SO2 + Ba(OH)2 → BaSO3 + H2O
x x x
2SO2 + Ba(OH)2 → Ba(HSO3)2
2y y y
Câu 9: Hấp thụ hoàn toàn 2,688 lít khí SO2(đktc) vào 2,5 lít Ba(OH)2 nồng độ a M. Thu được 17,36 gam kết tủa. Giá trị của a là
A. 0,04.
B. 0,03.
C. 0,048.
D. 0,43.
Hướng dẫn giải:
Đáp án A
Bảo toàn nguyên tố S:
Bảo toàn nguyên tố Ba:
Câu 10: Biết V lít SO2 (đktc) tác dụng với 500ml dung dịch Ca(OH)2 0,5M tạo thành 12 gam kết tủa.Tìm giá trị lớn nhất của V?
A. 2,24.
B. 3,36.
C. 4,48.
D.8,96.
Hướng dẫn giải:
Đáp án D
Ta có:
Giá trị Vmax khi sinh ra hỗn hợp muối CaSO3 và Ca(HSO3)2
Bảo toàn nguyên tố Ca:
Bảo toàn nguyên tố S:
Câu 11: Dẫn V lít khí SO2 (ở đktc) qua 500 ml dung dịch Ca(OH)2 nồng độ x M , sau phản ứng thu được 3,6 gam kết tủa và dung dịch A. Đun nóng dung dịch A thu được thêm 2,4 gam kết tủa nữa. Giá trị của V và x là
A. 1,568 lít và 0,1 M
B. 22,4 lít và 0,05 M.
C. 0,1792 lít và 0,1 M
D. 1,12 lít và 0,2 M.
Hướng dẫn giải:
Đáp án A
Đun nóng dung dịch A thu được thêm kết tủa → có muối Ca(HSO3)2
Bảo toàn nguyên tố S:
Bảo toàn nguyên tố Ca:
mol
Câu 12: Hóa chất dùng để phân biệt CO2 và SO2 là
A. nước brom
B. Bari hiđroxit
C. phenolphtalein
D. dung dịch nước vôi trong.
Hướng dẫn giải:
Đáp án A
SO2 làm mất màu nước brom còn CO2 thì không
SO2 + Br2+ 2 H2O → 2 HBr + H2SO4
Câu 13: Cho các phản ứng sau:
a) 2SO2 + O2 2SO3
b) SO2 + 2H2S 3S + 2H2O
c) SO2 + Br2 + 2H2O → H2SO4 + 2HBr
d) SO2 + NaOH → NaHSO3
Các phản ứng mà SO2 có tính khử là:
A. a, c, d
B. a, b, d
C. a, c
D. a, d
Hướng dẫn giải:
Đáp án C
a/ 2SO2 + O2 2SO3
c/ SO2 + Br2 + 2H2O → H2SO4 + 2HBr
Trong hai phản ứng a và c, số oxi hóa của S trong SO2 tăng từ +4 lên +6 do đó SO2 thể hiện tính khử.
Câu 14: Hấp thụ hoàn toàn 1,12 lít khí SO2 (đktc) vào 150 ml dung dịch NaOH 1M. Cô cạn dung dịch thu được
A. hỗn hợp hai muối NaHSO3, Na2SO3 và NaOH dư
B. Hỗn hợp 2 chất NaOH, Na2SO3
C. Hỗn hợp hai chất SO2 dư, NaOH
D. Hỗn hợp hai muối NaHSO3, Na2SO3
Hướng dẫn giải:
Đáp án B
= 0,05 mol,n NaOH = 0,15 mol
Vì> 2→ chỉ tạo 1 muối là Na2SO3
SO2 + 2 NaOH → Na2SO3 + H2O
0,05 0,15 → 0,05
→ NaOH dư sau phản ứng
→ Dung dịch chứa 2 chất NaOH, Na2SO3
Câu 15:Cho V lít SO2 (đktc) tác dụng hết với dung dịch Br2 dư. Thêm tiếp vào dung dịch sau phản ứng BaCl2 dư thu được 2,33 gam kết tủa. Thể tích V là:
A. 0,112 lít
B. 1,12 lít
C. 0,224 lít
D. 2,24 lít
Hướng dẫn giải:
Đáp án C
.
Xem thêm các phương trình hóa học hay khác:
- H2S + CuSO4 → CuS↓ + H2SO4
- H2S + H2SO4 đậm đặc → SO2↑+ 2H2O + S↓
- 2H2S + 3O2 2SO2↑ + 2H2O
- H2S + 4Cl2 + 4H2O → H2SO4 + 8HCl
- S + O2 SO2
- H2S + 2NaOH → Na2S + 2H2O
- S + 6HNO3 → H2SO4 + 6NO2↑+ 2H2O
- H2S + NaOH → NaHS + H2O
- S + 2H2SO4 đặc 3SO2↑+ 2H2O
- 3H2S + 2HNO3 → 4H2O + 2NO↑ + 3S↓
- S + H2 H2S
- SO2 + Na2O Na2SO3
- SO2 + 2KOH → K2SO3 + H2O
- SO2 + H2S → 3S↓ + 2H2O
- 2SO2 + 2NaH → H2S↑ + Na2SO4
- SO2 + Br2 + 2H2O →H2SO4 + 2HBr
- SO2 + Cl2 + 2H2O → 2HCl + H2SO4
- 2SO2 + O2 + 2H2O → 2H2SO4
- 5SO2 + 2KMnO4 + 2H2O → 2MnSO4 + K2SO4 + 2H2SO4
- SO3 + H2O → H2SO4
- H2S + 2FeCl3 → S↓ + 2FeCl2 + 2HCl
- 3H2S + 2KMnO4 → 2KOH + 2MnO2↓ + 3S↓ + 2H2O
- H2S + 4Br2 + 4H2O → 8HBr + H2SO4
- SO2 + Ca(OH)2 → CaSO3↓ + H2O
Sách VietJack thi THPT quốc gia 2025 cho học sinh 2k7:
- Đề thi lớp 1 (các môn học)
- Đề thi lớp 2 (các môn học)
- Đề thi lớp 3 (các môn học)
- Đề thi lớp 4 (các môn học)
- Đề thi lớp 5 (các môn học)
- Đề thi lớp 6 (các môn học)
- Đề thi lớp 7 (các môn học)
- Đề thi lớp 8 (các môn học)
- Đề thi lớp 9 (các môn học)
- Đề thi lớp 10 (các môn học)
- Đề thi lớp 11 (các môn học)
- Đề thi lớp 12 (các môn học)
- Giáo án lớp 1 (các môn học)
- Giáo án lớp 2 (các môn học)
- Giáo án lớp 3 (các môn học)
- Giáo án lớp 4 (các môn học)
- Giáo án lớp 5 (các môn học)
- Giáo án lớp 6 (các môn học)
- Giáo án lớp 7 (các môn học)
- Giáo án lớp 8 (các môn học)
- Giáo án lớp 9 (các môn học)
- Giáo án lớp 10 (các môn học)
- Giáo án lớp 11 (các môn học)
- Giáo án lớp 12 (các môn học)








 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp



