Công thức bảo toàn số mol liên kết pi (hay, chi tiết)
Bài viết Công thức bảo toàn số mol liên kết pi hay nhất, chi tiết với bài tập minh họa có lời giải sẽ giúp học sinh nắm vững Công thức bảo toàn số mol liên kết pi từ đó biết cách làm bài tập về bảo toàn số mol liên kết pi.
Công thức bảo toàn số mol liên kết pi (hay, chi tiết)
Trong chương trình hóa học, chủ đề bảo toàn liên kết pi trong phản ứng cộng là phần kiến thức quan trọng giúp học sinh giải được nhiều bài toán khó. Bài viết dưới đây, đưa ra phương pháp chung để giải nhanh các bài tập hydrocarbon không no tác dụng với hiđro và brom. Bài viết sẽ giúp bạn đọc nâng cao khả năng giải bài tập nhanh và chính xác thông tiếp cận, làm quen với phương pháp này để đem lại hiệu quả học tập cao hơn.
1. Công thức bảo toàn số mol liên kết pi
Đối với các bài toán cộng Br2, H2 vào hydrocarbon không no thì nên áp dụng bảo toàn số mol liên kết π .
Hydrocarbon không no, mạch hở có k liên kết pi có công thức là CnH2n + 2 - 2k thì:
+ Số mol liên kết = nphân tử hydrocarbon?/sub> . số liên kết π = nphân tử hydrocarbon?/sub> .k
+ Số mol liên kết
Cách tính số liên kết π đối với hydrocarbon không no, mạch hở CxHy là:
Số liên kết
2. Bạn nên biết
Liên kết đôi C=C gồm một liên kết σ và một liên kết π; liên kết ba C ≡ C gồm một liên kết σ và hai liên kết π. Liên kết π kém bền hơn liên kết σ nên các alkene, alkyne dễ dàng tham gia phản ứng cộng tạo thành hợp chất no tương ứng.
*Phản ứng cộng H2
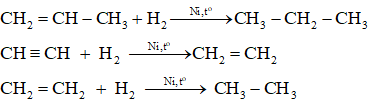
Khi đun nóng có kim loại niken (hoặc platin hoặc palađi) làm xúc tác, alkene và alkyne kết hợp với hiđro tạo thành alkane tương ứng.
Thí dụ :
Khi dùng xúc tác là hỗn hợp Pd/Pb CO3, hoặc Pd/BaSO4, alkyne chỉ cộng một phân tử hiđro tạo thành alkene.
⇒ Đặc tính này được dùng để điều chế alkene từ alkyne.
*Phản ứng cộng brom
Các alkene và alkyne làm mất màu dung dịch nước brom.
⇒Đây là một trong những phản ứng nhận biết hydrocarbon không no.
3. Mở rộng bảo toàn số mol liên kết pi
Đa phần các bài toán về phản ứng cộng sẽ kết hợp cả phản ứng cộng hiđro với cộng brom.
Bài toán có dạng: Nung nóng hỗn hợp khí X gồm H2 và hydrocarbon không no một thời gian với xúc tác Ni thu được hỗn hợp khí Y (thường cho biết tỉ khối). Dẫn hỗn hợp Y qua dung dịch nước brom dư.
Phương pháp giải:
+ Bảo toàn khối lượng: Mx = My
+ Bảo toàn số mol liên kết π : Số mol liên kết
4. Bài tập minh họa bảo toàn số mol liên kết pi
Bài 1 : Hỗn hợp X gồm 0,15 mol vinylacetylene và 0,6 mol H2. Nung nóng hỗn hợp X (xúc tác Ni) một thời gian, thu được hỗn hợp Y có tỉ khối so với H2 bằng 10. Dẫn hỗn hợp Y qua dung dịch brom dư, sau khi phản ứng xảy ra hoàn toàn, khối lượng brom tham gia phản ứng là
A. 12 gam.
B. 24 gam.
C. 8 gam.
D. 16 gam.
Hướng dẫn giải
Ta có: vinylacetylene có công thức là C4H4 ⇒ có 3 liên kết π
Bảo toàn khối lượng ta có:
Độ giảm số mol chính là số mol mà H2 phản ứng ⇒ nH2Pu = 0,75 - 0,45 = 0,3 mol
Áp dụng bảo toàn số mol liên kết π ta có:
Đáp án B
Câu 2: Hỗn hợp khí X gồm 0,5 mol H2 và 0,15 mol vinylacetylene. Nung X một thời gian với xúc tác Ni thu được hỗn hợp Y có tỉ khối so với bằng d. Dẫn hỗn hợp Y qua dung dịch brom dư, sau khi phản ứng xảy ra hoàn toàn, khối lượng brom tham gia phản ứng là 16 gam. Giá trị của d là
A. 29,33.
B. 14,67.
C. 13,54.
C. 6,77.
Hướng dẫn giải
Ta có: vinylacetylene có công thức là C4H4 ⇒ có 3 liên kết π
Áp dụng bảo toàn số mol liên kết π ta có:
Bảo toàn khối lượng ta có:
Đáp án B
Câu 3: Hỗn hợp khí A gồm 0,4 mol và 0,2 mol alkyne X. Nung A một thời gian với xúc tác Ni thu được hỗn hợp B có tỉ khối so với bằng 12. Dẫn hỗn hợp B qua dung dịch brom dư, sau khi phản ứng xảy ra hoàn toàn, khối lượng brom tham gia phản ứng là 8 gam. Công thức phân tử của X là
A. C3H4
B. C2H4
C. C4H6
D. C2H2
Hướng dẫn giải
Gọi công thức tổng quát của alkyne X là .CnH2n - 2 (n > 2)
Áp dụng bảo toàn số mol liên kết π ta có:
Bảo toàn khối lượng ta có:
Vậy công thức phân tử của X là C2H2
Đáp án D
Xem thêm các Công thức Hóa học lớp 11 quan trọng hay khác:
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Đề thi lớp 1 (các môn học)
- Đề thi lớp 2 (các môn học)
- Đề thi lớp 3 (các môn học)
- Đề thi lớp 4 (các môn học)
- Đề thi lớp 5 (các môn học)
- Đề thi lớp 6 (các môn học)
- Đề thi lớp 7 (các môn học)
- Đề thi lớp 8 (các môn học)
- Đề thi lớp 9 (các môn học)
- Đề thi lớp 10 (các môn học)
- Đề thi lớp 11 (các môn học)
- Đề thi lớp 12 (các môn học)
- Giáo án lớp 1 (các môn học)
- Giáo án lớp 2 (các môn học)
- Giáo án lớp 3 (các môn học)
- Giáo án lớp 4 (các môn học)
- Giáo án lớp 5 (các môn học)
- Giáo án lớp 6 (các môn học)
- Giáo án lớp 7 (các môn học)
- Giáo án lớp 8 (các môn học)
- Giáo án lớp 9 (các môn học)
- Giáo án lớp 10 (các môn học)
- Giáo án lớp 11 (các môn học)
- Giáo án lớp 12 (các môn học)

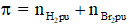
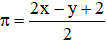
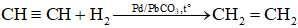
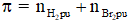
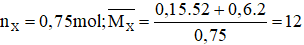
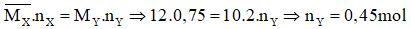
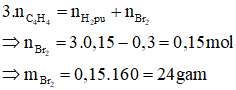
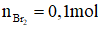
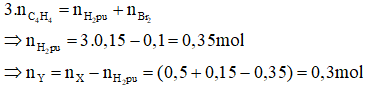
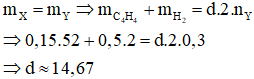
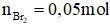
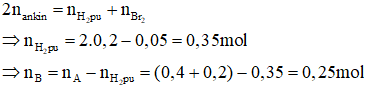
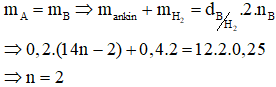





 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

