Công thức tính hằng số phân li axit (hay, chi tiết)
Bài viết Công thức tính hằng số phân li axit hay nhất, chi tiết với bài tập minh họa có lời giải sẽ giúp học sinh nắm vững Công thức tính hằng số phân li axit từ đó biết cách làm bài tập về tính hằng số phân li axit.
Công thức tính hằng số phân li axit (hay, chi tiết)
Sự điện li của axit yếu trong nước là quá trình thuận nghịch. Vậy có đại lượng nào đánh giá lực của axit đó hay không? Để có câu trả lời, các em hãy tham khảo bài viết dưới đây.
1. Công thức hằng số phân li axit
Xét cân bằng: CH3COOH ⇄ H- + CH3COO-
Vì nồng độ của nước được coi như hằng số nên ta có thể bỏ qua nồng độ của nước trong biểu thức xác định hằng số
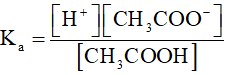
2. Bạn nên biết
- Đối với axit nhiều nấc sẽ có nhiều hằng số phân li ở các nấc khác nhau.
- Hằng số phân li axit chỉ phụ thuộc vào bản chất axit và nhiệt.
- Giá trị Ka càng nhỏ thì lực axit của nó càng yếu (hay tính axit càng yếu).
3. Mở rộng tính hằng số phân li axit
Mối liên hệ giữa hằng số Ka và Kb
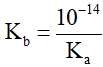 hay Ka.Kb =10-14
hay Ka.Kb =10-14
4. Bài tập minh họa tính hằng số phân li axit
Câu 1: Trong 2 lít dung dịch axit flohidric có chứa 4 gam HF nguyên chất. Độ điện li của axit này là 8%. Tính hằng số phân li của axit HF?
A. 6,96.10-4
B. 7,96.10-4
C. 6,96.10-3
D. 6,96.10-3
Hướng dẫn
nHF = 0,2 mol => [HF] =0,1 M
HF <=> H+ + F-
Bd 0,1
Pli x x x
CB 0,1-x x x(M)
∝ = 8% = x/ 0,1 => x= 8.10-3M
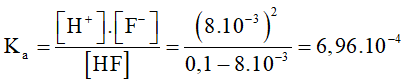
Đáp án A
Câu 2: Tính nồng độ ion H+ của dung dịch CH3COOH 0,1M, biết hằng số phân li của axit Ka= 1,75.10-5?
A. 2,32.10-3
B. 1,32.10-3
C. 2,52.10-3
D. 1,52.10-3
Hướng dẫn
Ta có:
CH3COOH ⇄ CH3COO- + H+
Ban đầu: 0,1 0 0
Phân li: x x x
Cân bằng: 0,1 - x x x (M)
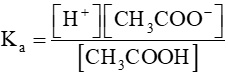
=> 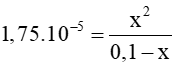
Vì CH3COOH là axit yếu → x << 0,1→ 0,1−x ≈ 0,1
=> 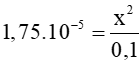
=> x= 1,32.10-3
Vậy [H+]=1,32.10-3M
Đáp án B
Câu 3: Cho dung dịch HCOOH 0,1M ở 25 có độ điện li là 4,3%. Tính hằng số phần li của HCOOH là:
A. 1,932.10-4
B. 1,732. 10-4
C. 1,932. 10-3
D. 1,732. 10-3
Hướng dẫn
HCOOH ⇄ HCOO- + H+
Bd 0,1
Pli 0,1∝ 0,1∝ 0,1∝
CB 0,1(1-∝) 0.1∝ 0,1∝
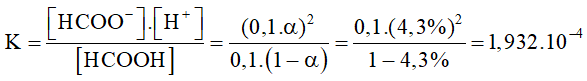
Đáp án A
Xem thêm các Công thức Hóa học lớp 11 quan trọng hay khác:
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Đề thi lớp 1 (các môn học)
- Đề thi lớp 2 (các môn học)
- Đề thi lớp 3 (các môn học)
- Đề thi lớp 4 (các môn học)
- Đề thi lớp 5 (các môn học)
- Đề thi lớp 6 (các môn học)
- Đề thi lớp 7 (các môn học)
- Đề thi lớp 8 (các môn học)
- Đề thi lớp 9 (các môn học)
- Đề thi lớp 10 (các môn học)
- Đề thi lớp 11 (các môn học)
- Đề thi lớp 12 (các môn học)
- Giáo án lớp 1 (các môn học)
- Giáo án lớp 2 (các môn học)
- Giáo án lớp 3 (các môn học)
- Giáo án lớp 4 (các môn học)
- Giáo án lớp 5 (các môn học)
- Giáo án lớp 6 (các môn học)
- Giáo án lớp 7 (các môn học)
- Giáo án lớp 8 (các môn học)
- Giáo án lớp 9 (các môn học)
- Giáo án lớp 10 (các môn học)
- Giáo án lớp 11 (các môn học)
- Giáo án lớp 12 (các môn học)






 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

