Công thức tính % khối lượng các nguyên tố trong hợp chất hữu cơ (hay, chi tiết)
Bài viết Công thức tính % khối lượng các nguyên tố trong hợp chất hữu cơ hay nhất, chi tiết với bài tập minh họa có lời giải sẽ giúp học sinh nắm vững Công thức tính % khối lượng các nguyên tố trong hợp chất hữu cơ từ đó biết cách làm bài tập về tính % khối lượng các nguyên tố trong hợp chất hữu cơ.
Công thức tính % khối lượng các nguyên tố trong hợp chất hữu cơ (hay, chi tiết)
Phân tích định tính nguyên tố nhằm xác định các nguyên tố có mặt trong hợp chất hữu cơ bằng cách phân huỷ hợp chất hữu cơ thành các hợp chất vô cơ đơn giản rồi nhận biết chúng bằng các phản ứng đặc trưng.Từ kết quả phân tích, người ta xác định được hàm lượng phần trăm nguyên tố trong hỗn hợp. Các bạn hãy tham khảo bài viết bên dưới để biết cách tính phần trăm khối lượng các nguyên tố nhé.
1. Công thức tính % khối lượng các nguyên tố trong hợp chất hữu cơ
Gọi công thức đơn giản nhất (CTĐGN) của hợp chất hữu cơ X là CxHyOzNt (x, y, z, t nguyên dương).
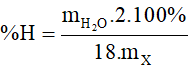
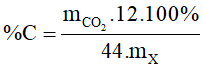
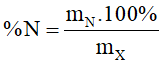 hay
hay 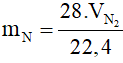
Ta có hệ quả sau:
x: y: z: t= 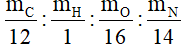
Hoặc x: y: z: t = 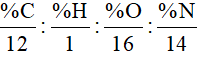
2. Bạn nên biết
- Công thức phân tử cho biết số nguyên tử của các nguyên tố có trong phân tử. - ---- Công thức đơn giản nhất cho biết tỉ lệ số nguyên tử của các nguyên tố có trong phân tử (biểu diễn bằng tỉ lệ các số nguyên tối giản).
- Công thức phân tử (chẳng hạn CxHyOzNt) có thể trùng hoặc là bội số của công thức đơn giản nhất (CpHqOrNs):
CxHyOzNt =(CpHqOrNs)n , n có thể là 1 hoặc 2, 3,...
x : y : z : t = p : q : r : s
3. Bài tập minh họa tính % khối lượng các nguyên tố trong hợp chất hữu cơ
Câu 1: Một hợp chất hữu cơ gồm C, H, O trong đó cacbon chiếm 61,22% về khối lượng. Công thức phân tử của hợp chất là
A. C4H10O
B. C5H6O2
C. C3H6O2
D. C2H2O3
Hướng dẫn
Đặt công thức phân tử có dạng
Ta có :
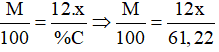
=> M= 19,6x
=> x=5, M=98
Đáp án B
Câu 2: Thành phần % của C, H, O trong hợp chất Z lần lượt là 54,6%; 9,1%; 36,3%. Công thức đơn giản nhất của Z là:
A. C2H4O
B. C2H4O2
C. C3H6O
D. C3H6O2
Hướng dẫn
Gọi công thức đơn giản nhất của Z là CxHyOz
Ta có:
x: y: z= 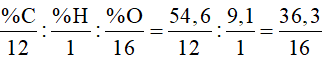
=> x: y: z = 2: 4: 1
Vậy công thức đơn giản nhất của Z là C2H4O
Đáp án A
Câu 3: Nicotin là chất độc gây nghiện có nhiều trong cây thuốc lá. Khói thuốc là có rất nhiều chất độc không những gây hại cho người hút mà còn ảnh hưởng đến những người xung quanh gây ra các bệnh hiểm nghèo như ung thư phổi, ung thư vòm họng... Thành phần phần trăm khối lượng các nguyên tố trong nicotin như sau: 74,07%C, 17,28%N, 8,64%H. Tỉ khối hơi của nicotin so với Heli (M = 4) là 40,5. Công thức phân tử của nicotin là
A. C8H10N2O.
B. C10H14N2O.
C. C10H14N2.
D. C5H7N.
Hướng dẫn
Nhận thấy %mC + %mH + %mN = 100% ⇒ Không có Oxi ⇒ Loại A và B.
Gọi công thức đơn giản nhất (CTĐGN) của nicotin có dạng: CxHyNt
x: y: t = 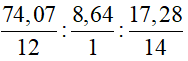 = 5: 7: 1
= 5: 7: 1
⇒ CTĐGN là (C5H7N)n. Với M[(C5H7N)n] = 40,5 × 4 = 162.
⇒ 81n = 162 ⇒ n = 2
⇒ CTPT là C10H14N2
⇒ Chọn C
Xem thêm các Công thức Hóa học lớp 11 quan trọng hay khác:
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Đề thi lớp 1 (các môn học)
- Đề thi lớp 2 (các môn học)
- Đề thi lớp 3 (các môn học)
- Đề thi lớp 4 (các môn học)
- Đề thi lớp 5 (các môn học)
- Đề thi lớp 6 (các môn học)
- Đề thi lớp 7 (các môn học)
- Đề thi lớp 8 (các môn học)
- Đề thi lớp 9 (các môn học)
- Đề thi lớp 10 (các môn học)
- Đề thi lớp 11 (các môn học)
- Đề thi lớp 12 (các môn học)
- Giáo án lớp 1 (các môn học)
- Giáo án lớp 2 (các môn học)
- Giáo án lớp 3 (các môn học)
- Giáo án lớp 4 (các môn học)
- Giáo án lớp 5 (các môn học)
- Giáo án lớp 6 (các môn học)
- Giáo án lớp 7 (các môn học)
- Giáo án lớp 8 (các môn học)
- Giáo án lớp 9 (các môn học)
- Giáo án lớp 10 (các môn học)
- Giáo án lớp 11 (các môn học)
- Giáo án lớp 12 (các môn học)






 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

