Đề kiểm tra 15 phút Hóa 11 Học kì 1 có đáp án (Bài số 1) (5 đề)
Đề kiểm tra 15 phút Hóa 11 Học kì 1 có đáp án (Bài số 1) (5 đề)
Dưới đây là danh sách Đề kiểm tra 15 phút Hóa 11 Học kì 1 có đáp án (Bài số 1) (5 đề). Hi vọng bộ đề thi này sẽ giúp bạn ôn luyện & đạt điểm cao trong các bài thi Hóa học 11.
Sở Giáo dục và Đào tạo .....
Đề kiểm tra 15 phút Học kì 1
Môn: Hóa học 11
Thời gian làm bài: 15 phút
(Đề 1)
Câu 1: Phương trình 2H+ + S2- → H2S là phương trình ion rút gọn của phản ứng?
A. FeS + 2HCl → FeCl2 + H2S.
B. 5H2SO4 đặc + 4Mg → 4MgSO4 + H2S + 4H2O.
C. K2S + 2HCl → 2KCl + H2S.
D. BaS + H2SO4 → BaSO4 + H2S.
Câu 2: Axit mạnh HNO3 và axit yếu HNO2 có cùng nồng độ mol 0,1M và ở cùng nhiệt độ. Sự so sánh nồng độ mol ion nào sau đây là đúng?
A. [H+] của HNO3 < [H+] của HNO2.
B. [H+] của HNO3 > [H+] của HNO2.
C. [H+] của HNO3 = [H+] của HNO2.
D. [NO3-] của HNO3 < [NO2-] của HNO2.
Câu 3: Cho a lít dung dịch KOH có pH = 12 vào 8 lít dung dịch HCl có pH = 3 thu được dung dịch Y có pH = 11. Giá trị của a là
A. 0,12.
B. 1,6.
C. 1,78.
D. 0,8.
Câu 4: Dung dịch X gồm 0,1 mol K+; 0,2 mol Mg2+; 0,1 mol Na+; 0,2 mol Cl- và a mol Y-. Ion Y- và a là
A. OH- và 0,4.
B. NO3- và 0,4.
C. OH- và 0,2.
D. NO3- và 0,2.
Câu 5: Chất nào dưới đây không phân li ra ion khi hòa tan trong nước?
A. MgCl2.
B. HClO3.
C. C6H12O6 (glucozơ).
D. Ba(OH)2.
Câu 6: Cho dãy các chất: Cr(OH)3, Al2(SO4)3, Mg(OH)2, Zn(OH)2, MgO, CrO3. Số chất trong dãy có tính chất lưỡng tính là
A. 2.
B. 4.
C. 5.
D. 3.
Câu 7: Một dung dịch có pH = 5, môi trường của dung dịch là
A. môi trường axit.
B. môi trường kiềm.
C. môi trường trung tính.
D. không xác định được.
Câu 8: Cho dãy các chất: Al2(SO4)3; C2H5OH; C12H22O11 (saccarozơ); CH3COOH; Ca(OH)2; CH3COONH4. Số chất điện li là
A. 2.
B. 3.
C. 4.
D. 5.
Câu 9: Tập hợp các ion nào sau đây có thể tồn tại đồng thời trong cùng một dung dịch?
A. NH4+, Na+, HSO3-, OH-.
B. Fe2+, NH4+, NO3-, SO42-.
C. Na+, Mg2+, OH-, NO3-.
D. Fe2+, K+, OH-, NO3-.
Câu 10. Một mẫu nước mưa có pH = 4,82. Vậy nồng độ H+ trong đó là
A. 10-4M.
B. 10-5M.
C. > 10-5M.
D. < 10-5M.
Đáp án & Hướng dẫn giải
Câu 1. C
A – PT ion rút gọn: FeS + 2H+ → Fe2+ + H2S ↑
B – PT ion rút gọn: SO42- + 10H+ + 4Mg → 4Mg2+ + H2S ↑ + 4H2O
C – PT ion rút gọn: 2H+ + S2- → H2S ↑
D – PT ion rút gọn: Ba2+ + S2- + 2H+ + SO42- → BaSO4 ↓ + H2S ↑
Câu 2. B
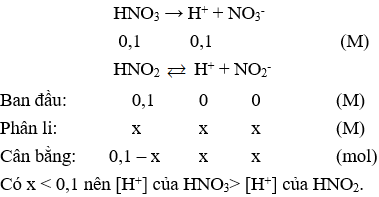
Câu 3. C
Dung dịch KOH có pH = 12 → pOH = 14 – 2 = 2
→ [OH-] = 10-2 = 0,01 (M) → nOH- ban đầu = 0,01.a (mol).
Dung dịch HCl có pH = 3 → [H+] = 10-3 (M) → nH+ban đầu = 8.10-3 (mol)
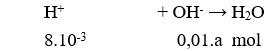
Dung dịch sau phản ứng có pH = 11 > 7 nên OH- dư
pOH sau = 14 – 11 = 3 → [OH-] dư = 10-3 (M)
→ nOH- dư = 10-3. (a + 8) = 0,01a – 8.10-3 → a = 1,78.
Câu 4. B
Do Mg2+ + 2OH- → Mg(OH)2↓ Loại A và C.
Bảo toàn điện tích:
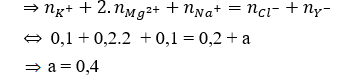
Câu 5. C
Loại A, B và D do axit (HClO3), bazơ (Ba(OH)2), muối (MgCl2) phân li ra ion khi hòa tan trong nước
Câu 6. A
Các chất lưỡng tính trong dãy gồm Cr(OH)2 và Zn(OH)2.
Câu 7. A
pH = 5 < 7. Vậy môi trường của dung dịch là môi trường axit.
Câu 8. C
Chất điện li gồm Al2(SO4)3, CH3COOH, Ca(OH)2, CH3COONH4.
Câu 9. B
Các ion trong B đều không kết hợp được với nhau tạo thành chất ↓, chất ↑ hoặc chất điện li yếu.
Câu 10. C
pH = 4,82 → [H+] = 10-4,82M > 10-5M.
Sở Giáo dục và Đào tạo .....
Đề kiểm tra 15 phút Học kì 1
Môn: Hóa học 11
Thời gian làm bài: 15 phút
(Đề 2)
Câu 1: Dung dịch HCl có pH = 3. Cần pha loãng dung dịch axit này (bằng nước) bao nhiêu lần để thu được dung dịch HCl có pH = 4?
A. 9.
B. 10.
C. 99.
D. 100.
Câu 2: Cho dung dịch chứa các ion sau: Na+, Mg2+, Ba2+, H+, Cl-. Muốn loại được nhiều cation ra khỏi dung dịch, có thể cho tác dụng với các chất nào sau đây?
A. Na2CO3.
B. Na2SO4.
C. K2CO3.
D. NaOH.
Câu 3: Cho các chất: H2O, HCl, NaOH, NaCl, CH3COOH, NH3, CuSO4. Các chất điện li yếu là
A. H2O, CH3COOH, NH3.
B. H2O, CH3COOH, CuSO4.
C. H2O, NaCl, CuSO4, CH3COOH.
D. CH3COOH, CuSO4, NaCl.
Câu 4. Phản ứng nào dưới đây là phản ứng trao đổi ion trong dung dịch?
A. Zn + H2SO4 → ZnSO4 + H2
B. Fe(NO3)3 + 3NaOH → Fe(OH)3 + 3NaNO3
C. 2Fe(NO3)3 + 2KI → 2Fe(NO3)2 + I2 + 2KNO3
D. Zn + 2Fe(NO3)3 → Zn(NO3)2 + 2Fe(NO3)2
Câu 5: Cô cạn dung dịch X chứa 0,1 mol Al3+; 0,1 mol Cu2+; 0,2 mol SO42- và 1 lượng ion Cl- thì thu được bao nhiêu gam muối khan?
A. 28,3.
B. 31,85.
C. 34,5.
D. 42,7.
Câu 6: Phương trình H+ + OH- → H2O là phương trình ion thu gọn của phản ứng có phương trình nào sau đây?
A. NaOH + NaHCO3 → Na2CO3 + H2O.
B. NaOH + HCl → NaCl + H2O.
C. H2SO4 + BaCl2 → BaSO4 + 2HCl.
D. 3HCl + Fe(OH)3 → FeCl3 + 3H2O.
Câu 7: Hiđroxit nào sau đây có tính lưỡng tính?
A. Al(OH)3.
B. Ba(OH)2
C. Ca(OH)2
D. NaOH.
Câu 8. Dãy ion nào sau đây có thể tồn tại trong cùng một dung dịch?
A. Na+, Cl-, S2-, Cu2+.
B. K+, OH-, Ba2+, HCO3-.
C. NH4+, Ba2+, NO3-, OH-.
D. HSO4-, NH4+, Na+, NO3-.
Câu 9: Giá trị pH của dung dịch HCl 0,001M là
A. 3.
B. 2.
C. 1.
D. 4.
Câu 10: Phương trình điện li viết đúng là
A. NaCl → Na2+ + Cl-.
B. Ba(OH)2 → Ba2+ + 2OH-.
C. C2H5OH → C2H5+ + OH-.
D. CH3COOH → CH3COO- + H+.
Đáp án & Hướng dẫn giải
Câu 1. B
Gọi V, V’ lần lượt là thể tích dung dịch HCl có pH = 3, pH = 4.
Dung dịch ban đầu có pH = 3 → [H+] = 10-3M → nH+ban đầu = 10-3V (mol).
Dung dịch sau khi pha loãng có pH = 4 → [H+] = 10-4M → nH+sau = 10-4V’ (mol)
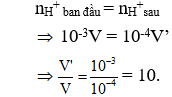
Vậy cần pha loãng axit 10 lần.
Câu 2. A
Mg2+ + CO32- → MgCO3↓
Ba2+ + CO32- → BaCO3↓
2H+ + CO32- → CO2↑ + H2O
Không chọn C vì sẽ đưa thêm cation K+ vào.
Câu 3. A
Các chất điện li yếu là các axit yếu, bazơ yếu, nước.
Câu 4. B
Các phản ứng A, C, D đều là phản ứng oxi hóa – khử.
Câu 5. B
Bảo toàn điện tích có:
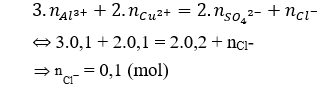
Bảo toàn khối lượng có:
mmuối = ∑mion = 0,1.27 + 0,1.64 + 0,2.96 + 0,1.35.5 = 31,85 (gam).
Câu 6. B
A – PT ion thu gọn: OH- + HCO3- → CO32- + H2O.
B – PT ion thu gọn: H+ + OH- → H2O .
C – PT ion thu gọn: Ba2+ + SO42- → BaSO4 ↓
D – PT ion thu gọn: 3H+ + Fe(OH)3 → Fe3+ + 3H2O.
Câu 7. A
Al(OH)3 có tính lưỡng tính.
Câu 8. D
Các ion HSO4-, NH4+, Na+, NO3- không kết hợp được với nhau tạo thành chất ↓, chất ↑ hoặc chất điện li yếu.
Câu 9. A
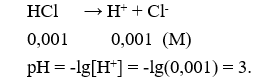
Câu 10. B
A sai vì NaCl → Na+ + Cl-.
C sai vì C2H5OH không phân li ra ion.
D sai vì CH3COOH ⇌ CH3COO- + H+.
Sở Giáo dục và Đào tạo .....
Đề kiểm tra 15 phút Học kì 1
Môn: Hóa học 11
Thời gian làm bài: 15 phút
(Đề 3)
Câu 1. Các ion nào sau đây không thể cùng tồn tại đồng thời trong cùng một dung dịch?
A. Na+, Mg2+, NO3-, SO42-.
B. Ba2+, Al3+, Cl-, NO3-.
C. Cu2+, Fe3+, SO42-, Cl-.
D. K+, NH4+, OH-, PO43-.
Câu 2. Đặc điểm phân li Zn(OH)2 trong nước là
A. theo kiểu bazơ.
B. vừa theo kiểu axit vừa theo kiểu bazơ.
C. theo kiểu axit.
D. không phân li.
Câu 3. Phản ứng tạo thành PbSO4 nào dưới đây không phải là phản ứng trao đổi ion trong dung dịch?
A. Pb(NO3)2 + Na2SO4 → PbSO4 + 2NaNO3.
B. Pb(OH)2 + H2SO4 → PbSO4 + 2H2O.
C. PbS + 4H2O2 → PbSO4 + 4H2O.
D. (CH3COO)2Pb + H2SO4 → PbSO4 + 2CH3COOH.
Câu 4. Cho các chất: HCl, H2O, HNO3, HF, KNO3, CH3COOH, H2S, Ba(OH)2. Số chất điện li yếu là
A. 5.
B. 6.
C. 7.
D. 4.
Câu 5. Một dung dịch có [H+] = 1,5.10-4 M. Môi trường của dung dịch là
A. axit.
B. kiềm.
C. trung tính.
D. không xác định được.
Câu 6. Đối với dung dịch axit mạnh HNO3 0,1M, nếu bỏ qua sự điện li của nước thì đánh giá nào về nồng độ mol ion sau đây là đúng?
A. [H+] = 0,1M.
B. [H+] < [NO3-].
C. [H+] > [NO3-].
D. [H+] < 0,1M.
Câu 7. Cho phương trình phản ứng: 2NaOH + H2SO4 → Na2SO4 + 2H2O. Phương trình ion rút gọn của phản ứng trên là
A. OH- + H+ → H2O.
B. 2OH- + H2+ → 2H2O.
C. SO42- + 2Na+ → Na2SO4.
D. NaOH + 2H+ → Na2+ + H2O.
Câu 8. Đối với dung dịch axit yếu CH3COOH 0,1M, nếu bỏ qua sự điện li của nước thì đánh giá nào về nồng độ mol ion sau đây là đúng?
A. [H+] = 0,1M.
B. [H+] < [CH3COO-].
C. [H+] > [CH3COO-].
D. [H+] < 0,1M.
Câu 9. Trộn 200 ml Ba(OH)2 0,01M với 200 ml KOH 0,03M thu được dung dịch X. Giá trị pH của dung dịch X là
A. 9.
B. 10.
C. 12,4.
D. 13,2.
Câu 10. Dung dịch X gồm a mol Na+; 0,15 mol K+; 0,1 mol HCO3-; 0,15 mol CO32- và 0,05 mol SO42-. Tổng khối lượng muối trong dung dịch X là
A. 33,8 gam.
B. 28,5 gam.
C. 29,5 gam.
D. 31,3 gam.
Đáp án & Hướng dẫn giải
Câu 1. D
Các ion K+, NH4+, OH-, PO43- không thể tồn tại trong cùng một dung dịch do:
NH4+ + OH- → NH3 ↑ + H2O.
Câu 2. B
Zn(OH)2 là hiđroxit lưỡng tính.
Sự phân li theo kiểu bazơ: Zn(OH)2 → Zn2+ + 2OH-.
Sự phân li theo kiểu axit: Zn(OH)2 → ZnO22- + 2H+.
Câu 3. C
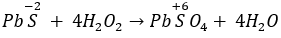
Câu 4. D
Chất điện li yếu gồm axit yếu, bazơ yếu, H2O và một số muối: HgCl2, Hg(CN)2 …
→ H2O, HF, CH3COOH, H2S là chất điện li yếu.
Câu 5. A
Có [H+] = 1,5.10-4 M > 10-7M Môi trường của dung dịch là môi trường axit.
Câu 6. A
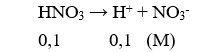
Câu 7. A
Câu 8. D
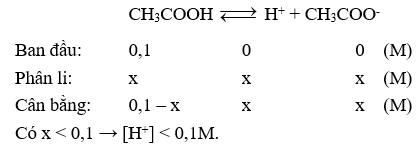
Câu 9. C
Số mol Ba(OH)2 = 0,2.0,01 = 0,002 mol; Số mol KOH = 0,2.0,03 = 0,006 mol
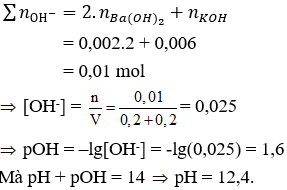
Câu 10. A
Áp dụng định luật bảo toàn điện tích có:
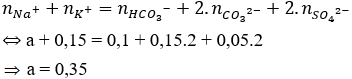
Bảo toàn khối lượng ta có:
mmuối = ∑mion = 0,35.23 + 0,15.39 + 0,1.61 + 0,15.60 + 0,05.96 = 33,8g.
Sở Giáo dục và Đào tạo .....
Đề kiểm tra 15 phút Học kì 1
Môn: Hóa học 11
Thời gian làm bài: 15 phút
(Đề 4)
Câu 1. Phương trình H+ + OH- → H2O là phương trình ion rút gọn của phản ứng có phương trình nào sau đây?
A. NaOH + NaHCO3 → Na2CO3 + H2O.
B. NaOH + HCl → NaCl + H2O.
C. Mg(OH)2 + 2HCl → MgCl2 + 2H2O.
D. 3HCl + Fe(OH)3 → FeCl3 + 3H2O.
Câu 2. Các hợp chất trong dãy chất nào sau đây đều có tính lưỡng tính?
A. Cr(OH)3, Fe(OH)2, Mg(OH)2.
B. Cr(OH)3, Zn(OH)2, Pb(OH)2.
C. Cr(OH)2, Zn(OH)2, Mg(OH)2.
D. Cr(OH)3, Pb(OH)2, Mg(OH)2.
Câu 3. Chất nào sau đây thuộc loại chất điện li yếu?
A. CH3COOH.
B. KOH.
C. HCl.
D. NaCl.
Câu 4. Các ion có thể tồn tại trong cùng một dung dịch là
A. Na+, NH4+, SO42-, Cl-.
B. Mg2+, Al3+, NO3-, CO32-.
C. Ag+, Mg2+, NO3-, Br-.
D. Fe3+, Ag+, NO3-, Cl-.
Câu 5. Cho 400 ml dung dịch KOH 0,1M vào 400 ml dung dịch MgCl2 0,2M thu được m gam kết tủa. Giá trị của m là
A. 2,9.
B. 1,16.
C. 2,32.
D. 4,64.
Câu 6. Dung dịch axit photphoric có chứa các ion (không kể H+ và OH- của nước) là
A. H+, PO43-.
B. H+, H2PO4-, PO43-.
C. H+, HPO42-, PO43-.
D. H+, H2PO4-, HPO42-, PO43-.
Câu 7. Để trung hòa 20 ml dung dịch HCl 0,1M cần 20 ml dung dịch NaOH xM. Giá trị của x là
A. 0,4.
B. 0,2.
C. 0,3.
D. 0,1.
Câu 8. Một dung dịch gồm: 0,03 mol K+; 0,04 mol Ba2+; 0,05 mol HCO3- và a mol ion Xn- (bỏ qua sự điện li của nước). Ion Xn- và giá trị của a lần lượt là
A. Cl- và 0,03.
B. NO3- và 0,06.
C. SO42- và 0,03.
D. OH- và 0,06.
Câu 9. Cho 10 ml dung dịch HCl có pH = 3. Thêm vào đó x ml nước cất và khuấy đều thu được dung dịch có pH = 4. Hỏi x bằng bao nhiêu?
A. 10.
B. 40.
C. 90.
D. 100.
Câu 10. Một dung dịch có [H+] = 2.10-4 M. Môi trường của dung dịch là
A. axit.
B. kiềm.
C. trung tính.
D. không xác định được.
Đáp án & Hướng dẫn giải
Câu 1. B
A – PT ion thu gọn: OH- + HCO3- → CO32- + H2O
B – PT ion thu gọn: H+ + OH- → H2O
C – PT ion thu gọn: Mg(OH)2 + 2H+ → Mg2+ + 2H2O
D – PT ion thu gọn: Fe(OH)3 + 3H+ → Fe3+ + 3H2O.
Câu 2. B
Các chất lưỡng tính: Cr(OH)3, Zn(OH)2, Pb(OH)2.
Câu 3. A
CH3COOH là axit yếu nên là chất điện li yếu.
Câu 4. A
Các ion Na+, NH4+, SO42-, Cl- không kết hợp được với nhau tạo thành chất ↓, chất ↑ hoặc chất điện li yếu.
Câu 5. B
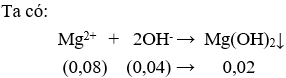
Theo PT Mg2+ dư, số mol kết tủa tính theo số mol OH-
Câu 6. D
H3PO4 là axit 3 nấc. Trong dung dịch nước, H3PO4 phân li theo từng nấc:
H3PO4 ⇌ H+ + H2PO4- (nấc 1 chủ yếu)
H2PO4- ⇌ H+ + HPO42- (nấc 2 kém hơn)
HPO42- ⇌ H+ + PO43- (nấc 3 rất yếu).
Câu 7. D
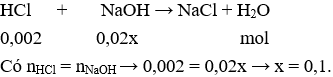
Câu 8. B
Loại C vì SO42- tạo kết tủa với Ba2+.
Loại D vì OH- phản ứng được với HCO3-.
Từ đáp án A và B Ion dạng X-
Bảo toàn điện tích:
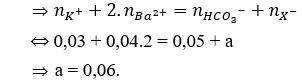
Câu 9. C
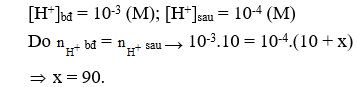
Câu 10. A
[H+] = 2.10-4 M > 10-7 M, vậy môi trường của dung dịch là môi trường axit.
Sở Giáo dục và Đào tạo .....
Đề kiểm tra 15 phút Học kì 1
Môn: Hóa học 11
Thời gian làm bài: 15 phút
(Đề 5)
Câu 1. Chất nào sau đây là chất điện li mạnh?
A. NaCl.
B. CH3COOH.
C. H2O.
D. HF.
Câu 2: Chất nào sau đây là chất điện li?
A. HCl.
B. C6H6.
C. CH4.
D. C2H5OH.
Câu 3: Phương trình điện li nào sau đây không đúng?
A. CH3COOH ⇌ CH3COO- + H+.
B. HCl → H+ + Cl-.
C. HClO → H+ + ClO-
D. Na3PO4→ 3Na+ + PO43- .
Câu 4: Dung dịch X chứa HCl với nồng độ mol là 0,01M. pH của dung dịch là
A. 1.
B. 2.
C. 3.
D. 4.
Câu 5. Cho các dung dịch có cùng nồng độ mol 0,1M: NaCl, CH3COOH, NH3, C2H5OH. Dung dịch có độ dẫn điện tốt nhất là
A. NaCl.
B. CH3COOH.
C. NH3.
D. C2H5OH.
Câu 6. Cho dung dịch X chứa các ion: H+, Ba2+, NO3- vào dung dịch Y chứa các ion: Na+, SO32-, SO42-, S2-. Số phản ứng xảy ra là
A. 1.
B. 2.
C. 3.
D. 4.
Câu 7: Một dung dịch có chứa các ion: Mg2+ (0,05 mol), K+ (0,15 mol), NO3- (0,1 mol) và SO42- (x mol). Giá trị của x là
A. 0,05.
B. 0,075.
C. 0.1.
D. 0,15.
Câu 8: Một dung dịch có [OH-] = 4,2.10-3, đánh giá nào dưới đây là đúng?
A. pH = 3.
B. pH = 4.
C. pH < 3.
D. pH > 4.
Câu 9: Cho dãy các chất: NaOH, Sn(OH)2, Pb(OH)2, Al(OH)3, Cr(OH)3. Số chất trong dãy có tính chất lưỡng tính là
A. 1.
B. 2.
C. 3.
D. 4.
Câu 10. Tập hợp các ion nào sau đây có thể tồn tại đồng thời trong cùng một dung dịch?
A. NH4+, Na+, HCO3-, OH-.
B. Fe2+, NH4+, NO3-, SO42-.
C. Na+, Fe2+, OH-, NO3-.
D. Cu2+, K+, OH-, NO3-.
Đáp án & Hướng dẫn giải
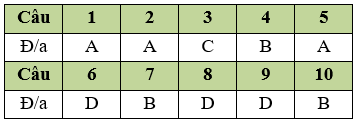
Câu 1. A
NaCl là muối tan được trong nước nên là chất điện li mạnh.
B, D sai vì CH3COOH; HF là các axit yếu nên là chất điện li yếu.
C sai vì H2O là chất điện li rất yếu.
Câu 2. A
Phương trình điện li của HCl:
HCl → H+ + Cl-
Câu 3. C
HClO là axit yếu nên là chất điện li yếu.
Phương trình điện li: HClO ⇌ H+ + ClO-
Câu 4. B
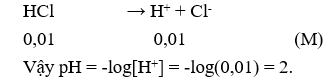
Câu 5. A
Các dẫn điện tốt (chất điện li mạnh) là các muối, axit mạnh, bazơ mạnh
→ Trong các chất trên, NaCl là muối; CH3COOH là axit yếu, NH3 là bazơ yếu, C2H5OH là ancol → NaCl là chất điện li mạnh → NaCl là chất dẫn điện tốt nhất.
Câu 6. D
2H+ + SO32- → H2O + SO2↑
2H+ + S2- → H2S↑
Ba2+ + SO32- → BaSO3↓
Ba2+ + SO42- → BaSO4↓.
Câu 7. B
Bảo toàn điện tích:
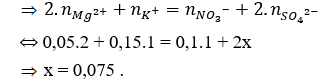
Câu 8. D
[OH-] = 4,2.10-3M pOH = –lg(4,2.10-3) = 2,38 pH = 14 – pOH = 11,62 > 4.
Câu 9. D
Các chất lưỡng tính là: Sn(OH)2, Pb(OH)2, Al(OH)3 và Cr(OH)3.
Câu 10. B
Các ion trong B đều không kết hợp được với nhau tạo thành chất ↓, chất ↑ hoặc chất điện li yếu.
Xem thêm các đề thi Hóa học 11 chọn lọc, có đáp án hay khác:
- Đề kiểm tra 15 phút Hóa 11 Học kì 1 có đáp án (Bài số 2) (3 đề)
- Đề kiểm tra Hóa học 11 Giữa kì 1 có đáp án (3 đề)
- Đề thi Hóa học 11 Giữa kì 1 có đáp án (3 đề)
- Đề thi Hóa học 11 Học kì 1 có đáp án (9 đề)
- Đề kiểm tra 15 phút Hóa 11 Học kì 2 có đáp án (Bài số 1) (8 đề)
Để học tốt lớp 11 các môn học sách mới:
- Giải bài tập Lớp 11 Kết nối tri thức
- Giải bài tập Lớp 11 Chân trời sáng tạo
- Giải bài tập Lớp 11 Cánh diều
Tủ sách VIETJACK shopee lớp 10-11 (cả 3 bộ sách):
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Giáo án lớp 11 (các môn học)
- Giáo án điện tử lớp 11 (các môn học)
- Giáo án Toán 11
- Giáo án Ngữ văn 11
- Giáo án Tiếng Anh 11
- Giáo án Vật Lí 11
- Giáo án Hóa học 11
- Giáo án Sinh học 11
- Giáo án Lịch Sử 11
- Giáo án Địa Lí 11
- Giáo án KTPL 11
- Giáo án HĐTN 11
- Giáo án Tin học 11
- Giáo án Công nghệ 11
- Giáo án GDQP 11
- Đề thi lớp 11 (các môn học)
- Đề thi Ngữ Văn 11 (có đáp án)
- Chuyên đề Tiếng Việt lớp 11
- Đề cương ôn tập Văn 11
- Đề thi Toán 11 (có đáp án)
- Đề thi Toán 11 cấu trúc mới
- Đề cương ôn tập Toán 11
- Đề thi Tiếng Anh 11 (có đáp án)
- Đề thi Tiếng Anh 11 mới (có đáp án)
- Đề thi Vật Lí 11 (có đáp án)
- Đề thi Hóa học 11 (có đáp án)
- Đề thi Sinh học 11 (có đáp án)
- Đề thi Lịch Sử 11
- Đề thi Địa Lí 11 (có đáp án)
- Đề thi KTPL 11
- Đề thi Tin học 11 (có đáp án)
- Đề thi Công nghệ 11
- Đề thi GDQP 11 (có đáp án)




 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

