Giáo án Hóa học 8 Chương 5: Hiđro - Nước mới nhất
Với mục đích giúp các Thầy / Cô giảng dạy môn Hóa học dễ dàng biên soạn Giáo án Hóa học lớp 8, VietJack biên soạn Bộ Giáo án Hóa học 8 Chương 5: Hiđro - Nước phương pháp mới theo hướng phát triển năng lực bám sát mẫu Giáo án môn Hóa học chuẩn của Bộ Giáo dục. Hi vọng tài liệu Giáo án Hóa học 8 này sẽ được Thầy/Cô đón nhận và đóng góp những ý kiến quí báu.
Mục lục Giáo án Hóa học 8 Chương 5: Hiđro - Nước
- Giáo án Hóa học 8 Bài 31: Tính chất - Ứng dụng của hiđro
- Giáo án Hóa học 8 Bài 31: Tính chất - Ứng dụng của hiđro (Tiết 2)
- Giáo án Hóa học 8 Bài 33: Điều chế khí hiđro - Phản ứng thế
- Giáo án Hóa học 8 Bài 34: Bài luyện tập 6
- Giáo án Hóa học 8 Bài 34: Bài luyện tập 6 (Tiết 2)
- Giáo án Hóa học 8 Bài 35: Bài thực hành 5
- Giáo án Hóa học 8 Bài 36: Nước
- Giáo án Hóa học 8 Bài 36: Nước (Tiết 2)
- Giáo án Hóa học 8 Bài 37: Axit - Bazơ - Muối
- Giáo án Hóa học 8 Bài 37: Axit - Bazơ - Muối (Tiết 2)
- Giáo án Hóa học 8 Bài 38: Bài luyện tập 7
- Giáo án Hóa học 8 Bài 39: Bài thực hành 6
Giáo án Hóa học 8 Bài 31: Tính chất - Ứng dụng của hiđro
I. MỤC TIÊU
1. Kiến thức :
HS biết được:
-Tính chất vật lí của hiđro: Trạng thái, màu sắc, tỉ khối, tính tan trong nước.
- TCHH của hiđro: tác dụng với oxi, tác dụng với oxit kim loại,
- Ứng dụng của H2.
2. Kĩ năng :
Quan sát thí nghiệm, hình ảnh... rút ra được nhận xét về TCVL và TCHH của hiđro.
3. Thái độ : kiên trì trong học tập – Yêu thích bộ môn và gìn giữ môi trường
4. Năng lực cần hướng tới :
- Năng lực tự học
- Năng lực giải quyết vấn đề thông qua môn Hóa học
- Năng lực sáng tạo
- Năng lực vận dụng kiến thức hóa học vào cuộc sống
- Năng lực giao tiếp
- Năng lực hợp tác
- Năng lực nghiên cứu và thực hành Hóa học
- Năng lực sử dụng ngôn ngữ Hóa Học
- Năng lực tính toán.
II. TRỌNG TÂM:
-Tính chất hóa học của hiđro
III. CHUẨN BỊ
1. Giáo Viên :
-Máy chiếu, PHT
-Dụng cụ: Lọ nút, giá thí nghiệm, đèn cồn, ống ngiệm có nhánh, cố thuỷ tinh, khay nhựa
-Hoá chất: 5 lọ khí H2, 1 lọ đựng khí O2, Zn viên, dd HCl
2. Học sinh :
-Ôn lại một số kiến thức: đơn chất, hợp chất, NTHH, thành phần của không khí.
-Đọc kĩ phần đọc thêm để giải thích các hiện tượng của bài học.
IV. TIẾN TRÌNH GIẢNG DẠY:
1. Ổn đinh trật tự - kiểm tra bài cũ
Bỏ qua kiểm tra bài cũ
2. Hoạt động dạy học
| GIÁO VIÊN | HỌC SINH | NỘI DUNG GHI BẢNG |
|---|---|---|
|
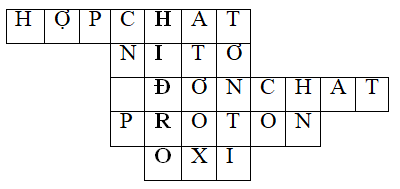
Hoạt động 1: Khởi động (5 p) Chơi giải ô chữ -Gồm 5 hàng ngang. +Hàng ngang 1: (7 chữ cái) Chất được tạo bởi hai hay nhiều nguyên tố hóa học gọi là gì? +Hàng ngang 2: (4 chữ cái) Tên một nguyên tố hóa học chiếm 1% thể tích không khí gọi là gì? +Hàng ngang 3: (7 chữ cái) Chất được tạo bởi một nguyên tố hóa học gọi là gì? +Hàng ngang 4: (6 chữ cái) Một loại hạt đặc trưng cho nguyên tố hóa học? +Hàng ngang 5: (3 chữ cái) Tên một nguyên tố hóa học duy trì sự cháy, sự sống? - Hiđro cũng là một đơn chất có nhiều ứng dụng trong đời sống và sản xuất. Hợp chất phổ biến của hiđro trong tự nhiên là gì? Chúng ta cùng nghiên cứu chương : V - HIĐRO. NƯỚC - Vậy, Hiđro có KHHH, CTHH, Tính chất và ứng dụng như thế nào? Ta cùng tìm hiểu bài đầu tiên của chương: TÍNH CHẤT – ỨNG DỤNG CỦA HIĐRO |
||
Hoạt động 2: Hình thành kiến thức (25 phút) |
||
I. Tính chất vật lí (5’) |
||
|
Gọi 2 hs viết KHHH và NTK. CTHH và PTK ?Khi nghiên cứu một nguyên tố cụ thể, thông thường đi theo trình tự như thế nào? -GV:Tiết học hôm nay chúng ta tìm hiểu I, II/1. ? KHHH và NTK của hiđro? ? CTHH và PTK như thế nào? Gv: Phân tử Hiđro gồm hai nguyên tử, vậy ở điều kiện thường, hiđro tồn tại ở trạng thái gì? Màu gì? Nặng hay nhẹ hơn không khí? Có tan được trong nước? Ta đi vào phần I. -Giới thiệu lọ đựng hiđro ?Nêu trạng thaí, màu sắc của H2 ? -Giới thiệu quả bóng có bơm khí H2 ?Nếu thả quả bóng ra thì hãy dự đoán hướng di chuyển của quả bóng? Gv: thả quả bóng để chứng minh dự đoán của học sinh. ?Vì sao quả bóng có thể bay lên được? ?Dựa vào cơ sở nào ta có thể chứng minh được khí H2 nhẹ hơn không khí? Gv: Từ đó các nhà khoa học cũng chứng minh được rằng Hiđro là chất khí nhẹ nhất trong tất cả các chất khí GV giới thiệu: ?1 lít nước ở 15oC hoà tan 20 ml khí H2, Nhận xét tính tan của khí hiđro trong nước? ? Suy nghỉ 1p, → thảo luận theo cặp 1p → hoàn thành TCVL của H2 ? -Nhận xét, và chốt kiến thức. Hiđro có những TCHH nào? Ta cùng tìm hiểu nội dung phần II. |
-Tính chất vật lý -Tính chất hóa học -Ứng dụng. -H: 1 đvC -H2 : 2 đvC HS quan sát -Nhận xét trạng thái, màu sắc → so sánh H2 với kk (Quả bóng bay lên). → Nhận xét tính tan trong nước của H2. Khí hiđro là chất khí, không màu, không mùi, không vị, nhẹ nhất trong các chất khí, tan rất ít trong nước. |
-KHHH: H NTK: 1đvC -CTHH: H2 PTK: 2đvC I. Tính chất vật lý. Hiđro là chất khí, không màu, nhẹ nhất trong các chất khí, tan ít trong nước. |
I. Tính chất hoá học. (20’) |
||
|
-Đọc nội dung thí nghiệm (a) Gv: giới thiệu dụng cụ, hóa chất. Gv biểu diễn thí nghiệm và yêu cầu học sinh chú ý các thao tác, ngọn lửa và sản phẩm sinh ra. - Giới thiệu cách thử khí H2 tính khiết, ? Các em nhận xét ngọn lửa H2 cháy trong kk? GV: đưa ngọn lửa H2 đang cháy vào lọ khí O2. ? Hãy quan sát và nhận xét? Chú ý: ngọn lửa và thành lọ đựng khí oxi GV: Hiđro cháy trong oxi tao ra hơi nước, đồng thời toả nhiều nhiệt → vì vậy người ta dùng hiđro làm nguyên liêu cho đèn xì oxi – hiđro để hàn cắt kim loại ?Nêu kết luận gì ? ?Xác định chất tham gia, chất sản phẩm cho thí nghiệm trên? ?Viết PTHH xảy ra ? ?Lúc thu H2 vào ống nghiệm và đưa gần ngọn lửa đèn cồn, em nghe âm thanh gì? Gv:Chúng ta sẽ làm rõ nguyên nhân nào gây nên tiếng nổ đó. -Đọc nội dung phần c -Thảo luận nhóm trả lời 3 câu hỏi: 3’ * Tại sao hỗn hợp khí H2 và O2 cháy lại gây tiếng nổ? *Nếu đốt cháy H2 ngay ở đầu ống dẫn khí, dù ở trong lọ khí oxi hay không khí, sẽ không gây ra tiếng nổ mạnh, vì sao? *Làm thế nào để biết dòng khí H2 là tinh khiết để có thể đốt cháy dòng khí đó mà không gây ra tiếng nổ mạnh? -Các nhóm treo bảng con, các nhóm khác nhận xét, bổ sung (nếu có) GV: nếu lấy tỉ lệ về thể tích Vhiđro /Voxi = 2/1 thì khi đốt hiđro, hỗn hợp sẽ gay nỗ mạnh ( hỗn hợp nỗ ) GV chốt kiến thức và ghi bảng * Chú ý: Ở bài thực hành tới chúng ta có điều chế, thu khí và đốt H2 thì phải hết sức cẩn thận, phải cho H2 thoát ra ngoài một thời gian rồi mới đốt. |
-1 hs đứng tại chỗ đọc -Chú ý -Quan sát -Ngọn lửa vàng mờ -Quan sát -Ngọn lửa cháy mạnh hơn, trên thành lọ chứa oxi có những giọt nước. -H2 tác dụng với oxi. -Chất tham gia: H2 và O2 Chất sản phẩm: H2O 2H2 + O2 -Có tiếng nổ -1 hs đọc nội dung phần c -Thảo luận nhóm (3’) *Vì: Khi đốt cháy rất nhanh và tỏa rất nhiều nhiệt. Nhiệt này làm cho thể tích nước tạo thành sau phản ứng tăng lên đột ngột, làm chấn động mạnh kk và gây nên tiếng nổ. *vì trong dụng cụ điều chế H2, kk chưa được cuốn ra hết và có chứa 1 phần khí oxi, nếu H2 thoát ra sẽ kết hợp với oxi không khí theo đúng tỉ lệ 2:1 thì sẽ gây tiếng nổ mạnh. *Thu khí H2 vào ống nghiệm và đốt trên ngọn lửa đèn cồn đến khi nghe tiếng nổ nhẹ hoặc không nghe tiếng nổ thì H2 sinh ra là tinh khiết. |
II. Tính chất hoá học 1 Tác dung với oxi : - H2 cháy trong khí oxi với ngọn lửa màu xanh, tỏa nhiệt → nước 2H2 + O2 -Hỗn hợp khí H2 và O2 theo tỉ lệ về thể tích 2:1 là hỗn hợp nổ mạnh |
Hoạt động 3: Củng cố, luyện tập (5p) |
||
-Hệ thống lại nội dung bài học -Luyện tập: Bằng Phương pháp hóa học hãy nhận biết 3 chất khí không màu bị mất nhãn đựng trong 3 lọ riêng biệt sau: oxi, hiđro và khí cacbonic |
Hướng dẫn: -Dùng que đóm còn tàn đỏ → O2 - Dùng nước vôi trong → CO2 |
|
Hoạt động 4: Vận dụng (5p) |
||
Đốt cháy Hiđro trong oxi thu được 10,8g nước. Tính thể tích khí oxi và Hiđro tham gia phản ứng ở đktc. |
-Tóm tắt: mH2O = 10,8 (g) VO2 = ?(l) VH2 = ?(l) Giải: a/ -Tính nH2O = PTHH: O2 + 2H2 -Từ (1) ta có: nO2 = → VO2đktc = n.22,4 b/ Từ (1) nH2 = nH2O = 0,6(mol) → VH2đktc = n.22,4 |
|
Hoạt động 5: Tìm tòi, mở rộng (2p) |
||
|
- Hệ thống lại nội dung bài giảng - Đọc bài đọc thêm để hiểu hơn hiện tượng nổ khi đốt H2 và O2 - BTVN: bài 6 sgk trang 109. - Học bài và soạn trước phần còn lại của bài |
||
V. RÚT KINH NGHIỆM
............................................................................................................................................................
............................................................................................................................................................
............................................................................................................................................................
............................................................................................................................................................
............................................................................................................................................................
Giáo án Hóa học 8 Bài 31: Tính chất - Ứng dụng của hiđro (Tiết 2)
I. MỤC TIÊU:
1. Kiến thức :
HS biết được:
- Phản ứng của H2 với oxit kim loại;
- Ứng dụng của H2
2. Kĩ năng :
-Viết được phương trình hóa học minh họa được tính khử của hiđro.
-Tính được thể tích khí hiđro (đktc) tham gia phản ứng và sản phẩm.
3. Thái độ : kiên trì trong học tập, yêu thích bộ môn
4. Năng lực cần hướng tới :
- Năng lực tự học
- Năng lực giải quyết vấn đề thông qua môn Hóa học
- Năng lực vận dụng kiến thức hóa học vào cuộc sống
- Năng lực giao tiếp
- Năng lực hợp tác
- Năng lực nghiên cứu và thực hành Hóa học
- Năng lực sử dụng ngôn ngữ Hóa Học
- Năng lực tính toán.
II. TRỌNG TÂM:
-Tính chất hóa học của hiđro (tt)
-Khái niệm về chất khử, sự khử.
III. CHUẨN BỊ:
1. Giáo viên
-Hoá chất: CuO, Zn, miếng Cu, dd HCl, diêm,
-Dụng cụ: Ống dẫn khí cao su, bình kíp đơn giản, đèn cồn, ống dẫn khí bằng thuỷ tinh rỗng hai đầu, miếng thuỷ tinh mỏng
2. Học sinh
Học bài cũ và chuẩn bị bài mới
IV. TIẾN TRÌNH BÀI GIẢNG:
1. Ổn định trật tự và kiểm tra bài cũ (5’)
a. So sánh sự giống nhau và khác nhau về tính chất vật lý giữa H2 và O2 ?
b. Tại sao trước khi đốt cháy H2 chúng ta cần phải thử độ tính khiết của H2 ? Nêu cách thử?
2. Hoạt động dạy học :
Hoạt động 1: Khởi động (2p)
Trong buổi học ngày hôm trước, cô đã cùng các em tìm hiểu các kiến thức có liên quan đến tính chất vật lý cũng như phản ứng của hiđro với oxi. Trong buổi học ngày hôm nay chúng ta cùng đi tìm hiểu xem phản ứng của H2 với oxit kim loại là như thế nào? Ứng dụng của H2 là ra sao?
Hoạt động 2: Hình thành kiến thức (25p)
| GIÁO VIÊN | HỌC SINH | NỘI DUNG |
|---|---|---|
Tìm hiểu: Tính chất hóa học còn lại của H2 |
||
|
Đọc cách tiến hành thí nghiêm. GV:Hướng dẫn học sinh làm thí nghiệm thí nghiệm H2 + CuO -Giới thiệu cho HS ống dẫn khí bằng thuỷ tinh thủng 2 đầu, có nút cao su với ống dẫn xuyên qua có đựng sẵn CuO ở trong, đèn cồn, ống nghiệm. ?Hãy quan sát và nêu màu sắc của CuO? GV:Vừa làm thí nghiệm vừa hướng dẫn HS điều chế khí H2 ?Yêu cầu HS quan sát hiện tượng sau khi cho luồng khí H2 đi qua ở nhiệt độ thường. Nhận xét ? GV:đưa đèn cồn đang cháy vào phía dưới ống nghiệm có CuO ? Em hãy quan sát và nêu hiện tượng xảy ra và nhận xét ? ?Yêu cầu HS so sánh màu của sản phẩm thu được với kim loại Cu rồi nêu tên của sản phẩm có màu đỏ gạch? ?Ngoài đồng, còn có sản phẩm nào khác? GV: chốt lại kiến thức ?Gọi 1 hs lên bảng viết PTHH. ? Khí H2 có vai trò gì trong phản ứng trên? Ngoài CuO, H2 cũng có thể khử nhiều oxit kim loại khác để tạo thành kim loại tương ứng -Treo bảng phụ có bài tập sau: Viết phương trình phản ứng hoá học khí H2 khử các oxit sau: a. Sắt (III) oxit (Fe2O3) b. Kẽm oxit (ZnO) ?Những hợp chất chứa oxi ở chất tham gia gọi là gì? ?Sau phản ứng các oxit kim loại đã tạo thành chất gì? GV: Ở những nhiệt độ khác nhau, H2 đã chiếm nguyên tử oxi của 1 số oxit kim loại để tạo ra kim loại. Đây là 1 trong những phương pháp điều chế kim loại ? Vậy Hiđro có những TCHH nào ? ?Em có kết luận gì về TCHH của H2 ? |
-1 hs đọc cách tiến hành -Quan sát -Chú ý theo dõi -CuO: màu đen -Quan sát. -Không có hiện tượng gì xảy ra → không có hiện tượng gì xảy ra. -Quan sát -Bột CuO từ màu đen chuyển dần sang màu đỏ gạch và trên miếng thuỷ tinh bị mờ. -Giống nhau (màu đỏ gạch) -Sản phẩm có tên đồng -Hơi nước H2 + CuO - chất khử Cho HS làm theo bàn 2’ a.Fe2O3 + 3H2 b/ ZnO + H2 -Oxit kim loại. -Kim loại -T/d với oxi và oxit kim loại - Ở nhiệt độ thích hợp, khí H2 không những kết hợp được với đơn chất oxi, mà nó còn có thể kết hợp được với nguyên tố oxi trong một số oxit kim loại. Khí H2 có tính khử. Các phản ứng này toả nhiều nhiệt. |
II. Tính chất hoá học 2.Tác dụng với đồng (II) oxit -Hiện tượng: Bột CuO có màu đen chuyển sang màu đỏ gạch là kim loại Cu. H2 + CuO *Kết luận: Ở nhiệt độ thích hợp, khí H2 không những kết hợp được với đơn chất oxi, mà nó còn có thể kết hợp được với nguyên tố oxi trong một số oxit kim loại. Khí H2 có tính khử. Các phản ứng này toả nhiều nhiệt. |
Tìm hiểu ứng dụng của H2 |
||
|
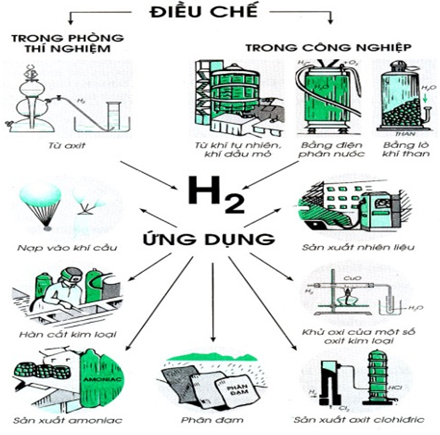
-Yêu cầu HS quan sát H 5.3 sgk và trên tranh đã che khuất tên ứng dụng ?Nêu ứng dụng của H2 . ?Phát tên ứng dụng của H2 và cho hs lên gắng trên tranh cho thích hợp. ?Dựa vào tính chất hoá học nào mà người ta ứng dụng H2 làm nhiên liệu? ?Dựa vào TCHH nào mà người ta ứng dụng H2 làm chất khử để có thể điều chế một số kim loại từ các oxit kim loại? ?H2 có thể bơm vào khinh khí cầu hoặc bong bóng bay là dựa vào tính chất vật lý nào? |
Quan sát. - Làm nhiên liệu - Làm nguyên liệu - Dùng làm chất khử -Dùng bơm vào khinh khí cầu, bóng thám hiểm Lần lượt từng hs lên gắng trên tranh H2 cháy trong oxi toả nhiều nhiệt -H2 tác dụng với oxit kim loại -H2 nhẹ nhất trong các chất khí. |
III. Ứng dụng của Hiđro. - Làm nhiên liệu - Làm nguyên liệu - Dùng làm chất khử -Dùng bơm vào khinh khí cầu, bóng thám hiểm |
Hoạt động 3: Luyện tập – vận dụng (5 phút)
-Hệ thống lại nội dung bài giảng
- Bài tập 3/109 : Chọn cụm từ thích hợp trong khung điền vào chổ trống trong các câu sau :
Hoạt động 4: Tìm tòi – mở rộng (5 phút)
- Hướng dẫn HS đọc phân đọc thêm SGK
Nhắc nhở HS:
-Học bài và làm bài tập 5,6 9 sgk tr 112
-Soạn trước bài 32
V. RÚT KINH NGHIỆM
............................................................................................................................................................
............................................................................................................................................................
............................................................................................................................................................
............................................................................................................................................................
Xem thêm các bài soạn Giáo án Hóa học lớp 8 theo hướng phát triển năng lực mới nhất, hay khác:
- Giáo án Hóa học 8 Chương 1: Chất - Nguyên tử - Phân tử
- Giáo án Hóa học 8 Chương 2: Phản ứng hóa học
- Giáo án Hóa học 8 Chương 3: Mol và tính toán hóa học
- Giáo án Hóa học 8 Chương 4: Oxi - Không khí
- Giáo án Hóa học 8 Chương 6: Dung dịch
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Loạt bài Giáo án Hóa học lớp 8 mới, chuẩn nhất của chúng tôi được biên soạn bám sát nội dung sgk Hóa học 8 theo chuẩn Giáo án của Bộ GD & ĐT.
Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Giáo án lớp 8 (các môn học)
- Giáo án điện tử lớp 8 (các môn học)
- Giáo án Toán 8
- Giáo án Ngữ văn 8
- Giáo án Tiếng Anh 8
- Giáo án Khoa học tự nhiên 8
- Giáo án KHTN 8
- Giáo án Lịch Sử 8
- Giáo án Địa Lí 8
- Giáo án GDCD 8
- Giáo án HĐTN 8
- Giáo án Tin học 8
- Giáo án Công nghệ 8
- Giáo án Vật Lí 8
- Giáo án Hóa học 8
- Giáo án Sinh học 8
- Đề thi lớp 8 (các môn học)
- Đề thi Ngữ Văn 8 (có đáp án)
- Chuyên đề Tiếng Việt lớp 8
- Đề thi Toán 8
- Đề cương ôn tập Toán 8
- Đề thi Tiếng Anh 8 (có đáp án)
- Đề thi Tiếng Anh 8 mới (có đáp án)
- Đề thi Khoa học tự nhiên 8 (có đáp án)
- Đề thi Lịch Sử và Địa Lí 8 (có đáp án)
- Đề thi GDCD 8 (có đáp án)
- Đề thi Tin học 8 (có đáp án)
- Đề thi Công nghệ 8 (có đáp án)

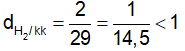
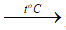 2H2O
2H2O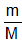 = 0,6 (mol)
= 0,6 (mol)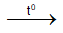 2H2O (1)
2H2O (1)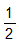 .nH2O = 0,3 (mol)
.nH2O = 0,3 (mol)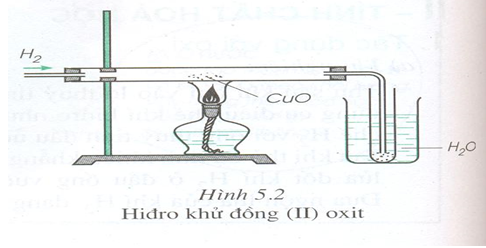






 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

