Chuyên đề dạy thêm KHTN 7 phần Hóa học
Tài liệu chuyên đề dạy thêm KHTN 7 phần Hóa học gồm các dạng bài tập từ cơ bản đến nâng cao với phương pháp giải chi tiết và bài tập tự luyện đa dạng giúp Giáo viên có thêm tài liệu giảng dạy Khoa học tự nhiên 7.
Chuyên đề dạy thêm KHTN 7 phần Hóa học
Chỉ từ 450k mua trọn bộ Chuyên đề dạy thêm Khoa học tự nhiên 7 phần Hóa học bản word có lời giải chi tiết:
- B1: gửi phí vào tk:
1133836868- CT TNHH DAU TU VA DV GD VIETJACK - Ngân hàng MB (QR) - B2: Nhắn tin tới Zalo VietJack Official - nhấn vào đây để thông báo và nhận giáo án
Chủ đề 1. Nguyên tử
A. KIẾN THỨC CẦN NẮM VỮNG
I. Mô hình nguyên tử của Rutherford – Bohr (Rơ-dơ-pho – Bo)
♦ Nguyên tử là những hạt vô cùng nhỏ và trung hòa về điện.
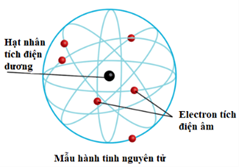
♦ Mô hình nguyên tử của Rutherford – Bo (mẫu hành tinh nguyên tử):
Nguyên tử có cấu tạo rỗng gồm:
+ Hạt nhân ở tâm mang điện tích dương.
+ Lớp vỏ chứa các electron mang điện tích âm chuyển động trên những quỹ đạo xác định xung quanh hạt nhân theo từng lớp khác nhau như các hành tinh quay xung quanh mặt trời.
II. Cấu tạo nguyên tử
|
Hạt nhân nguyên tử |
Vỏ nguyên tử |
|
- Hạt nhân nằm ở tâm và có kích thước rất nhỏ so với kích thước nguyên tử. - Hạt nhân gồm: proton (p), mang điện dương, điện tích +1 và neutron (n) không mang điện. - Hạt nhân có Z proton thì có điện tích là +Z và số đơn vị điện tích hạt nhân là Z. |
- Vỏ nguyên tử tạo bởi một hay nhiều electron (e) mang điện âm, mỗi e có điện tích -1. - Các electron được sắp xếp từ trong ra ngoài thành từng lớp: Lớp thứ nhất tối đa 2e; lớp thứ hai tối đa 8e; lớp thứ 3 (tạm thời) tối đa 8e; … - Nguyên tử trung hòa điện nên số p = số e. |
III. Khối lượng nguyên tử
♦ Đơn vị khối lượng nguyên tử (amu): 1 amu = 1,6605.10-24 g.
♦ Khối lượng nguyên tử: mnt = mp + mn + me ≈ mp + mn (do me rất nhỏ so với mp,n )
⇒ Khối lượng của nguyên tử tập trung chủ yếu ở hạt nhân, có thể coi khối lượng hạt nhân là khối lượng nguyên tử.
|
Cấu tạo nguyên tử |
Kí hiệu |
Khối lượng (amu) |
Điện tích |
|
|
Hạt nhân |
Proton |
p |
≈ 1 |
+1 |
|
Neutron |
n |
≈ 1 |
0 |
|
|
Vỏ |
Electron |
e |
≈ 0,00055 |
-1 |
B. BÀI TẬP
❖ BÀI TẬP TỰ LUẬN
Câu 1. Hãy điền các từ và cụm từ thích hợp vào chỗ trống:
(a) Nguyên tử là hạt (1)………….……... và (2) ……………………. Theo Rutherford – Bohr, nguyên tử có cấu tạo gồm hai phần là (3) …………… (mang (4)…………..…….) và (5) ………………….
tạo bởi (6) ………………… (mang (7) …………………..).
(b) Trong nguyên tử, các electron (8) ……………… xung quanh hạt nhân và (9) ………….. thành từng lớp.
(c) Trong nguyên tử, số proton bằng số (10) ……………. Phần lớn khối lượng nguyên tử tập trung ở (11) ……………
Câu 2. Hoàn thành thông tin về các loại hạt trong nguyên tử trong bảng sau:
|
Cấu tạo nguyên tử |
Kí hiệu |
Khối lượng (amu) |
Điện tích |
|
|
Hạt nhân |
Proton |
|
|
|
|
Neutron |
|
|
|
|
|
Vỏ |
Electron |
|
|
|
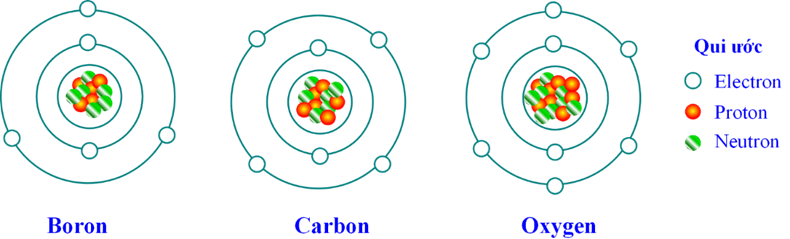
Câu 3. Hình vẽ dưới đây mô phỏng nguyên tử boron, carbon và oxygen:
(a) Hãy xác định số hạt proton, neutron, electron trong mỗi nguyên tử boron, carbon, oxygen.
(b) Các nguyên tử trên có mang điện tích không? Vì sao?
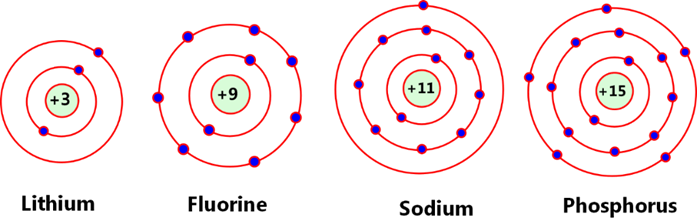
Câu 4. Cho biết sơ đồ một số nguyên tử sau:
Dựa vào sơ đồ trên hãy hoàn thành bảng sau:
|
|
Số proton |
Số electron |
Số lớp electron |
Số e lớp ngoài cùng |
|
Lithium |
|
|
|
|
|
Fluorine |
|
|
|
|
|
Sodium |
|
|
|
|
|
Phosphorus |
|
|
|
|
Câu 5.
(a) Vẽ sơ đồ cấu tạo nguyên tử nitrogen (7p); magnesium (12p); chlorine (17p); potassium (19p).
(b) Cho biết số electron, số lớp e, số e từng lớp, số e lớp ngoài cùng của các nguyên tử trên.
Câu 6. Một loại nguyên tử nitrogen có 7 proton và 7 neutron trong hạt nhân.
(a) Nguyên tử nitrogen này có bao nhiêu electron?
(b) Tính khối lượng của hạt nhân và của toàn nguyên tử nitrogen.
(c) Từ kết quả đó có thể coi khối lượng của nguyên tử là khối lượng của hạt nhân được không?
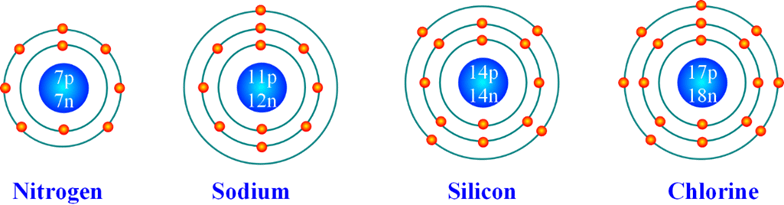
Câu 7. Cho biết sơ đồ một số nguyên tử sau:
Dựa vào sơ đồ trên hãy hoàn thành bảng sau:
|
Nguyên tử |
Số neutron |
Số proton |
Số electron |
Điện tích hạt nhân |
Khối lượng nguyên tử (amu) |
|
Nitrogen |
|
|
|
|
|
|
Sodium |
|
|
|
|
|
|
Silicon |
|
|
|
|
|
|
Chlorine |
|
|
|
|
|
Câu 8. Hãy cho biết:
(a) Nguyên tử có cấu tạo rỗng hay đặc? gồm những phần nào?
(b) Loại hạt nào được tìm thấy trong hạt nhân nguyên tử? khối lượng bằng bao nhiêu (amu)?
(c) Loại hạt nào được tìm thấy ở lớp vỏ nguyên tử? khối lượng bằng bao nhiêu (amu)?
(d) Trong nguyên tử, loại hạt nào mang điện? điện tích bằng bao nhiêu?
(e) Nguyên tử mang điện âm, điện dương hay không mang điện? Vì sao?
(g) Tại sao có thể nói khối lượng của nguyên tử tập trung hầu hết ở hạt nhân?
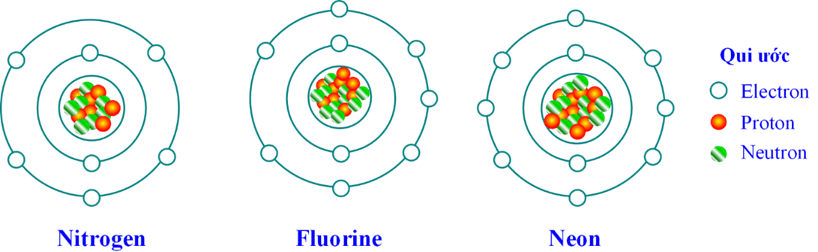
Câu 9. Hình vẽ dưới đây mô phỏng nguyên tử nitrogen, fluorine và neon:
(a) Hãy xác định số hạt proton, neutron, electron trong mỗi nguyên tử nitrogen, fluorine và neon.
(b) Trong ba nguyên tử trên thì hai hạt nào luôn có số lượng bằng nhau?
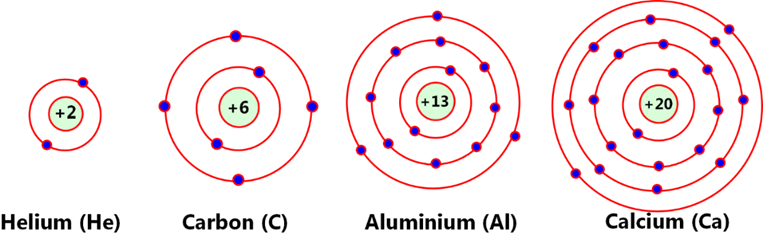
Câu 10: Cho biết sơ đồ một số nguyên tử sau:
Dựa vào sơ đồ trên hãy hoàn thành bảng sau:
|
|
Số proton |
Số electron |
Số lớp electron |
Số e lớp ngoài cùng |
|
Helium |
|
|
|
|
|
Carbon |
|
|
|
|
|
Aluminium |
|
|
|
|
|
Calcium |
|
|
|
|
Câu 11.
(a) Vẽ sơ đồ cấu tạo nguyên tử boron (5p); sodium (11p); sulfur (16p).
(b) Cho biết số electron, số lớp e, số e từng lớp, số e lớp ngoài cùng của các nguyên tử trên.
Câu 12. Hoàn thành bảng sau bằng cách điền thông tin thích hợp vào các ô trống:
|
Nguyên tử |
Số neutron |
Số proton |
Số electron |
Điện tích hạt nhân |
Khối lượng nguyên tử (amu) |
|
Neon |
10 |
10 |
|
|
|
|
Aluminium |
14 |
|
|
+13 |
|
|
Phosphorus |
|
15 |
|
|
31 |
|
Sulfur |
16 |
|
16 |
|
|
|
Potassium |
|
|
|
+19 |
39 |
|
Calcium |
20 |
|
|
|
40 |
................................
................................
................................
Xem thêm đề thi lớp 7 các môn học có đáp án hay khác:
Tài liệu giáo án lớp 7 các môn học chuẩn khác:
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Giải Tiếng Anh 12 Global Success
- Giải sgk Tiếng Anh 12 Smart World
- Giải sgk Tiếng Anh 12 Friends Global
- Lớp 12 Kết nối tri thức
- Soạn văn 12 (hay nhất) - KNTT
- Soạn văn 12 (ngắn nhất) - KNTT
- Giải sgk Toán 12 - KNTT
- Giải sgk Vật Lí 12 - KNTT
- Giải sgk Hóa học 12 - KNTT
- Giải sgk Sinh học 12 - KNTT
- Giải sgk Lịch Sử 12 - KNTT
- Giải sgk Địa Lí 12 - KNTT
- Giải sgk Giáo dục KTPL 12 - KNTT
- Giải sgk Tin học 12 - KNTT
- Giải sgk Công nghệ 12 - KNTT
- Giải sgk Hoạt động trải nghiệm 12 - KNTT
- Giải sgk Giáo dục quốc phòng 12 - KNTT
- Giải sgk Âm nhạc 12 - KNTT
- Giải sgk Mĩ thuật 12 - KNTT
- Lớp 12 Chân trời sáng tạo
- Soạn văn 12 (hay nhất) - CTST
- Soạn văn 12 (ngắn nhất) - CTST
- Giải sgk Toán 12 - CTST
- Giải sgk Vật Lí 12 - CTST
- Giải sgk Hóa học 12 - CTST
- Giải sgk Sinh học 12 - CTST
- Giải sgk Lịch Sử 12 - CTST
- Giải sgk Địa Lí 12 - CTST
- Giải sgk Giáo dục KTPL 12 - CTST
- Giải sgk Tin học 12 - CTST
- Giải sgk Hoạt động trải nghiệm 12 - CTST
- Giải sgk Âm nhạc 12 - CTST
- Lớp 12 Cánh diều
- Soạn văn 12 Cánh diều (hay nhất)
- Soạn văn 12 Cánh diều (ngắn nhất)
- Giải sgk Toán 12 Cánh diều
- Giải sgk Vật Lí 12 - Cánh diều
- Giải sgk Hóa học 12 - Cánh diều
- Giải sgk Sinh học 12 - Cánh diều
- Giải sgk Lịch Sử 12 - Cánh diều
- Giải sgk Địa Lí 12 - Cánh diều
- Giải sgk Giáo dục KTPL 12 - Cánh diều
- Giải sgk Tin học 12 - Cánh diều
- Giải sgk Công nghệ 12 - Cánh diều
- Giải sgk Hoạt động trải nghiệm 12 - Cánh diều
- Giải sgk Giáo dục quốc phòng 12 - Cánh diều
- Giải sgk Âm nhạc 12 - Cánh diều







 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

