Đề thi Hóa học 12 Học kì 2 trắc nghiệm - tự luận năm 2026 có đáp án (5 đề)
Dưới đây là danh sách Đề thi Hóa học 12 Học kì 2 trắc nghiệm - tự luận năm 2026 có đáp án (5 đề). Hi vọng bộ đề thi này sẽ giúp bạn ôn luyện để đạt điểm cao trong bài thi Hóa học 12.
Đề thi Học kì 2 Hóa 12
Sở Giáo dục và Đào tạo .....
Đề thi Học kì 2
Môn: Hóa Học 12
Thời gian làm bài: 45 phút
(Đề 1)
Cho nguyên tử khối của các nguyên tố: C = 12, H = 1, O = 16, Al = 27, Ca = 40, Cl = 35,5, Mg = 24.
I. Phần trắc nghiệm
Câu 1: Kim loại sắt không phản ứng được với dung dịch nào sau đây?
A. H2SO4 loãng.
B. HNO3 loãng.
C. HNO3 đặc nguội.
D. H2SO4 đặc nóng.
Câu 2: Trong tự nhiên, canxi sunfat tồn tại dưới dạng ngậm nước (CaSO4.2H2O) được gọi là
A. boxit.
B. đá vôi.
C. thạch cao sống.
D. thạch cao nung.
Câu 3: Điện phân Al2O3 nóng chảy với dòng điện cường độ 9,65A trong thời gian 3000 giây, thu được 2,16 gam Al. Hiệu suất của quá trình điện phân là
A. 60%.
B. 70%.
C. 80%.
D. 90%.
Câu 4: Tôn là sắt được tráng kim loại nào sau đây?
A. Cr.
B. Zn.
C. Sn.
D. Ni.
Câu 5: Thực hiện các thí nghiệm sau ở nhiệt độ thường:
(a) Cho bột Al vào dung dịch NaOH.
(b) Cho bột Fe vào dung dịch AgNO3.
(c) Cho CaO vào nước.
(d) Cho dung dịch Na2CO3 vào dung dịch CaCl2.
Số thí nghiệm có xảy ra phản ứng là
A. 4.
B. 2.
C. 3.
D. 1.
Câu 6: Dẫn 4,48 lít khí CO2 ở đktc vào lượng dư dung dịch Ca(OH)2. Khối lượng kết tủa thu được là
A. 10g.
B. 20g.
C. 30g.
D. 40g.
Câu 7: Cho Cu vào dung dịch Fe2(SO4)3. Sau khi cân bằng phương trình thì tổng hệ số (số nguyên tối giản) của tất cả các chất là
A. 6.
B. 4.
C. 5.
D. 9.
Câu 8: Phát biểu nào sau đây là sai?
A. Dung dịch K2Cr2O7 có màu da cam.
B. Cr2O3 tan được trong dung dịch NaOH loãng.
C. CrO3 là oxit axit.
D. Trong hợp chất, crom có số oxi hóa đặc trưng là +2, +3, +6.
Câu 9: Nhóm những chất khí (hoặc hơi) nào dưới đây đều gây hiệu ứng nhà kính khi nồng độ của chúng trong khí quyển vượt quá tiêu chuẩn cho phép?
A. CO2 và O2.
B. CO2 và CH4.
C. CH4 và H2O.
D. N2 và CO.
Câu 10: Phương trình hóa học nào sau đây là sai?
A. Cu + 2FeCl3 (dung dịch) → CuCl2 + 2FeCl2.
B. 2Na + 2H2O → 2NaOH + H2.
C. H2 + CuO → Cu + H2O.
D. Fe + ZnSO4 (dung dịch) → FeSO4 + Zn.
Câu 11: Oxi hóa hoàn toàn 15,1g hỗn hợp bột các kim loại Cu, Zn, Al bằng oxi thu được 22,3g hỗn hợp oxit. Cho các oxit tan bằng lượng vừa đủ dung dịch HCl. Khối lượng muối khan thu được là
A. 47,05g.
B. 63,9g.
C. 31,075g.
D. Đáp án khác.
Câu 12: Cho m gam Mg vào dung dịch HNO3 dư. Sau phản ứng hoàn toàn, thu được dung dịch X và 1,12 lít khí NO (đkc, sản phẩm khử duy nhất của N+5). Giá trị của m là
A. 1,8.
B. 2,4.
C. 3,6.
D. 6,0.
Câu 13: Phương pháp điều chế Al là
A. Điện phân dung dịch AlCl3.
B. Dùng Na đẩy Al ra khỏi dung dịch AlCl3.
C. Điện phân nóng chảy Al2(SO4)3.
D. Điện phân nóng chảy Al2O3.
Câu 14: Kim loại dẫn điện tốt nhất là:
A. Cu.
B. Ag.
C. Al.
D. Fe.
Câu 15: Chất tác dụng với dung dịch Na2CO3 tạo khí thoát ra là
A. HCl.
B. Na2SO4.
C. FeSO4.
D. BaCl2.
II. Phần tự luận
Câu 1 (1,5 điểm): Bằng phương pháp hóa học hãy nhận biết các khí: CO, CO2, SO2 đựng trong các bình riêng biệt, mất nhãn.
Câu 2 (2 điểm): Nhúng một thanh sắt nặng 100 gam vào 100 ml dung dịch hỗn hợp gồm Cu(NO3)2 0,2M và AgNO3 0,2M. Sau một thời gian lấy thanh kim loại ra, rửa sạch làm khô cân được 101,72 gam (giả thiết các kim loại tạo thành đều bám hết vào thanh sắt). Tính khối lượng sắt đã phản ứng.
Câu 3 (2 điểm): Hòa tan hoàn toàn 1,23 gam hỗn hợp X gồm Cu và Al vào dung dịch HNO3 đặc, nóng thu được 1,344 lít khí NO2 (sản phẩm khử duy nhất, ở đktc) và dung dịch Y. Sục từ từ khí NH3 đến dư vào dung dịch Y, sau khi phản ứng xảy ra hoàn toàn thu được m gam kết tủa. Tính phần trăm khối lượng của Cu trong hỗn hợp X và giá trị của m.
Đáp án & Thang điểm
1. Phần trắc nghiệm (0,5 điểm/ 1 câu)
| Câu | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 |
| Đ/a | C | C | C | B | A | B | C | B | B | D | A | A | D | B | A |
Câu 1: Kim loại sắt không phản ứng được với dung dịch HNO3 đặc, nguội. Chọn đáp án C.
Câu 2: CaSO4.2H2O được gọi là thạch cao sống. Chọn đáp án C.
Câu 3:
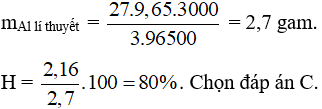
Câu 4: Tôn là sắt được tráng kim loại Zn. Chọn đáp án B.
Câu 5:
(a) 2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2
(b) Fe + 2AgNO3 → Fe(NO3)2 + 2Ag
(c) CaO + H2O → Ca(OH)2
(d) Na2CO3 + CaCl2 → CaCO3 + 2NaCl. Chọn đáp án A.
Câu 6:
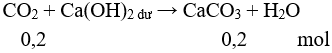
m↓ = 0,2.100 = 20 gam. Chọn đáp án B.
Câu 7: Cu + Fe2(SO4)3 → CuSO4 + 2FeSO4
Tổng hệ số (số nguyên tối giản) của tất cả các chất là 5. Chọn đáp án C.
Câu 8: Phát biểu sai: Cr2O3 tan được trong dung dịch NaOH loãng. Chọn đáp án B.
Câu 9: CO2 và CH4 đều gây hiệu ứng nhà kính khi nồng độ của chúng trong khí quyển vượt quá tiêu chuẩn cho phép. Chọn đáp án B.
Câu 10: Phương trình sai: Fe + ZnSO4 (dung dịch) → FeSO4 + Zn. Chọn đáp án D.
Câu 11: mO (oxit) = 22,3 – 15,1 = 7,2 gam → nO (oxit) = 0,45 mol
nHCl = 2.nO (oxit) = ngốc axit = 0,9 mol.
mmuối = mKL + mgốc axit = 15,1 + 0,9.35,5 = 47,05 gam. Chọn đáp án A.
Câu 12: Bảo toàn e: 2.nMg = 3.nNO → nMg = 0,075 mol → m = 0,075.24 = 1,8 gam. Chọn đáp án A.
Câu 13: Phương pháp điều chế Al là: Điện phân nóng chảy Al2O3. Chọn đáp án D.
Câu 14: Kim loại dẫn điện tốt nhất là Ag. Chọn đáp án B.
Câu 15: Na2CO3 + 2HCl → 2NaCl + CO2 + H2O. Chọn đáp án A.
2. Phần tự luận
Câu 1 (1,5 điểm): Dẫn từng khí lần lượt qua ống nghiệm đựng nước brom, khí nào làm mất màu nước brom là SO2
Hai khí còn lại dẫn qua ống nghiệm đựng nước vôi trong, khí nào làm xuất hiện vẩn đục trắng là CO2
SO2 + Br2 + H2O → 2HBr + H2SO4
CO2 + Ca(OH)2 dư → CaCO3 + H2O
Câu 2 (2 điểm): Tính được số mol Cu(NO3)2: 0,02 mol, số mol AgNO3: 0,02 mol
Phản ứng xảy ra theo thứ thự:
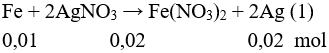
mthanh sắt = 100 + (0,02.108 – 0,01.56) =101,6 gam < 101,72 gam.
Xảy ra tiếp phản ứng:
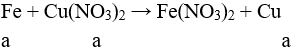
mthanh sắt = 100 + 0,02.108 + a.64 – 56.(0,01 + a) = 101,72
→ a = 0,015 mol
mFe pư = (0,01 + 0,015).56 = 1,4 gam.
Câu 3 (2 điểm): Tính được số mol NO2: 0,06 mol
Gọi số mol Al và Cu lần lượt là x và y mol
→ 27x + 64y = 1,23 (1)
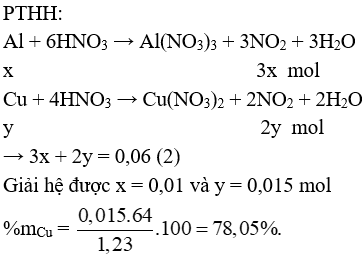
Dung dịch Y gồm: Al(NO3)3: 0,01 mol; Cu(NO3)2: 0,015 mol và có thể có HNO3 dư
PTHH tạo kết tủa:
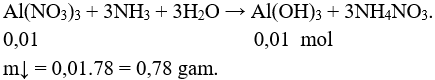
Chú ý: HS làm theo cách khác đúng vẫn cho điểm tối đa.
Sở Giáo dục và Đào tạo .....
Đề thi Học kì 2
Môn: Hóa Học 12
Thời gian làm bài: 45 phút
(Đề 2)

Cho nguyên tử khối của các nguyên tố: C = 12, H = 1, O = 16, Cu = 64, Fe = 56, Na = 23, K = 39, Zn = 65, Mg = 24, Ba = 137.
I. Phần trắc nghiệm
Câu 1: Cho 1,44 gam kim loại M (có hoá trị II) tác dụng với dung dịch H2SO4 loãng, dư. Sau phản ứng thu được dung dịch X và 1,344 lít khí (đkc). Kim loại M là
A. Ba.
B. Mg.
C. Zn.
D. Fe.
Câu 2: Chất nào sau đây gây ra tính cứng tạm thời của nước?
A. Ca(HCO3)2.
B. NaOH.
C. CaCl2.
D. HCl.
Câu 3: Nguyên tắc chung được dùng để điều chế kim loại là
A. cho hợp chất chứa ion kim loại tác dụng với chất khử.
B. oxi hoá ion kim loại trong hợp chất thành nguyên tử kim loại.
C. khử ion kim loại trong hợp chất thành nguyên tử kim loại.
D. cho hợp chất chứa ion kim loại tác dụng với chất oxi hoá.
Câu 4: Trường hợp nào sau đây dung dịch từ không màu chuyển sang màu xanh?
A. Nhúng lá nhôm vào dung dịch HCl.
B. Nhúng lá đồng vào dung dịch AgNO3.
C. Thêm vài giọt phenolphtalein vào dung dịch NaOH.
D. Thêm Fe vào dung dịch NH3 đặc.
Câu 5: Cho 3,84 gam Cu phản ứng với 80 ml dung dịch HNO3 1,0M thoát ra a lít NO. Nếu cho 3,84 gam Cu phản ứng với 80 ml dung dịch chứa HNO3 1,0M và H2SO4 0,5 M thoát b lít NO. Biết NO là sản phẩm khử duy nhất, các thể tích khí đo ở cùng điều kiện. Quan hệ giữa a và b là
A. b = a.
B. b = 2a.
C. 2b = 5a.
D. 2b = 3a.
Câu 6: Cho Cr tác dụng với O2 (to). Sản phẩm thu được là
A. CrO.
B. Cr2O3.
C. Cr3O4.
D. CrO3.
Câu 7: Hòa tan hoàn toàn 10,6 gam muối vô cơ X vào dung dịch H2SO4 loãng dư thu được 2,24 lít một chất khí Y có tỷ khối so với H2 là 22. X là chất nào sau đây?
A. NaHCO3.
B. Na2CO3.
C. K2SO3.
D. KHSO3.
Câu 8: Để hòa tan hoàn toàn 0,1 mol Fe2O3 và 0,1 mol Fe cần tối thiểu bao nhiêu lít dung dịch H2SO4 1M (loãng)?
A. 0,6.
B. 0,5.
C. 0,3.
D. 0,4.
Câu 9: Cu (Z = 29), cấu hình electron nguyên tử của đồng là
A. 1s22s22p63s23p63d94s2.
B. 1s22s22p63s23p63d104s1.
C. 1s22s22p63s23p63d84s3.
D. 1s22s22p63s23p63d104s2.
Câu 10: Tỉ lệ số người chết về bệnh phổi do hút thuốc lá gấp hàng chục lần số người không hút thuốc là. Chất gây nghiện và gây ung thư có trong thuốc lá là
A. nicotin.
B. aspirin.
C. cafein.
D. moocphin.
Câu 11: Cho phản ứng hóa học: Fe + CuSO4 → FeSO4 + Cu. Trong phản ứng trên xảy ra
A. sự oxi hóa Fe và sự oxi hóa Cu.
B. sự oxi hóa Fe và sự khử Cu2+.
C. sự khử Fe2+ và sự khử Cu2+.
D. sự khử Fe2+ và sự oxi hóa Cu.
Câu 12: Kim loại M phản ứng được với: dung dịch HCl, dung dịch Cu(NO3)2, dung dịch HNO3 (đặc, nguội). Kim loại M là
A. Fe.
B. Al.
C. Ag.
D. Zn.
Câu 13: Để nhận biết ion Fe2+ trong dung dịch ta dùng dung dịch
A. NaCl.
B. KOH.
C. K2SO4.
D. NaNO3.
Câu 14: Cho 5,6 gam Fe tác dụng với HNO3 đặc, nóng, dư, thu được V lít khí NO2 (sản phẩm khử duy nhất ở đktc). Giá trị của V là
A. 3,36.
B. 6,72.
C. 1,493.
D. 2,24.
Câu 15: Cho dãy các chất: NH4Cl, (NH4)2SO4, NaCl, MgCl2, FeCl2, AlCl3. Số chất trong dãy tác dụng với lượng dư dung dịch Ba(OH)2 tạo thành kết tủa là
A. 4.
B. 1.
C. 5.
D. 3.
II. Phần tự luận
Câu 1 (1,5 điểm): Bằng phương pháp hóa học, hãy phân biệt các dung dịch sau: NaCl, AlCl3, MgCl2 đựng trong các bình riêng biệt, mất nhãn.
Câu 2 (2 điểm): Cho hỗn hợp X gồm: Fe, ZnO và MgSO3 vào dung dịch H2SO4 (loãng, dư) thu được dung dịch Y và khí Z.
- Cho Z lội qua nước vôi trong dư thu được chất rắn G.
- Cho dd NaOH dư vào dung dịch Y thu được kết tủa Q và dung dịch R. Nung Q ngoài không khí đến khối lượng không đổi được chất rắn T. Biết các phản ứng xảy ra hoàn toàn. Xác định các chất có trong Y, Z, G, Q, R, T và viết các PTHH xảy ra.
Câu 3 (2 điểm): Nung nóng 46,6 gam hỗn hợp gồm Al và Cr2O3 (trong điều kiện không có không khí) đến khi phản ứng xảy ra hoàn toàn. Chia hỗn hợp thu được sau phản ứng thành hai phần bằng nhau. Phần một phản ứng vừa đủ với 300 ml dung dịch NaOH 1M (loãng), sau phản ứng thấy thoát ra V lít khí ở đktc. Để hòa tan hết phần hai cần vừa đủ dung dịch chứa a mol HCl. Tính giá trị của a và V.
Đáp án & Thang điểm
1. Phần trắc nghiệm (0,5 điểm/ 1 câu)
| Câu | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 |
| Đ/a | B | A | C | B | B | B | B | C | B | A | B | D | B | B |
Câu 1: Bảo toàn e: 2.nM = 2.nkhí → nM = 0,06 mol → MM = 1,44 : 0,06 = 24. Vậy M là Mg. Chọn đáp án B.
Câu 2: Ca(HCO3)2 gây ra tính cứng tạm thời của nước. Chọn đáp án A.
Câu 3: Nguyên tắc chung được dùng để điều chế kim loại là khử ion kim loại trong hợp chất thành nguyên tử kim loại. Chọn đáp án C.
Câu 4: Cu + 2AgNO3 (không màu) → Cu(NO3)2 (xanh) + 2Ag. Chọn đáp án B.
Câu 5:
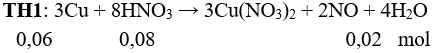
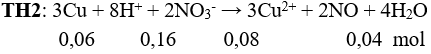
a : b = 0,02 : 0,04 = 1 : 2. Chọn đáp án B.
Câu 6: 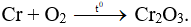
Câu 7: Mkhí = 2.22 = 44 → Loại đáp án C và D.
Giả sử A đúng:
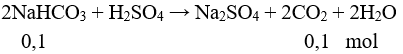
→ mmuối X = 0,1.84 = 8,4 gam ≠ 10,6 gam. Vậy A sai. Chọn đáp án B.
Câu 8:
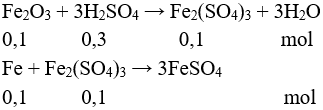
Vaxit = 0,3 lít. Chọn đáp án C.
Câu 9: Cu (Z = 29): 1s22s22p63s23p63d104s1. Chọn đáp án B.
Câu 10: Chất gây nghiện và gây ung thư có trong thuốc lá là nicotin. Chọn đáp án A.
Câu 11: Cho phản ứng hóa học: Fe + CuSO4 → FeSO4 + Cu. Trong phản ứng trên xảy ra sự oxi hóa Fe và sự khử Cu2+. Chọn đáp án B.
Câu 12: Kim loại Zn phản ứng được với: dung dịch HCl, dung dịch Cu(NO3)2, dung dịch HNO3 (đặc, nguội). Chọn đáp án D.
Câu 13: Để nhận biết ion Fe2+ trong dung dịch ta dùng dung dịch KOH. Hiện tượng: xuất hiện kết tủa màu trắng hơi xanh, hóa nâu đỏ trong không khí. Chọn đáp án B.
Câu 14: Bảo toàn e: 3.nFe = nkhí = 0,3 → Vkhí = 0,3.22,4 = 6,72 lít. Chọn đáp án B.
Câu 15: (NH4)2SO4 + Ba(OH)2 → BaSO4↓ + 2NH3 + 2H2O
MgCl2 + Ba(OH)2 → BaCl2 + Mg(OH)2 ↓
FeCl2 + Ba(OH)2 → BaCl2 + Fe(OH)2 ↓. Chọn đáp án D.
2. Phần tự luận
Câu 1 (1,5 điểm): Đánh số thứ thự từng lọ, trích mỗi lọ một ít dung dịch sang ống nghiệm đánh số tương ứng.
Chọn dung dịch NaOH làm thuốc thử.
Ống nghiệm nào xuất hiện kết tuả keo trắng, kết tủa tan khi thêm lượng dư NaOH là AlCl3.
Ống nghiệm nào xuất hiện kết tủa trắng, không tan khi dư NaOH là MgCl2.
Ống nghiệm nào không có hiện tượng xảy ra là NaCl.
PTHH:
3NaOH + AlCl3 → Al(OH)3 ↓+ 3NaCl
Al(OH)3 + NaOH → NaAlO2 + 2H2O
2NaOH + MgCl2 → Mg(OH)2 + 2NaCl
Câu 2 (2 điểm): Fe + H2SO4 → FeSO4 + H2
ZnO + H2SO4 → ZnSO4 + H2O
MgSO3 + H2SO4 → MgSO4 + SO2 + H2O
dd Y gồm: Fe SO4; ZnSO4; MgSO4 và H2SO4 dư
Khí Z gồm H2 và SO2
Z + dd nước vôi trong dư:
SO2 + Ca(OH)2 → CaSO3 + H2O
Vậy G là CaSO3
Y + dd NaOH dư
2NaOH + H2SO4 → Na2SO4 + 2H2O
FeSO4 + 2NaOH → Fe(OH)2↓ + Na2SO4
MgSO4 + 2NaOH → Mg(OH)2 ↓ + Na2SO4
ZnSO4 + 2NaOH → Zn(OH)2 ↓ + Na2SO4
Zn(OH)2 + 2NaOH → Na2ZnO2 + 2H2O
Kết tủa Q gồm: Mg(OH)2 và Fe(OH)2
dd R gồm: Na2SO4, Na2ZnO2, NaOH dư
Nung Q ngoài không khí
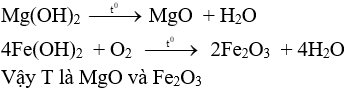
Câu 3 (2 điểm):
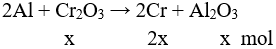
Theo bài ra Al dư, Đặt nCr2O3 pư = x mol, nAl dư = y mol
→ 52.2x + 102.x + 27y = 46,6 : 2
→ 206x + 27y = 23,3
Phần 1 :
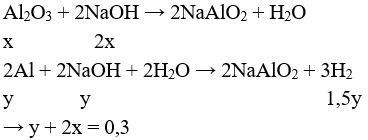
Giải hệ được : x = 0,1 mol; y = 0,1 mol
→ chất rắn mối phần chứa 0,2 mol Cr; 0,1 mol Al; 0,1 mol Al2O3.
Bảo toàn điện tích có:
nHCl = nCl- = 3.nAl3+ + 2.nCr+ = 3.2.0,1 + 3.0,1 + 2.0,2 = 1,3 mol
V = 0,15.22,4 = 3,36 lít.
Chú ý: HS làm theo cách khác đúng vẫn cho điểm tối đa.
Sở Giáo dục và Đào tạo .....
Đề thi Học kì 2
Môn: Hóa Học 12
Thời gian làm bài: 45 phút
(Đề 3)
Cho nguyên tử khối của các nguyên tố: C = 12, H = 1, O = 16, Cu = 64, N = 14, Mg = 24, Ba = 137, Al = 27, Cr = 52.
I. Phần trắc nghiệm
Câu 1: Ion Cu2+ oxi hóa được kim loại nào sau đây?
A. Al.
B. Au.
C. Ag.
D. Cu.
Câu 2: Để phân biệt CO2 và SO2 chỉ cần dùng thuốc thử là
A. nước brom.
B. CaO.
C. dung dịch Ba(OH)2.
D. dung dịch NaOH.
Câu 3: Hợp chất nào sau đây không tác dụng với dung dịch NaOH?
A. Cr(OH)2.
B. CrO3.
C. Cr(OH)3.
D. CrCl3.
Câu 4: Hấp thụ hoàn toàn 3,36 lít khí CO2 (đktc) vào 125 ml dung dịch Ba(OH)2 1M, thu được dung dịch X. Coi thể tích dung dịch không thay đổi, nồng độ mol của chất tan trong dung dịch X là
A. 0,6M.
B. 0,2M.
C. 0,1M.
D. 0,4M.
Câu 5: Nung 6,58 (g) Cu(NO3)2 trong bình kín không chứa không khí, sau một thời gian thu được 4,96 (g) chất rắn và hỗn hợp khí X. Hấp thụ hoàn toàn X vào nước để được 300 ml dung dịch Y. Dung dịch Y có pH bằng
A. 1.
B. 4.
C. 3.
D. 2.
Câu 6: Cho FeO tác dụng với dung dịch HCl. Vai trò của FeO là
A. chất oxi hoá.
B. oxit axit.
C. chất khử.
D. oxit bazơ.
Câu 7: Chất X có đặc điểm: Đốt trên ngọn lửa đèn khí, ngọn lửa chuyển sang màu vàng. X không tác dụng với dung dịch BaCl2. X là
A. NaHCO3.
B. K2CO3.
C. Na2CO3.
D. KHCO3.
Câu 8: Cho các dung dịch: HCl, NaOH đặc, NH3, KCl. Số dung dịch phản ứng được với Cu(OH)2 là
A. 1.
B. 3.
C. 2.
D. 4.
Câu 9: Cho hỗn hợp CuO và Fe vào dung dịch HNO3 loãng nguội. Nhận thấy CuO và Fe đều phản ứng hết. Sau phản ứng thu được dung dịch X, chất khí Y và chất rắn không tan Z. Cho dung dịch NaOH dư vào dung dịch X được kết tủa T. Kết tủa T phải chứa
A. Fe(OH)2 và Cu(OH)2.
B. Fe(OH)2.
C. Fe(OH)3 và Cu(OH)2.
D. Cu(OH)2.
Câu 10: Tác nhân chủ yếu gây mưa axit là
A. SO2 và NO2.
B. CH4 và NH3.
C. CO và CH4.
D. CO và CO2.
Câu 11: Sục khí CO2 đến dư vào dung dịch NaAlO2. Hiện tượng xảy ra là
A. có kết tủa nâu đỏ.
B. có kết tủa keo trắng, sau đó kết tủa lại tan.
C. có kết tủa keo trắng.
D. dung dịch vẫn trong suốt.
Câu 12: Thể tích dung dịch HNO3 1M (loãng) ít nhất cần dùng để hoà tan hoàn toàn một hỗn hợp gồm 0,15 mol Fe và 0,15 mol Cu là (biết phản ứng tạo chất khử duy nhất là NO)
A. 0,3 lít.
B. 0,6 lít.
C. 0,8 lít.
D. 1,0 lít.
Câu 13: Dãy nào sau đây chỉ gồm các chất vừa tác dụng được với dung dịch HCl, vừa tác dụng được với dung dịch AgNO3?
A. Fe, Ni, Sn.
B. Al, Fe, CuO.
C. Zn, Cu, Mg.
D. Hg, Na, Ca.
Câu 14: Cho luồng khí CO (dư) đi qua 9,1 gam hỗn hợp gồm CuO và Al2O3 nung nóng đến khi phản ứng hoàn toàn, thu được 8,3 gam chất rắn. Khối lượng CuO có trong hỗn hợp ban đầu là
A. 4,0 gam.
B. 0,8 gam.
C. 8,3 gam.
D. 2,0 gam.
Câu 15: Cho dãy các chất: Cr(OH)3, Al2(SO4)3, Mg(OH)2, Zn(OH)2, MgO, CrO3. Số chất trong dãy có tính chất lưỡng tính là
A. 4.
B. 5.
C. 3.
D. 2.
II. Phần tự luận
Câu 1 (1,5 điểm): Bằng phương pháp hóa học, hãy phân biệt các khí sau: CO2, SO2, H2S đựng trong các bình riêng biệt, mất nhãn.
Câu 2 (2 điểm): Hỗn hợp X gồm Na, Al và Fe (với tỉ lệ số mol giữa Na và Al tương ứng là 2 : 1). Cho X tác dụng với H2O (dư) thu được chất rắn Y và V lít khí. Cho toàn bộ Y tác dụng với dung dịch H2SO4 loãng (dư) thu được 0,25V lít khí. Biết các khí đo ở cùng điều kiện, các phản ứng đều xảy ra hoàn toàn. Xác định tỉ lệ số mol của Fe và Al trong X.
Câu 3 (2 điểm): Nung hỗn hợp bột gồm 15,2 gam Cr2O3 và m gam Al ở nhiệt độ cao. Sau khi phản ứng hoàn toàn, thu được 23,3 gam hỗn hợp rắn X. Cho toàn bộ hỗn hợp X phản ứng với axit HCl (nóng, dư) thoát ra V lít khí H2 (ở đktc). Tính giá trị của V.
Đáp án & Thang điểm
1. Phần trắc nghiệm (0,5 điểm/ 1 câu)
| Câu | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 |
| Đ/a | A | A | A | B | A | D | A | C | B | A | C | C | A | A | D |
Câu 1: 2Al + 3Cu2+ → 2Al3+ + 3Cu . Chọn đáp án A.
Câu 2: SO2 làm mất màu dung dịch brom còn CO2 thì không. Chọn đáp án A.
Câu 3: Cr(OH)2 không tác dụng với dung dịch NaOH. Chọn đáp án A.
Câu 4:
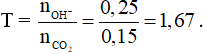
Sau phản ứng thu được 2 muối BaCO3 (x mol) và Ba(HCO3)2 ( y mol)
Bảo toàn C: x + 2y = 0,15.
Bảo toàn Ba: x + y = 0,125.
Giải hệ được: x = 0,1 và y = 0,025
CM chất tan = 0,025 : 0,125 = 0,2M. Chọn đáp án B.
Câu 5:
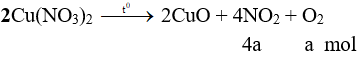
mkhí = 6,58 – 4,96 = 46.4a + 32a → a = 7,5.10-3 mol
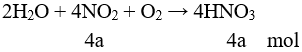
CM (HNO3) = 4a : 0,3 = 0,1 → pHY = 1. Chọn đáp án A.
Câu 6: FeO + 2HCl → FeCl2 + H2O
Vai trò của FeO là oxit bazơ. Chọn đáp án D.
Câu 7: Đốt trên ngọn lửa đèn khí, ngọn lửa chuyển sang màu vàng → X chứa nguyên tố Na.
X không tác dụng với dung dịch BaCl2. X là NaHCO3. Chọn đáp án A.
Câu 8: Các dung dịch: HCl, NH3 phản ứng được với Cu(OH)2. Chọn đáp án C.
Câu 9: CuO + 2HNO3 → Cu(NO3)2 + H2O
Fe + 4HNO3 → Fe(NO3)3 + NO + 2H2O
Fe dư + 2Fe(NO3)3 → 3Fe(NO3)2
Fedư + Cu(NO3)2 → Fe(NO3)2 + Cu.
Dung dịch X: Fe(NO3)2, chất khí Y: NO, chất rắn Z: Cu
Fe(NO3)2 + 2NaOH → Fe(OH)2 + 2NaNO3.
T chứa Fe(OH)2. Chọn đáp án B.
Câu 10: Tác nhân chủ yếu gây mưa axit là SO2 và NO2. Chọn đáp án A.
Câu 11: CO2 + NaAlO2 + 2H2O → Al(OH)3 ↓ + NaHCO3.
Hiện tượng xảy ra là có kết tủa keo trắng. Chọn đáp án C.
Câu 12: Để HNO3 là ít nhất thì phản ứng chỉ oxi hóa Fe → Fe2+.
Bảo toàn e: 3.nNO = 2.nFe + 2.nCu = 0,6 mol → nNO = 0,2 mol.
nHNO3 = 2.nFe + 2.nCu + nNO = 0,8 mol → V = 0,8 lít. Chọn đáp án C.
Câu 13: Fe, Ni, Sn vừa tác dụng được với dung dịch HCl, vừa tác dụng được với dung dịch AgNO3. Chọn đáp án A.
Câu 14: mChất rắn ↓ = mO (CuO) = 9,1 – 8,3 = 0,8 gam.
nO (CuO) = nCuO = 0,8 : 16 = 0,05 mol → mCuO = 0,05.80 = 4gam. Chọn đáp án A.
Câu 15: Cr(OH)3, Zn(OH)2 có tính chất lưỡng tính. Chọn đáp án D.
2. Phần tự luận
Câu 1 (1,5 điểm): Dẫn lần lượt từng khí qua ống nghiệm đựng nước vôi trong, nếu ống nghiệm xuất hiện vẩn đục trắng → khí là CO2 và SO2 (I), không hiện tượng là H2S.
Dẫn 2 khí ở nhóm I qua ống nghiệm đựng dung dịch brom, khí làm mất màu dung dịch brom là SO2, không hiện tượng là CO2.
PTHH:
SO2 + Ca(OH)2 → CaSO3 ↓ + H2O
CO2 + Ca(OH)2 → CaCO3 ↓ + H2O
SO2 + Br2 + 2H2O → 2HBr + H2SO4
Câu 2 (2 điểm): Gọi số mol Al là x mol → số mol Na là 2x mol
Cho X tác dụng với H2O
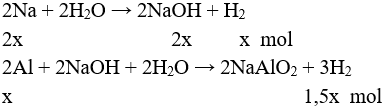
→ Vkhí = 2,5x.22,4 = V (1)
Chất rắn Y là Fe
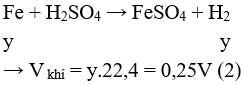
Lấy (2) : (1) được y : x = 5 : 8.
Câu 3 (2 điểm): Bảo toàn khối lượng: mCr2O3 + mAl = mcr sau → mAl = 8,1 gam
Tính được: số mol Cr2O3 = 0,1 mol, số mol Al = 0,3 mol

Chú ý: HS làm theo cách khác đúng vẫn cho điểm tối đa.
Sở Giáo dục và Đào tạo .....
Đề thi Học kì 2
Môn: Hóa Học 12
Thời gian làm bài: 45 phút
(Đề 4)
Cho nguyên tử khối của các nguyên tố: C = 12, H = 1, O = 16, Fe = 56, Cu = 64, Al = 27, Cr = 52.
I. Phần trắc nghiệm
Câu 1: Dung dịch Ba(HCO3)2 phản ứng với dung dịch nào sau đây không xuất hiện kết tủa?
A. Dung dịch Ba(OH)2.
B. Dung dịch NaOH.
C. Dung dịch HCl.
D. Dung dịch Na2CO3.
Câu 2: Tính chất vật lí của kim loại không do các electron tự do quyết định là
A. tính dẫn điện.
B. ánh kim.
C. khối lượng riêng.
D. tính dẫn nhiệt.
Câu 3: Trong công nghiệp, hai kim loại được điều chế bằng phương pháp điện phân nóng chảy hợp chất của chúng là
A. Al và Fe.
B. Na và Fe.
C. Cu và Ag.
D. Na và Al.
Câu 4: Cho dung dịch muối X đến dư vào dung dịch muối Y, thu được kết tủa Z. Hòa tan hoàn toàn Z vào dung dịch HNO3 (loãng, dư), thu được khí không màu hóa nâu trong không khí. X và Y lần lượt là
A. AgNO3 và FeCl2.
B. AgNO3 và FeCl3.
C. Na2CO3 và BaCl2.
D. AgNO3 và Fe(NO3)2.
Câu 5: Đồng thau là hợp kim
A. Cu – Zn.
B. Cu – Ni.
C. Cu – Sn.
D. Cu – Au.
Câu 6: Khử hoàn toàn m gam Fe2O3 cần vừa đủ 3,36 lít khí CO (ở đktc). Khối lượng sắt thu được sau phản ứng là
A. 8,4.
B. 5,6.
C. 2,8.
D. 16,8.
Câu 7: Cho các nhận xét sau:
(1) Al và Cr đều tác dụng được với dung dịch HCl và dung dịch NaOH.
(2) Dẫn khí CO2 đến dư vào dung dịch Ca(OH)2 thì cuối cùng thu được kết tủa.
(3) Kim loại dẫn điện tốt nhất là Au.
(4) Thêm NaOH vào dung dịch FeCl2 thì thu được kết tủa màu trắng xanh.
(5) Để phân biệt Al và Al2O3 ta có thể dùng dung dịch NaOH.
Số nhận xét không đúng là
A. 3.
B. 2.
C. 5.
D. 4.
Câu 8: Nhận định nào sau đây là sai?
A. Ở nhiệt độ thường, Ni bền với không khí và nước.
B. Kẽm là kim loại hoạt động, có tính khử mạnh hơn sắt.
C. Thiếc ở ô 50, nhóm IVA, chu kì 5 của bảng tuần hoàn.
D. Kẽm là kim loại lưỡng tính.
Câu 9: Một mẫu khí thải được sục vào dung dịch CuSO4, thấy xuất hiện kết tủa màu đen. Hiện tượng này do chất nào có trong khí thải gây ra?
A. H2S.
B. NO2.
C. SO2.
D. CO2.
Câu 10: Nhúng một tấm Fe có khối lượng 12g vào dung dịch CuCl2, sau một thời gian khối lượng của tấm kim loại tăng lên so với ban đầu là 0,5g. Hàm lượng Fe trong tấm sắt sau phản ứng là
A. 96,0%.
B. 68,0%.
C. 90,5%.
D. 56,5%.
Câu 11: Cho 31,2 gam hỗn hợp bột Al và Al2O3 tác dụng với dung dịch NaOH dư thoát ra 13,44 lít khí (đktc). Khối lượng mỗi chất trong hỗn hợp đầu là
A. 21,6 gam Al và 9,6 gam Al2O3.
B. 5,4 gam Al và 25,8 gam Al2O3.
C. 16,2 gam Al và 15,0 gam Al2O3.
D. 10,8 gam Al và 20,4 gam Al2O3.
Câu 12: Để phân biệt hai dung dịch KNO3 và Mg(NO3)2 đựng trong hai lọ riêng biệt, ta có thể dùng dung dịch
A. HCl.
B. NaOH.
C. NaCl.
D. MgCl2.
Câu 13: Khi dẫn từ từ khí CO2 đến dư vào dung dịch Ca(OH)2 thấy có
A. bọt khí và kết tủa trắng.
B. bọt khí bay ra.
C. kết tủa trắng xuất hiện.
D. kết tủa trắng, sau đó kết tủa tan dần.
Câu 14: Sục 2,24 lít khí CO2 (đktc) vào 150 ml dung dịch NaOH 1M. Sau khi phản ứng xảy ra hoàn toàn trong dung dịch có chứa
A. Na2CO3 và NaHCO3.
B. Na2CO3.
C. NaHCO3.
D. Na2CO3 và NaOH.
Câu 15: Trong các năng lượng sau đây, nhóm các nguồn năng lượng nào được coi là năng lượng sạch?
A. Nhiệt điện, hạt nhân, mặt trời.
B. Thủy điện, gió, mặt trời.
C. Hóa thạch, mặt tròi, thủy điện.
D. Thủy điện, gió, nhiệt điện.
II. Phần tự luận
Câu 1 (1,5điểm): Bằng phương pháp hóa học, hãy phân biệt các dung dịch sau: KCl, Na2SO4, NaNO3 chứa trong các lọ riêng biệt, mất nhãn.
Câu 2 (2 điểm): Cho 10 gam hỗn hợp kim loại gồm Fe, Cr và Al tác dụng với lượng dư dung dịch NaOH thấy thu được 0,672 lít khí ở đktc. Lấy phần chất rắn còn lại tác dụng với lượng dư HCl (khi không có không khí) thu được 3,808 lít khí ở đktc. Tính % khối lượng mỗi kim loại trong hỗn hợp ban đầu.
Câu 3 (2 điểm): Điện phân nóng chảy Al2O3 với anot than chì (hiệu suất điện phân 100%) thu được m kg Al ở catot và 67,2 m3 (ở đktc) hỗn hợp khí X có tỉ khối so với hiđro bằng 16. Lấy 2,24 lít (ở đktc) hỗn hợp khí X sục vào dung dịch nước vôi trong (dư) thu được 2 gam kết tủa. Tính giá trị của m.
Đáp án & Thang điểm
1. Phần trắc nghiệm (0,5 điểm/ 1 câu)
| Câu | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 |
| Đ/a | C | C | D | D | A | B | A | D | A | B | D | B | D | A | B |
Câu 1: Ba(HCO3)2 + 2HCl → BaCl2 + 2CO2 ↑ + 2H2O
Chọn đáp án C.
Câu 2: Khối lượng riêng của kim loại không do các electron tự do quyết định. Chọn đáp án C.
Câu 3: Trong công nghiệp, Na và Al được điều chế bằng phương pháp điện phân nóng chảy hợp chất của chúng. Chọn đáp án D.
Câu 4: AgNO3 + Fe(NO3)2 → Ag + Fe(NO3)3
Z là Ag.
3Ag + 4HNO3 → 3AgNO3 + NO + 2H2O. Chọn đáp án D.
Câu 5: Đồng thau là hợp kim Cu – Zn. Chọn đáp án A.
Câu 6:
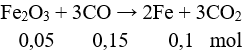
mFe = 0,1.56 = 5,6 gam. Chọn đáp án B.
Câu 7:
(1) Sai vì Cr không tác dụng được với dung dịch NaOH.
(2) Sai vì CO2 dư thì Ca(OH)2 + 2CO2 → Ca(HCO3)2 ⇒ không thu được ↓.
(3) Sai vì kim loại dẫn điện tốt nhất là Ag.
(4) Đúng vì: FeCl2 + 2NaOH → 2NaCl + Fe(OH)2↓ (trắng xanh).
(5) Đúng vì: 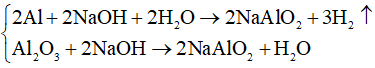
⇒ sủi bọt khí không màu là Al, còn lại là Al2O3.
⇒ (1), (2) và (3) sai ⇒ chọn đáp án A.
Câu 8: Nhận định sai: “Kẽm là kim loại lưỡng tính”. Chọn đáp án D.
Câu 9: CuSO4 + H2S → CuS (↓ đen) + H2SO4. Chọn đáp án A.
Câu 10:
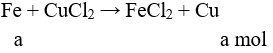
mKL tăng = 64a – 56a = 0,5 → a = 0,0625 mol
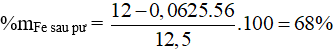
Câu 11: Bảo toàn e: 3.nAl = 2.nkhí → nAl = 0,4 mol → mAl = 0,4.27 = 10,8 gam. Chọn đáp án D.
Câu 12: Dùng dung dịch NaOH, xuất hiện kết tủa trắng → Mg(NO3)2, không hiện tượng là KNO3. Chọn đáp án B.
Câu 13: CO2 + Ca(OH)2 → CaCO3 ↓ + H2O
CaCO3 ↓ + H2O + CO2 dư → Ca(HCO3)2. Chọn đáp án D.
Câu 14: Đặt 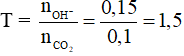
Câu 15: Nhóm các nguồn năng lượng nào được coi là năng lượng sạch: Thủy điện, gió, mặt trời. Chọn đáp án B.
2. Phần tự luận
Câu 1 (1,5điểm): Đánh số thứ tự từng lọ, trích mỗi lọ một ít sang ống nghiệm đánh số tương ứng.
Dùng BaCl2 làm thuốc thử, ống nghiệm nào xuất hiện kết tủa trắng là Na2SO4.
Không hiện tượng là: KCl và NaNO3 (I)
BaCl2 + Na2SO4 → BaSO4 ↓ + 2NaCl
Phân biệt nhóm I, dùng AgNO3, ống nghiệm nào xuất hiện kết tủa trắng là KCl, không hiện tượng là NaNO3
AgNO3 + KCl → AgCl ↓ + KNO3
Câu 2 (2 điểm): Gọi số mol Fe, Cr và Al lần lượt là x, y và z (mol)
→ 56x + 52y + 27z = 10 (1)
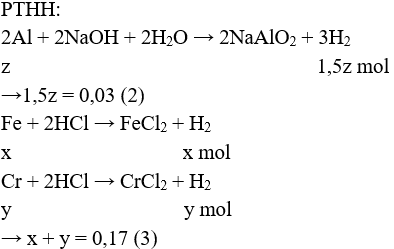
Giải hệ được: x = 0,155, y = 0,015, z = 0,02
Tính được %mFe = 86,8%; %mCr = 7,8%; %mAl = 5,4%.
Câu 3 (2 điểm):
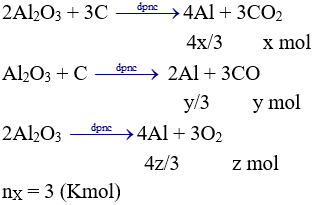
Trong 2,24 lít X: nCO2 = 0,02 mol; nCO = 0,08 mol;
Nếu X chỉ có CO và CO2 thì 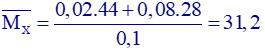
Trong X nCO2 = 0,6 (Kmol). Ta có hpt:
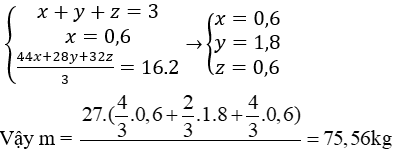
Chú ý: HS làm theo cách khác đúng vẫn cho điểm tối đa.
Sở Giáo dục và Đào tạo .....
Đề thi Học kì 2
Môn: Hóa Học 12
Thời gian làm bài: 45 phút
(Đề 5)
Cho nguyên tử khối của các nguyên tố: C = 12, H = 1, O = 16, Cu = 64, Zn = 65, Fe = 56, Al = 27.
I. Phần trắc nghiệm
Câu 1: Trong các phản ứng sau phản ứng nào sai?
A. 3Fe + 2O2 → Fe3O4
B. Fe + CuSO4 dd → FeSO4 + Cu
C. Fe + 2HCldd → FeCl2 + H2
D. Fe + Cl2 → FeCl2
Câu 2: Kim loại nào sau đây phản ứng mạnh với nước ở nhiệt độ thường ?
A. Ca
B. Fe
C. Cu
D. Ag.
Câu 3: Đốt cháy 11,9 gam hỗn hợp gồm Zn, Al trong khí Cl2 dư. Sau khi các phản ứng xảy ra hoàn toàn, thu được 40,3 gam hỗn hợp muối. Thể tích khí Cl2 (đktc) đã phản ứng là
A. 6,72 lít.
B. 11,2 lít.
C. 8,96 lít.
D. 17,92 lít.
Câu 4: Có 3 kim loại X, Y, Z thỏa mãn các tính chất sau:
- X tác dụng với dung dịch HCl, không tác dụng với dung dịch NaOH và dung dịch HNO3 đặc, nguội.
- Y tác dụng được với dung dịch HCl và dung dịch HNO3 đặc nguội, không tác dụng với dung dịch NaOH.
- Z tác dụng được với dung dịch HCl và dung dịch NaOH, không tác dụng với dung dịch HNO3 đặc nguội. X, Y, Z lần lượt có thể là
A. Fe, Mg, Zn.
B. Zn, Mg, Al.
C. Fe, Al, Mg.
D. Fe, Mg, Al.
Câu 5: Nhận định nào sau đây là đúng?
A. Cr là kim loại lưỡng tính.
B. Cr hoạt động hóa học mạnh hơn Zn và Fe.
C. Cr tác dụng với HNO3 đặc, nguội giải phóng NO2.
D. Cr bị thụ động hóa trong H2SO4 đặc, nguội.
Câu 6: Cho phản ứng hóa học sau: 2FeO + 4H2SO4 → Fe2(SO4)3 + SO2 + 2H2O. Trong phản ứng này FeO đóng vai trò là
A. chất oxi hóa.
B. vừa là chất khử, vừa là chất oxi hóa.
C. chất khử.
D. không là chất khử hay oxi hóa.
Câu 7: Để nhận biết ion nitrat, thường dùng Cu và dung dịch axit sulfuric loãng đun nóng là vì
A. Phản ứng tạo ra kết tủa màu vàng và dung dịch có màu xanh.
B. Phản ứng tạo ra dung dịch có màu xanh và khí không mùi làm xanh giấy quỳ ẩm.
C. Phản ứng tạo ra kết tủa màu xanh.
D. Phản ứng tạo dung dịch có màu xanh và khí không màu hóa nâu trong không khí.
Câu 8: Để đánh giá sự ô nhiễm kim loại nặng trong nước thải của một nhà máy, người ta lấy một ít nước, cô đặc rồi thêm dung dịch Na2S vào thấy xuất hiện kết tủa màu vàng. Hiện tượng trên chứng tỏ nước thải bị ô nhiễm bởi ion
A. Fe2+.
B. Cu2+.
C. Pb2+.
D. Cd2+.
Câu 9: Cho các hợp chất sau: Al2O3; Al(OH)3; MgO; FeO; Cr2O3; Cr(OH)3; CrO3; ZnO. Số hợp chất có tính lưỡng tính là
A. 5.
B. 6.
C. 7.
D. 8.
Câu 10: Cho 3,2 gam bột Cu tác dụng với 100 ml dung dịch hỗn hợp gồm HNO3 0,8M và H2SO4 0,2M. Sau khi các phản ứng xảy ra hoàn toàn, sinh ra V lít khí NO (sản phẩm khử duy nhất, ở đktc). Giá trị của V là
A. 0,746.
B. 0,448.
C. 1,792.
D. 0,672.
Câu 11: Để phân biệt các dung dịch hóa chất riêng biệt KOH, (NH4)2SO4, NH4Cl, K2SO4 có thể dùng hóa chất nào sau đây?
A. dd BaCl2.
B. dd AgNO3.
C. dd Ba(OH)2.
D. dd HCl.
Câu 12: Tiến hành các thí nghiệm sau:
(a) Cho dung dịch AgNO3 vào dung dịch HBr.
(b) Cho Al2O3 vào dung dịch NaOH loãng, dư.
(c) Cho Cu vào dung dịch H2SO4 đặc, nóng, dư.
(d) Cho dung dịch Ba(OH)2 vào dung dịch NaHCO3.
Sau khi kết thúc các phản ứng, số thí nghiệm thu được kết tủa là:
A. 3.
B. 2.
C. 1.
D. 4.
Câu 13: Cho dãy các chất: Cu, Fe3O4, NaHCO3 và Al(OH)3. Số chất trong dãy tác dụng được với dung dịch H2SO4 loãng là
A. 1.
B. 2.
C. 3.
D. 4.
Câu 14: Kim loại có những tính chất vật lý chung nào sau đây?
A. Tính dẻo, tính dẫn nhiệt, nhiệt độ nóng chảy cao.
B. Tính dẫn điện, tính dẫn nhiệt, có khối lượng riêng lớn, có ánh kim.
C. Tính dẻo, tính dẫn điện, tính dẫn nhiệt và có ánh kim.
D. Tính dẻo, có ánh kim, tính cứng.
Câu 15: Cho hỗn hợp X gồm 0,1 mol Na và 0,2 mol Al vào nước dư, sau phản ứng hoàn toàn thấy thoát ra V lít khí H2 (đktc). Giá trị của V là
A. 2,24.
B. 4,48.
C. 6,72.
D. 7,84.
II. Phần tự luận
Câu 1 (1,5 điểm): Viết các phương trình phản ứng xảy ra trong các thí nghiệm được mô tả sau:
a/ Hòa tan FeCl2 vào nước rồi thêm H2SO4 loãng dư, sau đó thêm dung dịch KMnO4 dư thấy có khí màu vàng lục thoát ra và dung dịch thu được có chứa muối mangan (II).
b/ Hòa tan Fe3O4 trong dung dịch H2SO4 đặc nóng dư được dung dịch A và khí B mùi hắc. Sục khí B vào dung dịch brom hoặc dung dịch KMnO4 đều thấy các dung dịch này bị nhạt màu.
Câu 2 (2 điểm): Hoà tan hoàn toàn 0,3 mol hỗn hợp gồm Al và Al4C3 vào dung dịch KOH (dư), thu được a mol hỗn hợp khí và dung dịch X. Sục khí CO2 (dư) vào dung dịch X, lượng kết tủa thu được là 46,8 gam. Tính giá trị của a.
Câu 3 (2 điểm): Cho một lượng bột Zn vào dung dịch X gồm FeCl2 và CuCl2. Khối lượng chất rắn sau khi các phản ứng xảy ra hoàn toàn nhỏ hơn khối lượng bột Zn ban đầu là 0,5 gam. Cô cạn phần dung dịch sau phản ứng thu được 13,6 gam muối khan. Tính khối lượng từng muối trong X.
Đáp án & Thang điểm
1. Phần trắc nghiệm (0,5 điểm/ 1 câu)
| Câu | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 |
| Đ/a | D | A | C | D | D | C | D | D | A | D | C | B | C | C | B |
Câu 1: 2Fe + 3Cl2 → 2FeCl3. Chọn đáp án D.
Câu 2: Ca phản ứng mạnh với nước ở nhiệt độ thường. Chọn đáp án A.
Câu 3: Bảo toàn khối lượng: mkhí = 40,3 – 11,9 = 28,4 gam → nkhí =0,4 mol.
→ Vkhí = 0,4.22,4 = 8,96 lít. Chọn đáp án C.
Câu 4:
- X tác dụng với dung dịch HCl, không tác dụng với dung dịch NaOH và dung dịch HNO3 đặc, nguội. X là Fe.
- Y tác dụng được với dung dịch HCl và dung dịch HNO3 đặc nguội, không tác dụng với dung dịch NaOH. Y là Mg.
- Z tác dụng được với dung dịch HCl và dung dịch NaOH, không tác dụng với dung dịch HNO3 đặc nguội. Z là Al.
Chọn đáp án D.
Câu 5: Nhận định đúng: Cr bị thụ động hóa trong H2SO4 đặc, nguội. Chọn đáp án D.
Câu 6: 2FeO + 4H2SO4 → Fe2(SO4)3 + SO2 + 2H2O. Số oxi hóa Fe tăng từ + 2 lên + 3.
FeO đóng vai trò là chất khử. Chọn đáp án C.
Câu 7: Để nhận biết ion nitrat, thường dùng Cu và dung dịch axit sulfuric loãng đun nóng là vì Phản ứng tạo dung dịch có màu xanh và khí không màu hóa nâu trong không khí. Chọn đáp án D.
Câu 8: Cd2+ + S2- → CdS ↓ vàng. Chọn đáp án D.
Câu 9: Hợp chất có tính lưỡng tính là Al2O3; Al(OH)3; Cr2O3; Cr(OH)3; ZnO. Chọn đáp án A.
Câu 10:
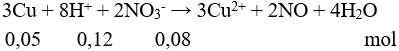
H+ hết → nNO = 0,12 : 4 = 0,03 mol → V = 0,672 lít. Chọn đáp án D.
Câu 11: Dùng Ba(OH)2, đun nóng
+/ Không hiện tượng → KOH
+/ Có khí không màu, mùi khai → NH4Cl
+ Có kết tủa trắng → K2SO4
+ Vừa có khí không màu, mùi khai, vừa có kết tủa trắng →(NH4)2SO4.
Câu 12:
(a) AgNO3 + HBr → AgBr ↓ + HNO3
(d) Ba(OH)2 + 2NaHCO3 → BaCO3↓ + Na2CO3 + 2H2O. Chọn đáp án B.
Câu 13: Các chất: Fe3O4, NaHCO3 và Al(OH)3 tác dụng được với dung dịch H2SO4 loãng. Chọn đáp án C.
Câu 14: Kim loại có những tính chất vật lý chung: Tính dẻo, tính dẫn điện, tính dẫn nhiệt và có ánh kim. Chọn đáp án C.
Câu 15:
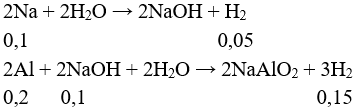
→ Vkhí = (0,05 + 0,15).22,4 = 4,48 lít. Chọn đáp án B.
2. Phần tự luận
Câu 1 (1,5 điểm):
a. Phương trình phản ứng:
10FeCl2 + 6KMnO4 + 24H2SO4 → 5Fe2(SO4)3 + 10Cl2 + 3K2SO4 + 6MnSO4 + 24H2O
b. 2Fe3O4 + 10H2SO4 (đặc nóng) → 3Fe2(SO4)3 + SO2 + 10H2O
Khí A là SO2:
SO2 + Br2 + 2H2O → H2SO4 + 2HBr
5SO2 + 2KMnO4 + 2H2O → K2SO4 + 2MnSO4+ 2H2SO4
Câu 2 (2 điểm): Đặt số mol Al là x, số mol Al4C3 là y mol
→ x + y = 0,3 mol (1)
Kết tủa là Al(OH)3: 0,6 mol
Bảo toàn Al: x + 4y = 0,6 (2)
Giải hệ phương trình được: x = 0,2 và y = 0,1
Khí gồm H2 và CH4
Bảo toàn e: có 2.nH2 = 3.nAl → nH2 = 0,3 mol
Bảo toàn C: có nCH4 = 3.nAl4C3 = 0,3
a = 0,3 + 0,3 = 0,6 mol.
Câu 3 (2 điểm): Gọi số mol CuCl2 và FeCl2 lần lượt là x và y (mol)
PTHH:
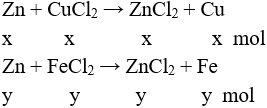
mCr↓ = 0,5 → 65 (x + y) – (64x + 56y) = 0,5
→ x + 9y = 0,5 (1)
Muối sau phản ứng là ZnCl2: 0,1 mol
→ x + y = 0,1 (2)
Giải hệ được: x = 0,05 và y = 0,05
mCuCl2 = 0,05.135 = 6,75g;
mFeCl2 = 0,05.127 = 6,35g.
Chú ý: HS làm theo cách khác đúng vẫn cho điểm tối đa.
Xem thêm bộ đề thi Hóa học 12 mới năm 2026 chọn lọc khác:
- [2021] Đề thi khảo sát chất lượng đầu năm Hóa học 12 (3 đề)
- Bộ 20 Đề thi Hóa học 12 Giữa học kì 1 năm 2026 tải nhiều nhất
- Đề thi Hóa học 12 Giữa học kì 1 năm 2026 có ma trận (15 đề)
- Đề thi Hóa học 12 Giữa kì 1 năm 2026 có đáp án (3 đề)
- Đề thi Hóa học 12 Giữa kì 1 năm 2026 có đáp án (3 đề)
- Đề thi Học kì 1 Hóa học 12 năm 2026 có đáp án (3 đề)
- Đề thi Hóa học 12 Giữa kì 2 trắc nghiệm năm 2026 có đáp án (3 đề)
- Đề thi Hóa học 12 Giữa kì 2 trắc nghiệm - tự luận năm 2026 có đáp án (5 đề)
- Đề thi Hóa học 12 Giữa kì 2 trắc nghiệm năm 2026 có đáp án (3 đề)
- Đề thi Hóa học 12 Giữa kì 2 trắc nghiệm - tự luận năm 2026 có đáp án (5 đề)
- Đề thi Hóa học 12 Học kì 2 trắc nghiệm năm 2026 có đáp án (3 đề)
Để học tốt lớp 12 các môn học sách mới:
- Giải bài tập Lớp 12 Kết nối tri thức
- Giải bài tập Lớp 12 Chân trời sáng tạo
- Giải bài tập Lớp 12 Cánh diều
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Giáo án lớp 12 (các môn học)
- Giáo án điện tử lớp 12 (các môn học)
- Giáo án Toán 12
- Giáo án Ngữ văn 12
- Giáo án Vật Lí 12
- Giáo án Hóa học 12
- Giáo án Sinh học 12
- Giáo án Địa Lí 12
- Giáo án Lịch Sử 12
- Giáo án Lịch Sử 12 mới
- Giáo án GDCD 12
- Giáo án Kinh tế Pháp luật 12
- Giáo án Tin học 12
- Giáo án Công nghệ 12
- Giáo án GDQP 12
- Đề thi lớp 12 (các môn học)
- Đề thi Ngữ văn 12
- Đề thi Toán 12
- Đề thi Tiếng Anh 12 mới
- Đề thi Tiếng Anh 12
- Đề thi Vật Lí 12
- Đề thi Hóa học 12
- Đề thi Sinh học 12
- Đề thi Địa Lí 12
- Đề thi Lịch Sử 12
- Đề thi Giáo dục Kinh tế Pháp luật 12
- Đề thi Giáo dục quốc phòng 12
- Đề thi Tin học 12
- Đề thi Công nghệ 12






 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

