Đề thi Hóa học 12 Giữa kì 2 trắc nghiệm năm 2026 có đáp án (3 đề)
Dưới đây là danh sách Đề thi Hóa học 12 Giữa kì 2 trắc nghiệm năm 2026 có đáp án (3 đề). Hi vọng bộ đề thi này sẽ giúp bạn ôn luyện để đạt điểm cao trong bài thi Hóa học 12.
Đề thi Hóa học 12 Giữa kì 2
Chỉ từ 150k mua trọn bộ Đề thi Hóa học 12 Giữa kì 2 theo cấu trúc mới bản word có lời giải chi tiết:
- B1: gửi phí vào tk:
1133836868- CT TNHH DAU TU VA DV GD VIETJACK - Ngân hàng MB (QR) - B2: Nhắn tin tới Zalo VietJack Official - nhấn vào đây để thông báo và nhận đề thi
Đề thi Giữa kì 2 - Trắc nghiệm
Sở Giáo dục và Đào tạo .....
Đề thi Giữa học kì 1
Môn: Hóa Học 12
Thời gian làm bài: 45 phút
(Đề 1)

Cho nguyên tử khối một số nguyên tố: H = 1, C = 12, N = 14, O = 16, Na = 23, Mg = 24, S = 32, Cl = 35,5, K = 39, Ca = 40, Ba = 137, Cu = 64, Ag = 108.
Câu 1: Trường hợp nào dưới đây không có sự phù hợp giữa tên quặng sắt và công thức hợp chất chính có trong quặng?
A. Manhetit chứa Fe2O3.
B. Pirit sắt chứa FeS2 .
C. Hematit nâu chứa Fe2O3.nH2O
D. Xiđerit chứa FeCO3.
Câu 2: Điện phân nóng chảy Al2O3 với anot than chì (hiệu suất điện phân 100%) thu được m kg Al ở catot và 67,2 m3 (ở đktc) hỗn hợp khí X có tỉ khối so với hiđro bằng 16. Lấy 2,24 lít (ở đktc) hỗn hợp khí X sục vào dung dịch nước vôi trong (dư) thu được 2 gam kết tủa. Giá trị của m là
A. 108,0.
B. 67,5.
C. 54,0.
D. 75,6.
Câu 3: Để luyện được 500 tấn thép cacbon (thành phần gồm Fe và C) chứa 1,4% C, cần dùng x tấn quặng hematit đỏ chứa 0% tạp chất trơ. Hiệu suất quá trình là 75%. Giá trị của x là
A. 939,05.
B. 528,21.
C. 1878,10.
D. 1056,43.
Câu 4: Hỗn hợp X gồm: Al, Al2O3, Al(OH)3. X tan hoàn toàn trong
A. H2SO4 đặc, nguội, dư.
B. dd NaOH dư.
C. dd CuCl2 dư.
D. HNO3 đặc, nguội.
Câu 5: Cho phản ứng sau: a Al + b HNO3 → c Al(NO3)3 + d N2O + e H2O. Sau khi cân bằng, tổng giá trị của (a + b + d) là
A. 41.
B. 23.
C. 25.
D. 14.
Câu 6: Nung nóng m gam hỗn hợp Al và Fe2O3 (trong môi trường không có không khí) đến khi phản ứng xảy ra hoàn toàn, thu được hỗn hợp rắn Y. Chia Y thành hai phần bằng nhau:
- Phần 1 tác dụng với dung dịch H2SO4 loãng (dư), sinh ra 3,08 lít khí H2 (ở đktc).
- Phần 2 tác dụng với dung dịch NaOH (dư), sinh ra 0,84 lít khí H2 (ở đktc). Giá trị của m là
A. 22,75
B. 21,40.
C. 29,40.
D. 29,43.
Câu 7: Nhôm bền trong môi trường không khí và nước là do
A. Nhôm là kim loại thụ động trong HNO3 đặc nguội và H2SO4 đặc, nguội.
B. Nhôm có tính dẫn điện tốt.
C. Có màng oxit Al2O3 bền vững bảo vệ.
D. Có màng hiđroxit Al(OH)3 bền vững bảo vệ.
Câu 8: Phèn chua được dùng trong ngành công nghiệp thuộc da, công nghiệp giấy, chất cầm màu trong nhuộm vải … Công thức hoá học của phèn chua là
A. Na2SO4.2Al2(SO4)3.24H2O.
B. 2K2SO4.FeSO4.24H2O.
C. NaFe(SO4)2.12H2O.
D. K2SO4.Al2(SO4)3.24H2O.
Câu 9: Fe phản ứng được với tất cả các chất trong nhóm nào sau đây?
A. NaOH; C; CuCl2; Cl2.
B. H2SO4 (đặc, nguội); FeCl3.
C. HNO3 loãng; S.
D. Al2O3; HNO3 đặc.
Câu 10: Quặng nào sau đây là tốt nhất để luyện Gang?
A. Fe2O3.
B. FeS2.
C. Fe2O3.nH2O.
D. Fe3O4.
Câu 11: Phát biểu nào sau đây đúng?
A. Nhôm là một kim loại lưỡng tính.
B. Al(OH)3 là một hiđroxit lưỡng tính.
C. AlCl3, Al2O3 đều là chất lưỡng tính.
D. Al(OH)3 tan trong dung dịch NH3 dư.
Câu 12: Phản ứng hóa học xảy ra trong trường hợp nào dưới đây không thuộc loại phản ứng nhiệt nhôm?
A. Al tác dụng với Fe2O3 nung nóng.
B. Al tác dụng với CuO nung nóng.
C. Al tác dụng với Fe3O4 nung nóng.
D. Al tác dụng với axit H2SO4 đặc nóng.
Câu 13: Tính chất vật lí nào sau đây không phải là tính chất vật lí của Al?
A. Dẫn điện và dẫn nhiệt tốt.
B. Kim loại nhẹ.
C. Có tính nhiễm từ.
D. Màu trắng, dẻo.
Câu 14: Khi nung Fe với iốt trong môi trường trơ thu được sản phẩm X. Công thức của X là
A. Fe3O4 .
B. Fe2I.
C. FeI2.
D. FeI3.
Câu 15: Xét 2 phương trình phản ứng theo sơ đồ sau:
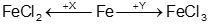
A. HCl, FeCl3.
B. Cl2 , HCl.
C. CuCl2 , Cl2.
D. Cl2 , FeCl3.
Câu 16: Có các kim loại Cu, Al, Fe và các dung dịch muối CuCl2, Fe(NO3)3, AgNO3 . Kim loại tác dụng được với 2 trong 3 dung dịch muối là
A. Cu.
B. Al .
C. Fe.
D. Al, Fe.
Câu 17: Khi cho bột sắt vào dd AgNO3 dư, hãy cho biết có những phản ứng nào sau đây xảy ra trong thí nghiệm?
Fe + 2Ag+ → Fe2+ + 2Ag↓(1)
Fe + 3Ag+ → Fe3+ + 3Ag↓(2)
Fe + 2Fe3+ → 3Fe2+ (3)
Fe2+ + Ag+ → Fe3+ + Ag↓(4)
A. (2) và (3).
B. (1) và (3).
C. (1).
D. (1) và (4).
Câu 18: Quặng chính để sản xuất Al là?
A. Boxit.
B. Saphia.
C. Đất sét.
D. Mica.
Câu 19: Al không tan trong dung dịch nào sau đây?
A. H2SO4 đặc, nóng.
B. NaOH.
C. H2SO4 loãng.
D. HNO3 đặc, nguội.
Câu 20: Đốt Fe dư trong hơi Brom thu được hỗn hợp gồm 2 chất rắn. Hãy cho biết thành phần của chất rắn đó:
A. FeBr2 và Fe.
B. FeBr3, Br2.
C. FeBr3 và Fe.
D. FeBr2 và FeBr3.
Câu 21:Biết cấu hình của Fe3+ là: [Ar]3d5. Tổng số e trong nguyên tử của Fe là
A. 26.
B. 23.
C. 15.
D. 56.
Câu 22: Nung hỗn hợp bột gồm Al và Fe3O4 trong bình kín (không có không khí) đến khi phản ứng hoàn toàn, thu được hỗn hợp X. Cho X vào nước vôi trong dư, thấy không có khí thoát ra. Vậy hỗn hợp X gồm
A. Al2O3, Fe2O3, Fe.
B. Al2O3, Fe.
C. Al2O3, Fe3O4, Al.
D. Al2O3, Fe, Al.
Câu 23: Cho các hợp kim sau: Al-Fe (I); Zn-Fe (II); Fe-C (III); Sn-Fe (IV). Khi tiếp xúc với dung dịch chất điện li, số hợp kim Fe bị ăn mòn trước là
A. 3.
B. 1.
C. 2.
D. 4.
Câu 24: Cho m gam hỗn hợp G gồm: Na, Al, Fe vào nước dư thu được 4,48 lít khí (ở đktc).
Mặt khác cho m gam G ở trên vào dung dịch NaOH dư thu được 7,84 lít khí (ở đktc) và dung dịch X, chất rắn Y. Hòa tan hoàn toàn Y vào H2SO4 đặc, nóng thu được 5,04 lít khí (ở đktc).
Giá trị của m là
A. 23,9.
B. 47,8.
C. 16,1.
D. 32,2
Câu 25: Quá trình tạo Gang và tạo xỉ xảy ra ở bộ phận nào của Lò cao?
A. Thân lò.
B. Phía trên của nồi lò.
C. Bụng lò.
D. Nồi lò.
Câu 26: Cho các khẳng định sau:
(1) Al là kim loại nặng hơn Ba.
(2) Al là kim loại dẫn điện bằng 2/3 Cu và nhẹ bằng 1/3 Cu.
(3) Al là kim loại dẻo nhất trong các kim loại.
(4) Trong điện phân Al2O3 nóng chảy, Al sinh ra ở trạng thái lỏng.
Khẳng định đúng là
A. (2) và (4).
B. (1) và (4).
C. (2) và (3).
D. (1), (3) và (4).
Câu 27: Cho m gam Fe vào dung dịch HCl dư thu được 5,04 lít khí ở đktc. Giá trị của m là
A. 8,4.
B. 12,6.
C. 6,3.
D. 5,04.
Câu 28: Cho 0,01 mol Fe vào 50ml dung dịch AgNO3 1M khi phản ứng kết thúc khối lượng AgNO3 thu được là
A. 3,6.
B. 3,24.
C. 2,16.
D. 1,08.
Câu 29: Tính chất nào sau đây là tính chất chung của các hợp chất: FeO, Fe3O4, Fe2O3?
A. Tính lưỡng tính.
B. Tính oxi hóa và tính khử.
C. Tính khử.
D. Tính oxi hoá.
Câu 30: Cho 5,6 gam Fe tác dụng với HNO3 loãng dư, thu được V lít khí NO (sản phẩm khử duy nhất ở đktc). Giá trị của V là
A. 3,36.
B. 6,72.
C. 1,493.
D. 2,24.
Đáp án & Thang điểm
Câu 1. A
Manhetit chứa Fe3O4.
Câu 2. D
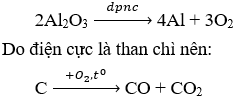
Vậy khí X có thể có: CO; CO2 và O2
Đặt số mol của CO; CO2 và O2 có trong 2,24 lít khí X lần lượt là a, b và c (mol)
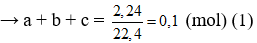
Có MX = 16.2 = 32 → mX = 28a + 44b + 32c = 32.0,1 = 3,2 (gam) (2)
Sục X vào Ca(OH)2 dư:
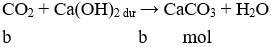
→ n↓ = b = 0,02 (mol) (3)
Từ (1); (2) và (3) có: a = 0,06; b = 0,02 và c = 0,02.
Bảo toàn O có số mol O2thu được sau điện phân là:
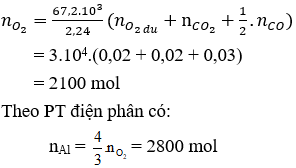
→ mAl = 2800.27 = 75600 gam = 75,6 kg.
Câu 3. A
Ta có sơ đồ:
Fe2O3 → 2Fe
160g → 2.56g
x tấn → 500.98,6% tấn
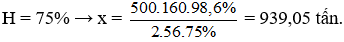
Câu 4. B
2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2
Al2O3 + 2NaOH → 2NaAlO2 + H2O
Al(OH)3 + NaOH → NaAlO2 + 2H2O
Câu 5. A
8 Al + 30 HNO3 → 8 Al(NO3)3 + 3 N2O + 15 H2O
→ a + b + d = 8 + 30 + 3 = 41.
Câu 6. A
Hỗn hợp sau phản ứng phản ứng với NaOH → sau khi nung nóng hỗn hợp có Al dư. Chất rắn Y gồm Al dư; Fe; Al2O3
Phần 2: Áp dụng định luật bảo toàn electron:
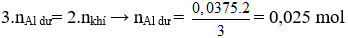
Phần 1: Áp dụng định luật bảo toàn electron:
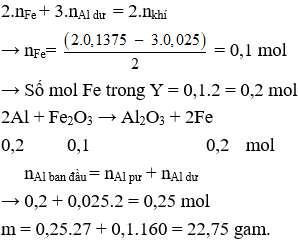
Câu 7. C
Nhôm bền trong môi trường không khí và nước do nhôm có màng oxit Al2O3 bảo vệ.
Câu 8. D
Phèn chua: K2SO4.Al2(SO4)3.24H2O.
Câu 9. C
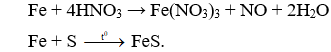
Câu 10. D
Quặng có hàm lượng sắt cao nhất khi luyện gang sẽ có hiệu quả cao nhất.
→ Quặng tốt nhất đề luyện gang là Fe3O4.
Câu 11. B
A sai vì không có khái niệm kim loại lưỡng tính.
C sai vì AlCl3 không phải là chất lưỡng tính.
D sai vì Al(OH)3 không tan trong NH3 dư.
Câu 12. D
Phản ứng nhiệt nhôm là phản ứng của nhôm với oxit kim loại
→ Al tác dụng với axit H2SO4 đặc nóng không phải là phản ứng nhiệt nhôm.
Câu 13. C
Nhôm không có tính nhiễm từ.
Câu 14. C
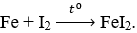
Câu 15. C
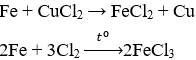
Câu 16. A
Cu + CuCl2 → không phản ứng
2Cu + 2FeCl3 → CuCl2 + 2FeCl2
Cu + 2AgNO3 → Cu(NO3)2 + 2Ag.
Câu 17. D
Câu 18. A
Quặng chính để sản xuất nhôm là quặng boxit.
Câu 19. D
Al bị thụ động hóa trong HNO3 đặc, nguội.
Câu 20. C
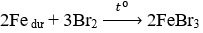
Câu 21. A
Fe → Fe3+ + 3e
→ Cấu hình electron của Fe là: [Ar]3d64s2.
Vậy số electron trong nguyên tử Fe là: 26.
Câu 22. B
Do khi cho X vào nước vôi trong dư không thấy có khí thoát ra nên trong X không có Al dư.
Lại có phản ứng hoàn toàn nên X là Al2O3 và Fe.
Câu 23. C
Fe bị ăn mòn trước khi điện cực còn lại là chất có tính khử yếu hơn
Hợp kim trong đó Fe bị ăn mòn trước là: Fe-C (III); Sn-Fe (IV).
Câu 24. C
Gọi số mol Na, Al và Fe có trong m gam G lần lượt là x, y và z (mol)
Do khi cho G vào nước thu được số mol khí ít hơn khi cho G vào NaOH dư nên khi cho G vào nước dư chỉ có Na phản ứng hết.
PTHH:
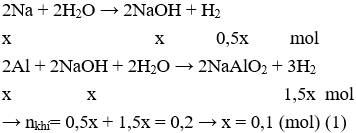
Cho G vào KOH dư, Na và Al phản ứng hết, chất rắn Y là Fe không phản ứng.
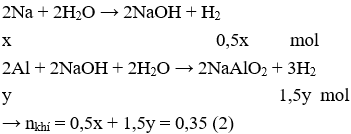
Thay (1) vào (2) được: y = 0,2 (mol).
Cho Y vào H2SO4 đặc, nóng có phản ứng:
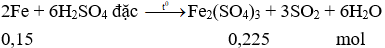
Vậy m = 0,1. 23 + 0,2.27 + 0,15.56 = 16,1 (gam).
Câu 25. C
Quá trình tạo gang và xỉ xảy ra ở bụng lò.
Câu 26. A
(1) sai Al nhẹ hơn Ba.
(3) sai vì Au dẻo hơn Al.
Câu 27. B
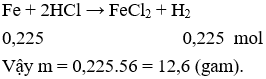
Câu 28. B
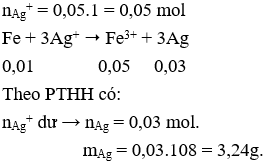
Câu 29. D
FeO, Fe3O4, Fe2O3 đều có tính oxi hóa.
Câu 30. D
Bảo toàn electron có: 3.nFe = 3.nNO → nNO = nFe = 0,1 mol
→ V = 0,1.22,4 = 2,24 lít.
Sở Giáo dục và Đào tạo .....
Đề thi Giữa học kì 1
Môn: Hóa Học 12
Thời gian làm bài: 45 phút
(Đề 2)
Cho nguyên tử khối: H = 1, N = 14, O = 16, S = 32, Mg = 24, Fe = 64, Fe = 56, Cl = 35,5, Cr = 52, Al = 27, Na = 23, K = 39, Zn = 65, Mn = 55.
Câu 1: Crom không tan được trong dung dịch
A. H2SO4 đặc, nguội.
B. HNO3 đặc, nóng.
C. HCl đặc.
D. HBr đặc, nguội.
Câu 2: Đốt Fe trong khí clo thiếu thu được hỗn hợp gồm 2 chất rắn. Thành phần của chất rắn đó là
A. FeCl2 và FeCl3.
B. Fe, FeCl2, FeCl3.
C. FeCl2 và Fe.
D. FeCl3 và Fe.
Câu 3: Thuốc thử duy nhất để nhận biết các dung dịch: FeCl2, FeCl3, CrCl3, CuCl2 là
A. Dung dịch H2SO4 loãng.
B. Quỳ tím.
C. Dung dịch Ba(OH)2 dư.
D. Dung dịch HCl.
Câu 4: Hoà tan 5,6 gam Fe bằng dung dịch H2SO4 loãng (dư), thu được dung dịch X. Dung dịch X phản ứng vừa đủ với V ml dung dịch KMnO4 0,5M. Giá trị của V là
A. 20.
B. 80.
C. 60.
D. 40.
Câu 5: Khối lượng K2Cr2O7 tác dụng vừa đủ với 0,6 mol FeSO4 trong môi trường H2SO4 loãng là
A. 26,4 gam.
B. 29,4agam.
C. 27,4 gam.
D. 28,4 gam.
Câu 6: Khi cho 41,4 gam hỗn hợp X gồm Fe2O3, Cr2O3 và Al2O3 tác dụng với dung dịch NaOH đặc (dư), sau phản ứng thu được chất rắn có khối lượng 16 gam. Để khử hoàn toàn 41,4 gam X bằng phản ứng nhiệt nhôm, phải dùng 10,8 gam Al. Thành phần phần trăm theo khối lượng của Cr2O3 trong hỗn hợp X là
A. 50,67%.
B. 36,71%.
C. 66,67%.
D. 20,33%.
Câu 7: Cho 5,2 gam Cr tác dụng với HNO3 loãng dư, thu được V lít khí NO (sản phẩm khử duy nhất ở đktc). V có giá trị là
A. 3,36.
B. 6,72.
C. 2,24.
D. 4,48.
Câu 8: Cần bao nhiêu tấn quặng manhetit chứa 80% Fe3O4 để có thể luyện được 800 tấn gang có hàm lượng 95%? Biết lượng Fe hao hụt trong sản xuất là 1%.
A. 5213,61 tấn.
B. 1325,16 tấn.
C. 3512,61 tấn.
D. 2351,16 tấn.
Câu 9: Tính chất nào sau đây là tính chất chung của các hợp chất: FeO, Fe2O3, Fe(OH)2, Fe(OH)3?
A. Tính khử.
B. Tính bazơ.
C. Tính oxi hoá.
D. Tính axit.
Câu 10: Hoà tan hỗn hợp 3 kim loại gồm Al, Fe và Cr vào dung dịch NaOH dư, thu được 6,72L khí và 10,8g chất rắn. Cho chất rắn này tác dụng với dung dịch HCl (dư) thu được 4,48L khí. Các chất khí đo ở đktc. Hàm lượng %Cr có trong hỗn hợp ban đầu là
A. 35,21.
B. 33,33.
C. 32,1.
D. 34,57.
Câu 11: Có các kim loại Cu, Ag, Fe và các dung dịch muối Cu(NO3)2, Fe(NO3)3, AgNO3 . Kim loại nào tác dụng được với cả 3 dung dịch muối ?
A. Cu, Fe.
B. Cu.
C. Ag .
D. Fe.
Câu 12: Khi cho bột sắt dư vào dd AgNO3, hãy cho biết có những phản ứng nào sau đây xảy ra?
Fe + 2Ag+ → Fe2+ + 2Ag↓(1)
Fe + 3Ag+ → Fe3+ + 3Ag↓(2)
Fe + 2Fe3+ → 3Fe2+ (3)
Fe2+ + Ag+ → Fe3+ + Ag↓(4)
A. (1) (4) và (3).
B. (2) và (3).
C. (1).
D. Đáp án khác.
Câu 13: Cho 6,72 gam Fe vào 400 ml dung dịch HNO3 1M, đến khi phản ứng xảy ra hoàn toàn, thu được khí NO (sản phẩm khử duy nhất) và dung dịch X. Dung dịch X có thể hoà tan tối đa m gam Cu. Giá trị của m là
A. 3,20.
B. 3,84.
C. 1,92.
D. 0,64.
Câu 14: Tính chất vật lí nào sau đây không phải là tính chất vật lí của sắt?
A. Có tính nhiễm từ.
B. Màu trắng xám, giòn, dễ rèn.
C. Kim loại nặng.
D. Dẫn điện và dẫn nhiệt tốt.
Câu 15: Các số oxi hoá đặc trưng của Crom trong hợp chất là
A. +2, +4, +6.
B. +2, +3, +6.
C. +3, +4, +6.
D. +1, +2, +4, +6.
Câu 16: Hoà tan hoàn toàn 2,81 gam hỗn hợp gồm Fe2O3, MgO, ZnO trong 500 ml axit H2SO4 0,1M (vừa đủ). Sau phản ứng, hỗn hợp muối sunfat khan thu được khi cô cạn dung dịch có khối lượng là
A. 5,81 gam.
B. 6,81 gam.
C. 4,81 gam.
D. 3,81 gam.
Câu 17:Dãy chất nào sau đây phản ứng với cả 2 dung dịch HCl và KOH?
A. ZnO, CrO3, Cr(OH)2.
B. ZnO, CrO3, Cr(OH)3.
C. ZnO, Cr2O3, Cr(OH)2.
D. Cr2O3, ZnO, Cr(OH)3.
Câu 18: Trường hợp nào dưới đây không có sự phù hợp giữa tên quặng sắt và công thức hợp chất chính có trong quặng?
A. Pirit chứa FeS2.
B. Manhetit chứa Fe3O4.
C. Xiđerit chứa FeCO3.
D. Hematit nâu chứa Fe2O3.
Câu 19: Phản ứng nào sau đây không đúng?
A. 2FeO + 4H2SO4 đặc → Fe2(SO4)3 + SO2 + 4H2O.
B. Fe3O4 + 4H2SO4 loãng → Fe2(SO4)3 + 4H2O.
C. 2Fe + 6H2SO4 đặc → Fe2(SO4)3 + 3SO2 + 6H2O.
D. 6FeCl2 + 3Br2 → 2FeBr3 + 4FeCl3.
Câu 20: Cho sơ đồ phản ứng sau : chất X + H2SO4 → FeSO4 + SO2 + H2O. Hãy cho biết, chất X có thể là chất nào trong số các chất sau:
A. FeSO3.
B. Fe.
C. FeS.
D. Tất cả đều thoả mãn.
Câu 21: Chọn câu đúng:
A. Khi thêm dung dịch bazơ vào muối cromat màu vàng sẽ tạo thành đicromat có màu da cam.
B. Khi thêm dung dịch bazơ vào muối cromat màu da cam sẽ tạo thành đicromat có màu vàng.
C. Khi thêm dung dịch axit vào muối cromat màu da cam sẽ tạo thành đicromat có màu vàng.
D. Khi thêm dung dịch axit vào muối cromat màu vàng sẽ tạo thành đicromat có màu da cam.
Câu 22: Biết cấu hình của Fe là: 1s22s22p63s23p63d64s2. Vị trí của Fe trong bảng tuần hoàn là
A. Ô: 20, chu kì: 3, nhóm VIIIA.
B. Ô: 26, chu kì: 4, nhóm VIIIB.
C. Ô: 26, chu kì: 4, nhóm IIA.
D. Ô: 25, chu kì: 3, nhóm IIB.
Câu 23: Khi đốt Fe với bột lưu huỳnh trong điều kiện không có oxi thu được chất X. Hãy cho biết công thức của X.
A. FeS.
B. FeS2.
C. Fe2S3.
D. Cả hỗn hợp 3 chất.
Câu 24: Hỗn hợp X gồm Al, Fe2O3, Cu có số mol bằng nhau. Hỗn hợp X tan hoàn toàn trong
A. AgNO3 dư.
B. NaOH dư.
C. HCl dư.
D. NH3 dư.
Câu 25: Khử hoàn toàn 16 gam bột oxit sắt bằng khí CO ở nhiệt độ cao. Sau phản ứng khối lượng khí thu được tăng thêm so với khối lượng khí ban đầu 4,8 gam. Công thức của oxit sắt là
A. Fe2O3.
B. FeO.
C. FeO2.
D. Fe3O4.
Câu 26: Thứ tự một số cặp oxi hoá - khử trong dãy điện hoá như sau: Mg2+/Mg; Fe2+/Fe; Cu2+/Cu; Fe3+/Fe2+; Ag+/Ag. Dãy chỉ gồm các chất, ion tác dụng được với ion Fe3+ trong dung dịch là
A. Mg, Fe2+, Ag.
B. Fe, Cu, Ag+.
C. Mg, Cu, Cu2+.
D. Mg, Fe, Cu.
Câu 27: Phản ứng nào sau đây đã được viết không đúng?
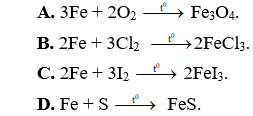
Câu 28: Xét phương trình phản ứng:
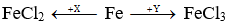
A. HCl, FeCl3.
B. AgNO3 dư, Cl2.
C. FeCl3 , Cl2.
D. Cl2 , FeCl3.
Câu 29: Hoà tan hoàn toàn 1,84 gam hỗn hợp Fe và Mg trong lượng dư dung dịch HNO3 thấy thoát ra 0,04 mol khí NO duy nhất(đktc). Số mol Fe và Mg trong hỗn hợp lần lượt là
A. 0,03 mol và 0,03 mol.
B. 0,01 mol và 0,03 mol.
C. 0,03 mol và 0,02 mol.
D. 0,02 mol và 0,03 mol.
Câu 30: Tìm câu phát biểu đúng:
A. Fe chỉ có tính khử, hợp chất sắt (III) chỉ có tính oxi hoá, hợp chất sắt (II) chỉ có tính khử.
B. Fe chỉ có tính khử, hợp chất sắt (III) chỉ có tính oxi hoá, hợp chất sắt (II) chỉ có tính khử và tính oxi hoá.
C. Fe chỉ có tính khử, hợp chất sắt (III) chỉ có tính oxi hoá, hợp chất sắt (II) chỉ có tính oxi hoá .
D. Fe chỉ có tính oxi hoá, hợp chất sắt (III) chỉ có tính oxi hoá, hợp chất sắt (II) chỉ có tính khử.
Đáp án & Thang điểm
Câu 1. A
Crom bị thụ động hóa trong H2SO4 đặc, nguội.
Câu 2. D
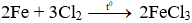
Do Cl2 thiếu nên Fe dư, hỗn hợp sau phản ứng gồm: FeCl3 và Fe dư.
Câu 3. C
Dùng Ba(OH)2 dư
+ Có kết tủa xanh → CuCl2
Cu2+ + 2OH- → Cu(OH)2 (↓ xanh)
+ Có kết tủa nâu đỏ → FeCl3
Fe3+ + 3OH- → Fe(OH)3 (↓ nâu đỏ)
+ Có kết tủa trắng hơi xanh, để trong không khí chuyển dần sang màu nâu đỏ.
Fe2+ + 2OH- → Fe(OH)2 (↓ trắng xanh)
4Fe(OH)2 + O2 + 2H2O → 4 Fe(OH)3 (↓ nâu đỏ)
+ Có kết tủa màu lục xám xuất hiện, sau đó kết tủa tan dần trong Ba(OH)2 dư.
Cr3+ + 3OH- → Cr(OH)3 (↓ lục xám)
Cr(OH)3↓ + OH- → CrO2- + 2H2O
Câu 4. D
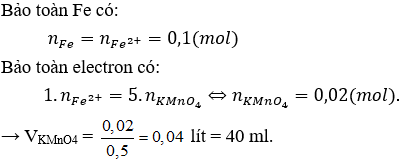
Câu 5. B
Bảo toàn electron có: 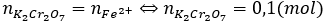
Khối lượng KMnO4 là: m = 0,1.294 = 29,4 (gam)
Câu 6. B
Gọi số mol Fe2O3, Cr2O3 và Al2O3 trong X lần lượt là x, y và z (mol)
mx = 41,4 gam → 160x + 152y + 102z = 41,4 (1)
Cho X tác dụng với NaOH đặc dư, có Fe2O3 không phản ứng
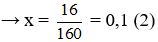
Khử X bằng Al có Fe2O3 và Cr2O3 phản ứng:
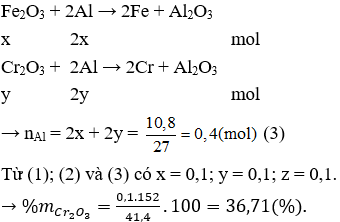
Câu 7. C
Bảo toàn electron có: 3.nCr = 3.nkhí → nkhí = nCr = 0,1 (mol)
→ Vkhí = 0,1.22,4 = 2,24 lít.
Câu 8. B
Lượng Fe hao hụt trong sản xuất là 1% nên H = 99%.
Khối lượng sắt có trong 800 tấn gang chứa 95% sắt là : 800.95% = 760 (tấn).
Khối lượng sắt thực tế cần phải có là : 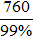
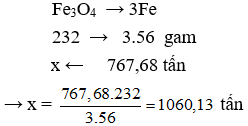
Khối lượng quặng manhetit cần dùng là : 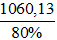
Câu 9. B
FeO; Fe2O3: oxit bazơ
Fe(OH)2, Fe(OH)3: bazơ.
Câu 10. C
Gọi số mol Al, Fe và Cr trong hỗn hợp lần lượt là x, y và z (mol)
Cho hỗn hợp kim loại vào NaOH dư chỉ có Al phản ứng
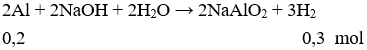
→ x = 0,2 (mol) (1)
Chất rắn sau phản ứng gồm Fe và Cr
→ 56y + 52z = 10,8 (2)
Cho Fe và Cr tác dụng với HCl có phản ứng:
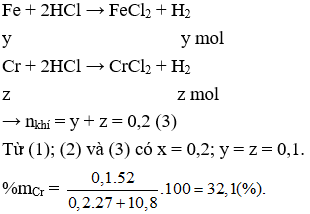
Câu 11. B
Cu + Cu(NO3)2 → không phản ứng
Cu + 2Fe(NO3)3 → Cu(NO3)2 + 2Fe(NO3)2
Cu + 2AgNO3 → Cu(NO3)2 + 2Ag.
Câu 12. C
Do bột sắt dư, nên sản phẩm thu được là Fe2+ và Ag.
Câu 13. C
Ta có các phương trình:
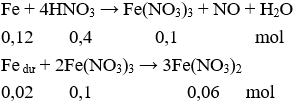
Dung dịch X có: Fe(NO3)2: 0,06 mol và Fe(NO3)3 0,06 mol
Cho Cu vào X có phản ứng:
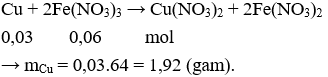
Câu 14. B
Sắt dẻo.
Câu 15. B
Crom có số oxi hóa từ +1 đến +6 trong đó số oxi hóa đặc trưng là +2; +3; +6.
Câu 16. B
Ta có: nO (oxit) = naxit = 0,05 (mol)
mKL (oxit) = moxit – mO (oxit) = 2,81 – 0,05.16 = 2,01 (gam)
mmuối = mKL + mgốc axit = 2,01 + 0,05.96 = 6,81 (gam).
Câu 17. D
A, B sai do CrO3 là oxit axit không tác dụng với HCl.
C sai do Cr(OH)2 không có tính lưỡng tính, không tác dụng được với NaOH.
Câu 18. D
Hemantit nâu: Fe2O3.nH2O.
Câu 19. B
Fe3O4 + 4H2SO4 loãng → Fe2(SO4)3 + FeSO4 + 4H2O.
Câu 20. A
FeSO3 + H2SO4 loãng → FeSO4 + SO2 + H2O.
Câu 21. D
2CrO42- (vàng) + 2H+ ⇌ Cr2O72- (da cam) + H2O
Câu 22. B
Fe ở ô 26 do (z = 26); chu kỳ 4 (do có 4 lớp electron); nhóm VIIIB (do có 8 electron hóa trị, nguyên tố d).
Câu 23. A
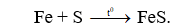
Câu 24. C
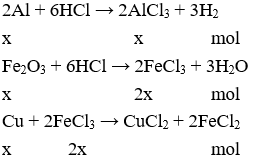
Câu 25. A
Khối lượng khí tăng lên so với ban đầu chính là khối lượng O trong oxit.
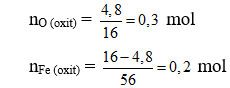
Đặt công thức oxit sắt là FexOy. Ta có:
x : y = nFe : nO = 0,2 : 0,3 = 2 : 3.
Vậy oxit sắt là: Fe2O3.
Câu 26. D
Câu 27. C
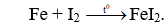
Câu 28. C
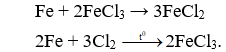
Câu 29. D
Gọi số mol Fe và Mg trong hỗn hợp lần lượt là x và y (mol)
nhh = 1,04 gam → 56x + 24y = 1,84 (1)
Bảo toàn electron có: 3.nFe + 2.nMg = 3.nNO → 3x + 2y = 0,12 (2)
Từ (1) và (2) có: x = 0,02 và y = 0,03.
Câu 30. B
Sở Giáo dục và Đào tạo .....
Đề thi Giữa học kì 1
Môn: Hóa Học 12
Thời gian làm bài: 45 phút
(Đề 3)
Cho nguyên tử khối: H = 1, N = 14, O = 16, S = 32, Mg = 24, Fe = 64, Fe = 56, Cl = 35,5, Cr = 52, Al = 27, Na = 23, K = 39, Zn = 65, Mn = 55.
Câu 1: Cho 1 lá sắt vào dung dịch chứa 1 trong những muối sau: ZnCl2 (1); CuSO4 (2); Pb(NO3)2 (3); NaNO3 (4); MgCl2 (5); AgNO3 (6). Số trường hợp xảy ra phản ứng là
A. 5.
B. 3.
C. 2.
D. 4.
Câu 2: Không thể điều chế trực tiếp FeCl3 trong phòng thí nghiệm bằng cách thực hiện phản ứng nào sau đây ?
A. Fe2O3 + HCl.
B. FeCl2 + Cl2.
C. Fe + HCl.
D. Fe + Cl2.
Câu 3: Cho sơ đồ chuyển hoá: 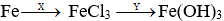
A. HCl, Al(OH)3.
B. NaCl, Cu(OH)2.
C. Cl2, NaOH.
D. HCl, NaOH.
Câu 4: Hoà tan hoàn toàn một oxit sắt vào dung dịch HNO3 đặc, nóng thu được dung dịch X và không thấy có khí thoát ra. Oxit đó là
A. Fe2O3.
B. FeO.
C. Fe3O4.
D. A và C.
Câu 5: Cho dãy các chất: Fe, FeO, Fe3O4, Fe(OH)2, Fe(OH)3. Số chất trong dãy khi tác dụng với dung dịch HNO3 loãng sinh ra sản phẩm khí (chứa nitơ) là
A. 4.
B. 2.
C. 3.
D. 5.
Câu 6: Khi hòa tan Fe vào dung dịch HNO3 loãng sinh ra NO thì chất bị khử là
A. Fe.
B. Ion NO3-.
C. Ion H+.
D. H2O.
Câu 7: Quặng sắt nào sau đây có hàm lượng sắt lớn nhất ?
A. Manhetit.
B. Hematit.
C. Pirit sắt.
D. Xiđerit.
Câu 8: Cho các chất sau: Cr, CrO, Cr(OH)2, CrO3, Cr(OH)3. Có bao nhiêu chất thể hiện tính chất lưỡng tính ?
A. 3.
B. 1.
C. 4.
D. 2.
Câu 9: Cho chuỗi phản ứng : MCl2 → M(OH)2 → M(OH)3 → Na[M(OH)4] .Vậy M là kim loại nào sau đây:
A. Cr.
B. Zn.
C. Fe.
D. Al.
Câu 10: Thêm từ từ dung dịch NaOH đến dư vào dung dịch Na2Cr2O7 được dd X, ta quan sát được sự chuyển màu của dung dịch như sau:
A. Từ vàng sang da cam.
B. Từ da cam sang vàng.
C. Từ không màu sang da cam.
D. Từ không màu sang vàng.
Câu 11: Để phân biệt dung dịch CrCl3 và dung dịch FeCl2 người ta dùng lượng dư dung dịch
A. Na2SO4.
B. KHSO4.
C. KOH.
D. NaNO3.
Câu 12: Thêm dung dịch NaOH dư vào dung dịch muối CrCl3, nếu thêm tiếp dung dịch brom thì thu được sản phẩm có chứa crom là
A. CrO2.
B. Cr(OH)3.
C. Na2Cr2O7.
D. Na2CrO4.
Câu 13: Cho Cu tác dụng với:
(1) dd HCl + NaNO3;
(2) dd KNO3;
(3) khí clo;
(4) dd AgNO3;
(5) dd FeCl2;
(6) dd KOH;
(7) dd FeCl3;
(8) dd HNO3;
(9)(H2SO4 (l) + O2) . Cu tác dụng được với bao nhiêu chất?
A. 6. B. 5. C. 3. D. 4.
Câu 14: Hòa tan hoàn toàn x mol Fe vào dung dịch chứa y mol FeCl3 và z mol HCl, thu được dung dịch chỉ chứa một chất tan duy nhất. Biểu thức liên hệ giữa x, y và z là
A. 2x = y + 2z.
B. x = y – 2z.
C. 2x = y + z.
D. y = 2x.
Câu 15: Cho hỗn hợp Fe và Cu vào dung dịch FeCl3 sau khi phản ứng xảy ra hoàn toàn người ta thu được dung dịch X và chất rắn Y. Cho Y tác dụng với HCl không thấy khí thoát ra. Như vậy trong dung dịch X có chứa:
A. FeCl2, FeCl3, H2O.
B. CuCl2, FeCl2, H2O.
C. CuCl2, H2O, FeCl3.
D. FeCl3, H2O.
Câu 16: Khối lượng bột nhôm cần dùng để thu được 65 gam crom từ Cr2O3 bằng phản ứng nhiệt nhôm (giả sử hiệu suất phản ứng là 100%) là
A. 40,5 gam.
B. 67,5 gam.
C. 33,75 gam.
D. 54,0 gam.
Câu 17: Cho m gam bột crom phản ứng hoàn toàn với dung dịch HCl (nóng, dư) thu được V lít khí H2 (đktc). Mặt khác, cũng m gam bột crom trên phản ứng hoàn toàn với khí O2 (dư), thu được 45,6 gam oxit duy nhất. Giá trị của V là
A. 6,72.
B. 20,16
C. 13,44.
D. 3,36.
Câu 18: Khử 16g Fe2O3 bằng CO ở nhiệt độ cao thu được một hỗn hợp rắn X gồm Fe2O3, Fe3O4, FeO, Fe. Cho X tác dụng hết với H2SO4 đặc, nóng, dư thu được dung dịch Y. sau khi cô cạn dung dịch Y, khối lượng muối khan thu được là
A. 18g.
B. 30g.
C. 40g.
D. 25g.
Câu 19: Khử hoàn toàn 17,6 gam hỗn hợp X gồm Fe, FeO, Fe2O3 cần 1,792 lít CO (ở đktc). Khối lượng sắt thu được là
A. 16,0 gam.
B. 8,0 gam.
C. 5,6 gam.
D. 16,32 gam.
Câu 20: Hỗn hợp A gồm Fe3O4, FeO, Fe2O3 mỗi oxit đều có 0,6 mol. Thể tích dung dịch HCl 1M cần để hoàn tan hoàn toàn hỗn hợp A là
A. 9,62 lit.
B. 8 lit.
C. 14,4 lit.
D. 9,6 lit.
Câu 21: Cho 28 gam hỗn hợp gồm MgO, Fe2O3, CuO tác dụng hoàn toàn và vừa đủ với 200ml dung dịch H2SO4 2,5M. Khối lượng muối thu được là
A. 67,0 gam.
B. 86,8 gam.
C. 43,4 gam.
D. 68,0 gam.
Câu 22: Hòa tan hoàn toàn hỗn hợp gồm 0,1 mol Fe2O3 và 0,2 mol FeO vào dd HCl dư thu được dd A. Cho NaOH dư vào dd A thu được kết tủa B. Lọc lấy kết tủa B rồi đem nung trong không khí đến khối lượng không đổi được m(g) chất rắn, m có giá trị là
A. 16g.
B. 32g.
C. 48g.
D. 52g.
Câu 23: Hòa tan 2,24 gam Fe bằng 300 ml dung dịch HCl 0,4 M , thu được dung dịch X và khí H2. Cho dung dịch AgNO3 dư vào X, thu được khí NO (sản phẩm khử duy nhất của 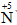
A. 18,3.
B. 8,61.
C. 7,36.
D. 9,15.
Câu 24. Cho phương trình phản ứng : a X + b Y(NO3)a → a X(NO3)b + b Y. Biết dung dịch Y(NO3)a có màu xanh. Hai kim loại X, Y lần lượt là
A. Cu, Fe.
B. Cu, Ag.
C. Zn, Cu.
D. Ag, Cu.
Câu 25: Dung dịch nào dưới đây không hoà tan được Cu?
A. Dung dịch FeCl3.
B. Dung dịch H2SO4 loãng.
C. Dung dịch hỗn hợp NaNO3 + HCl.
D. Dung dịch HNO3 đặc, nguội.
Câu 26: Phương trình hoá học nào sau đây thể hiện cách điều chế Cu theo phương pháp thuỷ luyện ?
A. Zn + CuSO4 → Cu + ZnSO4.
B. H2 + CuO → Cu + H2O.
C. CuCl2 → Cu + Cl2.
D. 2CuSO4 + 2H2O → 2Cu + 2H2SO4 + O2.
Câu 27: Cho 150ml dd FeCl2 1M vào dung dịch AgNO3 dư, lắc kĩ cho phản ứng xảy ra hoàn toàn thu được m gam chất rắn. Giá trị của m là
A. 43,05.
B. 59,25.
C. 16,20.
D. 57,4.
Câu 28: Hoà tan 12,8 gam Cu bằng axit H2SO4 đặc, nóng (dư), sinh ra V lít khí SO2 (sản phẩm khử duy nhất ở đktc). Giá trị của V là
A. 2,24.
B. 3,36.
C. 4,48.
D. 6,72.
Câu 29: Cho 28,8g Cu vào 500ml dd NaNO3 1M sau đó thêm vào 500ml dd HCl 2M thấy có khí NO bay ra, thể tích NO (đkc) là
A. 2,24 l.
B. 4,48 l.
C. 6,72 l.
D. 5,6 l.
Câu 30: Hòa tan hết 8,65g hỗn hợp kim loại gồm Mg, Al, Zn, Fe bằng dd H2SO4 loãng, dư thu được V lít khí ở đktc và 37,45g muối sunfat khan. Giá trị của V là
A. 1,344.
B. 1,008.
C. 1,12.
D. 6,72.
Đáp án & Thang điểm
Câu 1. B
Fe + ZnCl2 → không phản ứng.
Fe + CuSO4 → FeSO4 + Cu
Fe + Pb(NO3)2 → Fe(NO3)2 + Pb
Fe + NaNO3 → không phản ứng
Fe + MgCl2 → không phản ứng
Fe + 2AgNO3 → Fe(NO3)2 + 2Ag
Câu 2. C
Fe + 2HCl → FeCl2 + H2
Câu 3. C
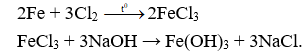
Câu 4. A
Do trong Fe2O3, sắt đã đạt số oxi hóa cao nhất.
Fe2O3 + 6HNO3 → 2Fe(NO3)3 + 3H2O
Câu 5. A
Các hợp chất của Fe, trong đó Fe chưa đạt số oxi hóa cao nhất khi tác dụng với HNO3 loãng sinh ra sản phẩm khí (chứa nitơ).
→ Các chất thỏa mãn yêu cầu bài toán: Fe, FeO, Fe3O4, Fe(OH)2.
Câu 6. B
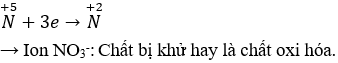
Câu 7. A
Manhetit: Fe3O4 có hàm lượng sắt lớn nhất.
Câu 8. B
Chất có tính lưỡng tính là: Cr(OH)3.
Câu 9. A
CrCl2 + 2NaOH → Cr(OH)2 ↓ + 2NaCl
4Cr(OH)2 + O2 + 2H2O → 4Cr(OH)3
Cr(OH)3 + NaOH → Na[Cr(OH)4]
Câu 10. B
Cr2O72- (da cam) + OH- ⇌ 2CrO42- (vàng) + H+
Câu 11. C
Dùng NaOH làm thuốc thử
+ Xuất hiện kết tủa trắng xanh, trong không khí chuyển dần sang màu nâu đỏ → FeCl2
FeCl2 + 2KOH → Fe(OH)2 ↓ trắng xanh + 2KCl
4Fe(OH)2 + O2 + 2H2O → 4Fe(OH)3 ↓ nâu đỏ
+ Xuất hiến kết tủa lục xám, sau đó KOH dư, kết tủa tan dần → CrCl3
CrCl3 + 3KOH → Cr(OH)3 ↓lục xám + 3KCl
Cr(OH)3 + KOH → K[Cr(OH)4]
Câu 12. D
CrCl3 + 3NaOH → Cr(OH)3 ↓lục xám + 3NaCl
Cr(OH)3 + NaOH → NaCrO2 + 2H2O
2NaCrO2 + 3Br2 + 8NaOH → 2Na2CrO4 + 6NaBr + 4H2O
Câu 13. A
Các trường hợp phản ứng với Cu là: dd HCl + NaNO3 (1); khí clo (3); dd AgNO3 (4); dd FeCl3(7); dd HNO3(8); (H2SO4(l) + O2) (9).
Câu 14. C
Theo bài ra, Fe hết, chất tan duy nhất thu được là FeCl2.
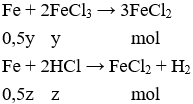
→ x = 0,5 y + 0,5 z hay 2x = y + z.
Câu 15. B
Theo bài ra, kết thúc phản ứng còn Cu dư. Vậy X không thể chứa FeCl3
→ loại A, C và D
Câu 16. C
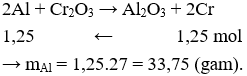
Câu 17. C
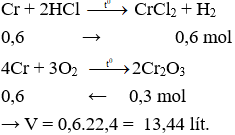
Câu 18. C
Cho X tác dụng hết với lượng dư H2SO4 đặc, nóng nên muối thu được chỉ có: Fe2(SO4)3
Bảo toàn Fe có:
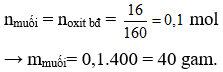
Câu 19. D
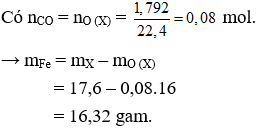
Câu 20. D
Ta có: nO(A) = 0,6.4 + 0,6 + 0,6.3 = 4,8 mol
nHCl = 2.nO = 2.4,8 = 9,6 mol
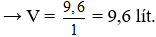
Câu 21. D
Ta có: nO (oxit) = naxit = 0,5 mol
→ mmuối = mKL + mgốc axit = (28 – 0,5.16) + 0,5.96 = 68 gam.
Câu 22. B
Theo bài ra, khi nung chất rắn B ngoài không khí thu được chất rắn là Fe2O3.
Bảo toàn Fe có: 0,1 + 0,1 = 0,2 mol
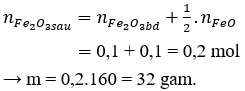
Câu 23. A
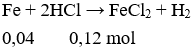
Dung dịch X gồm: HCl dư = 0,04 mol và FeCl2: 0,04 mol
Cho AgNO3 dư vào X có phản ứng:
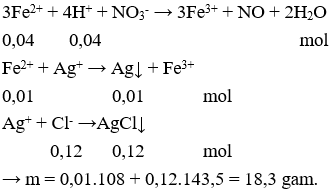
Câu 24. C
Dung dịch Y(NO3)a có màu xanh → Y là Cu
Theo phương trình hóa học có tính khử của X > Y.
Vậy X và Y lần lượt là Zn và Cu.
Câu 25. B
Cu không tác dụng với H2SO4 loãng.
Câu 26. A
Phương pháp thủy luyện: dùng kim loại mạnh đẩy kim loại yếu ra khỏi dung dịch muối.
Câu 27. B
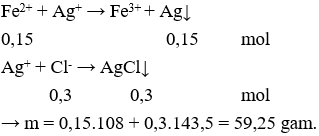
Câu 28. C
Bảo toàn electron có:
2.nCu = 2.nkhí → nkhí = nCu = 0,2 mol
→ V = 0,2.22,4 = 4,48 lít.
Câu 29. D
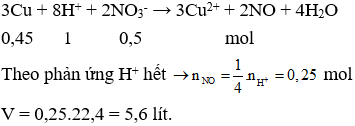
Câu 30. D
Ta có: mmuối = mKL + mgốc axit → mgốc axit = 37,45 – 8,65 = 28,8 gam.
nkhí = naxit = ngốc axit = mol
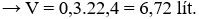
Sở Giáo dục và Đào tạo .....
Đề thi Giữa học kì 1
Môn: Hóa Học 12
Thời gian làm bài: 45 phút
(Đề 4)
Cho nguyên tử khối: H = 1, N = 14, O = 16, S = 32, Mg = 24, Fe = 64, Fe = 56, Cl = 35,5, Cr = 52, Al = 27, Na = 23, K = 39, Zn = 65, Mn = 55.
Câu 1: Công thức hóa học của sắt (III) hiđroxit là
A. Fe(OH)3.
B. Fe(OH)2.
C. Fe2O3.
D. FeO.
Câu 2: Hai chất nào sau đây đều là hiđroxit lưỡng tính?
A. Fe(OH)3, Al(OH)3.
B. Cr(OH)3, Al(OH)3.
C. NaOH, Al(OH)3 .
D. Cr(OH)3, Fe(OH)3.
Câu 3: Để khử hoàn toàn 8,0g bột Fe2O3 bằng bột Al (ở nhiệt độ cao, trong điều kiện không có không khí) thì khối lượng bột nhôm cần dùng là
A. 5,4g.
B. 8,1g.
C. 1,35g.
D. 2,7g.
Câu 4: Hòa tan hoàn toàn 5,6 gam Fe bằng dung dịch HNO3 (loãng, dư), thu được V lít khí NO (sản phẩm khử duy nhất, ở đktc). Giá trị của V là
A. 3,36.
B. 2,24.
C. 4,48.
D. 1,12.
Câu 5: Kim loại Fe phản ứng được với dung dịch
A. KNO3.
B. CuSO4.
C. Na2CO3.
D. CaCl2.
Câu 6: Cho dãy kim loại: Na, Al, Fe, Cu, Cr, Ag. Số kim loại trong dãy phản ứng được với dung dịch HCl là
A. 2.
B. 3.
C. 4.
D. 5.
Câu 7: Kim loại Fe phản ứng được với dung dịch nào sau đây tạo thành muối sắt (III) ?
A. Dung dịch CuSO4.
B. Dung dịch HNO3 loãng dư.
C. Dung dịch H2SO4 loãng.
D. Dung dịch HCl.
Câu 8: Số oxi hóa đặc trưng của crom trong hợp chất là
A. +2, +4, +6.
B. +2,+3,+6.
C. +3, +4, +6.
D. +2, +3, +4.
Câu 9: Trong bảng tuần hoàn các nguyên tố hóa học, nguyên tố 26Fe thuộc nhóm
A. VIB.
B. IA.
C. IIA.
D. VIIIB.
Câu 10: Nhiệt phân hoàn toàn Fe(OH)3 ở nhiệt độ cao thu được chất rắn là
A. Fe3O4.
B. Fe.
C. FeO.
D. Fe2O3.
Câu 11: Cho 10,0 gam hỗn hợp X gồm Fe và Cu phản ứng với dung dịch HCl loãng (dư), đến khi phản ứng xảy ra hoàn toàn thu được 3,36 lít khí H2 (đktc). Khối lượng của Cu trong 10,0 gam hỗn hợp X là
A. 5,6g.
B. 8,4g.
C. 2,8g.
D. 1,6g.
Câu 12: Trường hợp nào dưới đây không có sự phù hợp giữa tên quặng sắt và công thức hợp chất sắt chính có trong quặng?
A. Hematit nâu chứa Fe3O4.
B. Manhetit chứa Fe3O4.
C. Xiđêrit chứa FeCO3.
D. Pirit chứa FeS2.
Câu 13: Để khử hoàn toàn 16,6 gam hỗn hợp gồm Fe, FeO, Fe3O4, Fe2O3 đến Fe cần dùng vừa đủ 2,24 lít khí CO (đktc). Khối lượng Fe thu được là
A. 15g.
B. 16g.
C. 17g.
D. 18g.
Câu 14: Ngâm một đinh sắt trong dung dịch CuSO4, sau một thời gian lấy đinh sắt ra, sấy khô, đem cân thấy khối lượng tăng 1g. Khối lượng Fe tham gia phản ứng là
A. 7g.
B. 8g.
C. 5,6g.
D. 8,4g.
Câu 15: Cho dãy các chất: FeO, Fe, Cr(OH)3, Cr2O3. Số chất trong dãy phản ứng được với dung dịch HCl là
A. 1.
B. 2.
C. 3.
D. 4.
Câu 16: Cho 5,6g sắt tác dụng hết với khí Cl2 dư thu được m(g) muối. Giá trị của m là
A. 10,2g.
B. 7,9g.
C. 16,25g.
D. 14,6g.
Câu 17: Khử hoàn toàn 16g Fe2O3 bằng khí CO ở nhiệt độ cao, khí sinh ra sau phản ứng được dẫn vào dung dịch Ca(OH)2 dư. Khối lượng kết tủa thu được là
A. 10g.
B. 15g.
C. 20g.
D. 30g.
Câu 18: Hỗn hợp A gồm FeO, Fe2O3, Fe3O4. Trong hỗn hợp A, mỗi oxit đều có 0,1 mol. Khối lượng hỗn hợp A là
A. 23,2g.
B. 46,4g.
C. 232g.
D. 464g.
Câu 19:Biết Cr (z = 24) cấu hình electron của Cr3+ là
A. [Ar]3d54s1
B. [Ar]3d3
C. [Ar]3d44s2
D. [Ar]3d64s2
Câu 20: Phát biểu nào sau đây là sai?
A. Cr(OH)3 tan trong dung dịch NaOH.
B. Trong môi trường axit, Zn khử Cr3+ thành Cr.
C. Photpho bốc cháy khi tiếp xúc với CrO3.
D. Trong môi trường kiềm, Br2 oxi hóa CrO2- thành CrO42- .
Câu 21: Khi thêm axit HCl và muối K2CrO4 thì dung dịch tạo thành có màu
A. Màu vàng.
B. Màu da cam.
C. Màu lục.
D. Không màu.
Câu 22: Nhóm kim loại nào không tác dụng với HNO3 đặc nguội ?
A. Al, Fe, Cu.
B. Al, Fe, Cr.
C. Al, Cr, Zn.
D. Fe, Cu, Zn.
Câu 23: Cho 5,6 gam Fe tác dụng hết với 400ml dd HNO3 1M ta thu được dd X và khí NO (sản phẩm khử duy nhất) khi cô cạn X, khối lượng Fe(NO3)3 thu được là
A. 26,44g.
B. 24,2g.
C. 4,48g.
D. 21,6g.
Câu 24: Khối lượng K2Cr2O7 cần dùng để tác dụng đủ với 0,6 mol FeSO4 trong dung dịch (có H2SO4 làm môi trường) là
A. 26,4g.
B. 29,4g.
C. 27,4g.
D. 58,8g.
Câu 25: Cho phương trình: Fe2+ + Ag+ → Fe3+ + Ag. Phát biểu sai về phản ứng trên là ?
A. Ag+ oxi hóa được Fe2+.
B. Tính khử của Ag+ mạnh hơn Fe3+.
C. Fe2+ khử được Ag+.
D. Tính khử Fe2+ mạnh hơn Ag.
Câu 26: Cho phản ứng sau:
2NaCrO2 + 3Br2 + 8NaOH → 2Na2CrO4 + 6NaBr + 4H2O
Tổng hệ số của các chất tham gia phản ứng trong phương trình trên là:
A. 13.
B. 20.
C. 25.
D. 27.
Câu 27: Hòa tan hoàn toàn 14,7g hỗn hợp gồm Al, Cu, Fe (có số mol bằng nhau) trong dung dịch HNO3 dư thu được dung dịch Y và 1,344 lít (đktc) hỗn hợp khí gồm NO và N2O. Cô cạn cẩn thận dung dịch Y được 69,37g muối khan. Số mol HNO3 đã tham gia phản ứng là
A. 1,00935.
B. 0,2639.
C. 0,32265.
D. 0,9745.
Câu 28: Cho các chất sau: (1) Cl2, (2) H2SO4 loãng, (3) HNO3 loãng, (4) H2SO4 đặc, nguội. Khi cho Fe tác dụng với chất nào trong số các chất trên đều tạo được hợp chất trong đó sắt (III) ?
A. (1) , (2).
B. (1), (3) , (4).
C. (1), (2) , (3).
D. (1), (3).
Câu 29: Dung dịch muối FeCl3 không tác dụng với kim loại nào dưới đây ?
A. Zn.
B. Fe.
C. Cu.
D. Ag.
Câu 30: Cho 13,6g hỗn hợp Fe và Cr tác dụng hết với dung dịch HCl nóng thấy có 5,6 lít khí H2 thoát ra (đktc). Đem cô cạn dung dịch sau phản ứng thu được m gam muối khan. Giá trị m là
A. 31,35.
B. 31,75.
C. 22,48.
D. 22,45.
Đáp án & Thang điểm
Câu 1. A
Sắt (III) hiđroxit: Fe(OH)3.
Câu 2. B
Cr(OH)3, Al(OH)3 là các hiđroxit lưỡng tính.
Câu 3. D
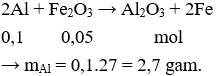
Câu 4. B
Bảo toàn electron có: nkhí = nFe = 0,1 mol → V = 0,1.22,4 = 2,24 lít.
Câu 5. B
Fe + CuSO4 → FeSO4 + Cu.
Câu 6. C
Kim loại phản ứng được với HCl là những kim loại đứng trước H trong dãy hoạt động hóa học.
→ Những kim loại phản ứng là: Na, Al, Fe, Cr.
Câu 7. B
Fe + 4HNO3 → Fe(NO3)3 + NO + 2H2O.
Câu 8. B
Crom có các số oxi hóa từ +1 đến +6. Trong đó số oxi hóa phổ biến là: +2,+3,+6.
Câu 9. D
Fe (z = 26): [Ar]3d63s2
→ Fe thuộc nhóm VIIIB (8 electron hóa trị, nguyên tố d).
Câu 10. D
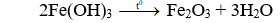
Câu 11. D
Cho Fe và Cu phản ứng với HCl loãng chỉ có Fe phản ứng
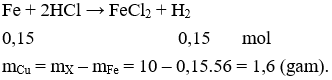
Câu 12. A
Hemantit nâu chứa Fe2O3.nH2O.
Câu 13. A
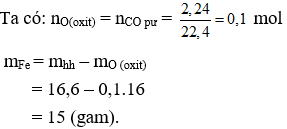
Câu 14. A
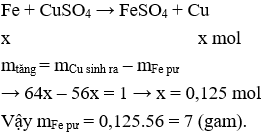
Câu 15. D
FeO + 2HCl → FeCl2 + H2O
Fe + 2HCl → FeCl2 + H2
Cr(OH)3 + 3HCl → CrCl3 + 3H2O
Cr2O3 + 6HCl → 2CrCl3 + 3H2O.
Câu 16. C
Muối là FeCl3
Bảo toàn Fe có nmuối = nFe = 0,1 mol
mmuối = 0,1.162,5 = 16,25 gam.
Câu 17. D
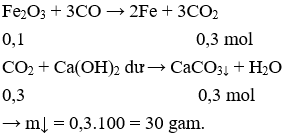
Câu 18. B
mA = 0,1 (72 + 160 + 232) = 46,4 gam.
Câu 19. B
Cr (Z = 24): [Ar]3d54s1 → Cr3+: B. [Ar]3d3.
Câu 20. B
Trong môi trường axit: 2Cr3+ + Zn → 2Cr2+ + Zn2+.
Câu 21. B
2CrO42- (vàng) + 2H+ Cr2O72- (da cam) + H2O
Câu 22. A
Al, Fe, Cr bị thụ động hóa trong HNO3 đặc, nguội.
Câu 23. B
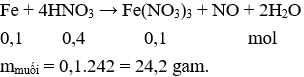
Câu 24. B
Áp dụng định luật bảo toàn electron có: nK2Cr2O7 = nFeSO4 → nK2Cr2O7 = 0,1 mol
Khối lượng K2Cr2O7 là: m = 0,1.294 = 29,4 gam.
Câu 25. B
Tính oxi hóa của Ag+ mạnh hơn Fe3+.
Câu 26. C
Tổng hệ số = 2 + 3 + 8 + 2 + 6 + 4 = 25.
Câu 27. A
Gọi số mol Al, Cu, Fe bằng nhau và bằng x mol
→ 27x + 64x + 56x = 14,7 → x = 0,1 (mol)
Do HNO3 dư nên muối trong Y gồm: Al(NO3)3: 0,1 mol; Cu(NO3)2: 0,1 mol; Fe(NO3)3 0,1 mol và NH4NO3 (có thể có) y mol.
mmuối = 69,37 (gam) → 213.0,1 + 188.0,1 + 242.0,1 + 80y = 69,37
→ y = 0,063375 mol
Gọi số mol NO và N2O lần lượt là a và b (mol)
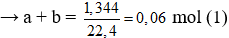
Bảo toàn electron có: 3.nAl + 2nCu + 3.nFe = 3a + 8b + 0,063375.8
→ 3a + 8b = 0,293 (2)
Từ (1) và (2) có a = 0,0374 và b = 0,0226.
Bảo toàn N có:
nAxit = 3.nAl + 2nCu + 3.nFe = 0,0374 + 2.0,0226 + 2. 0,063375 = 1,00935 mol.
Câu 28. D
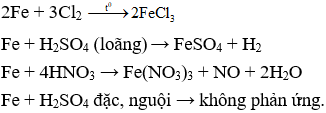
Câu 29. D
Ag + FeCl3 → không phản ứng.
Câu 30. A
Bảo toàn H có: nAxit = 2.nkhí = 0,5 mol
→ mmuối = mKL + mgốc axit = 13,6 + 0,5.35,5 = 31,35 gam.
Xem thêm bộ đề thi Hóa học 12 mới năm 2026 chọn lọc khác:
- [2021] Đề thi khảo sát chất lượng đầu năm Hóa học 12 (3 đề)
- Bộ 20 Đề thi Hóa học 12 Giữa học kì 1 năm 2026 tải nhiều nhất
- Đề thi Hóa học 12 Giữa học kì 1 năm 2026 có ma trận (15 đề)
- Đề thi Hóa học 12 Giữa kì 1 năm 2026 có đáp án (3 đề)
- Đề thi Hóa học 12 Giữa kì 1 năm 2026 có đáp án (3 đề)
- Đề thi Học kì 1 Hóa học 12 năm 2026 có đáp án (3 đề)
- Đề thi Hóa học 12 Học kì 2 trắc nghiệm năm 2026 có đáp án (3 đề)
- Đề thi Hóa học 12 Học kì 2 trắc nghiệm - tự luận năm 2026 có đáp án (5 đề)
Để học tốt lớp 12 các môn học sách mới:
- Giải bài tập Lớp 12 Kết nối tri thức
- Giải bài tập Lớp 12 Chân trời sáng tạo
- Giải bài tập Lớp 12 Cánh diều
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Giáo án lớp 12 (các môn học)
- Giáo án điện tử lớp 12 (các môn học)
- Giáo án Toán 12
- Giáo án Ngữ văn 12
- Giáo án Vật Lí 12
- Giáo án Hóa học 12
- Giáo án Sinh học 12
- Giáo án Địa Lí 12
- Giáo án Lịch Sử 12
- Giáo án Lịch Sử 12 mới
- Giáo án GDCD 12
- Giáo án Kinh tế Pháp luật 12
- Giáo án Tin học 12
- Giáo án Công nghệ 12
- Giáo án GDQP 12
- Đề thi lớp 12 (các môn học)
- Đề thi Ngữ văn 12
- Đề thi Toán 12
- Đề thi Tiếng Anh 12 mới
- Đề thi Tiếng Anh 12
- Đề thi Vật Lí 12
- Đề thi Hóa học 12
- Đề thi Sinh học 12
- Đề thi Địa Lí 12
- Đề thi Lịch Sử 12
- Đề thi Giáo dục Kinh tế Pháp luật 12
- Đề thi Giáo dục quốc phòng 12
- Đề thi Tin học 12
- Đề thi Công nghệ 12




 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

