Chuyên đề Hóa học 9 gồm 20 chuyên đề: Dãy hoạt động hoá học của kim loại; Độ tan - nồng độ dung dịch; Pha trộn dung dịch;
Xác định công thức hoá học; Bài toán về oxit và hỗn hợp oxit; Axit tác dụng với kim loại; ... được biên soạn với đầy đủ các mức độ.
Ý nghĩa:
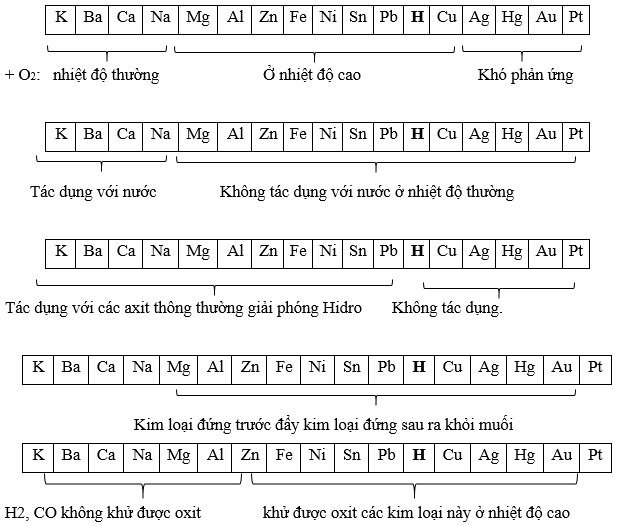
Chú ý:
Các kim loại đứng trước Mg phản ứng với nước ở nhiệt độ thường tạo thành dd Kiềm và giải phóng khí Hidro.
Trừ Au và Pt, các kim loại khác đều có thể tác dụng với HNO3 và H2SO4 đặc nhưng không giải phóng Hidro.
DẠNG 1. PHƯƠNG PHÁP ĐẠI SỐ>
Trong các phương pháp giải các bài toán Hoá học phương pháp đại số cũng thường được sử dụng. Phương pháp này có ưu điểm tiết kiệm được thời gian, khi giải các bài toán tổng hợp, tương đối khó giải bằng các phương pháp khác. Phương pháp đại số được dùng để giải các bài toán Hoá học sau:
a. Giải bài toán lập CTHH bằng phương pháp đại số.
Thí dụ: Đốt cháy một hỗn hợp 300ml hydrocarbon và amonia trong oxi có dư. Sau khi cháy hoàn toàn, thể tích khí thu được là 1250ml. Sau khi làm ngưng tụ hơi nước, thể tích giảm còn 550ml. Sau khi cho tác dụng với dung dịch kiềm còn 250ml trong đó có 100ml nitơ. Thể tích của tất cả các khí đo trong điều kiện như nhau. Lập công thức của hydrocarbon?/p>
Bài giải
Khi đốt cháy hỗn hợp hydrocarbon và amonia trong oxi phản ứng xảy ra theo phương trình sau:
4NH3 + 3O2 -> 2N2 + 6H2O (1)
CxHy + (x + O2 -> xCO2 + H2O (2)
Theo dữ kiện bài toán, sau khi đốt cháy amonia thì tạo thành 100ml nitơ. Theo PTHH (1) sau khi đốt cháy hoàn toàn amonia ta thu được thể tích nitơ nhỏ hơn 2 lần thể tích amonia trong hỗn hợp ban đầu, vậy thể tích amonac khi chưa có phản ứng là 100. 2 = 200ml. Do đó thể tích hiđro cácbon khi chưa có phản ứng là 300 - 200 = 100ml. Sau khi đốt cháy hỗn hợp tạo thành (550 - 250) = 300ml, cacbonnic và (1250 - 550 - 300) = 400ml hơi nước.
Từ đó ta có sơ đồ phản ứng:
CxHy + (x + ) O2 -> xCO2 + H2O
100ml 300ml400ml
Theo định luật Avogađro, có thể thay thế tỉ lệ thể tích các chất khí tham gia và tạo thành trong phản ứng bằng tỉ lệ số phân tử hay số mol của chúng.
CxHy + 5O2 -> 3CO2 + 4 H2O
=> x = 3; y = 8
Vậy CTHH của hydrocacbon là C3H8
b. Giải bài toán tìm thành phần của hỗn hợp bằng phương pháp đại số.
Thí dụ: Hoà tan trong nước 0,325g một hỗn hợp gồm 2 muối sodium chloride và potassium chloride. Thêm vào dung dịch này một dung dịch silver nitrate lấy dư - Kết tủa silver chloride thu được có khối lượng là 0,717g. Tính thành phần phần trăm của mỗi chất trong hỗn hợp.
Bài giải
n NaCl = a(mol) ; n KCl = b(mol)
=> 58,5a + 74,5b = 0,325(1)
NaCl + AgNO3 → AgCl + NaNO3
KCl + AgNO3 → AgCl + KNO3
=> n AgCl = a + b = 0,717/143,5 (2)
Từ (1)(2) suy ra a = 0,003 ; b = 0,002
Suy ra
%m NaCl = 0,003.58,5/0,325.100% = 54%
%m KCl = 100% -54% = 46%
DẠNG 2. PHƯƠNG PHÁP ÁP DỤNG ĐỊNH LUẬT BẢO TOÀN NGUYÊN TỐ VÀ KHỐI LƯỢNG
a/ Nguyên tắc:
Trong phản ứng hoá học, các nguyên tố và khối lượng của chúng được bảo toàn.
Từ đó suy ra:
+ Tổng khối lượng các chất tham gia phản ứng bằng tổng khối lượng các chất tạo thành.
+ Tổng khối lượng các chất trước phản ứng bằng tổng khối lượng các chất sau phản ứng.
b/ Phạm vi áp dụng:
Trong các bài toán xảy ra nhiều phản ứng, lúc này đôi khi không cần thiết phải viết các phương trình phản ứng và chỉ cần lập sơ đồ phản ứng để thấy mối quan hệ tỉ lệ mol giữa các chất cần xác định và những chất mà đề cho.
Bài 1. Cho một luồng khí clo dư tác dụng với 9,2g kim loại sinh ra 23,4g muối kim loại hoá trị I. Hãy xác định kim loại hoá trị I và muối kim loại đó.
Hướng dẫn giải:
Đặt M là KHHH của kim loại hoá trị I.
PTHH:2M+Cl2 →2MCl
2M(g)(2M + 71)g
9,2g23,4g
Ta có:23,4 x 2M=9,2(2M + 71)
Suy ra: M = 23.
Kim loại có khối lượng nguyên tử bằng 23 là Na.
Vậy muối thu được là: NaCl
Bài 2: Hoà tan hoàn toàn 3,22g hỗn hợp X gồm Fe, Mg và Zn bằng một lượng vừa đủ dung dịch H2SO4 loãng, thu được 1,344 lit hiđro (ở đktc) và dung dịch chứa m gam muối. Tính m?
Hướng dẫn giải:
PTHH chung:M+H2SO4 →MSO4+H2
áp dụng định luật BTKL ta có:
mMuối = = 3,22 + 98 * 0,06 - 2 * 0,06 = 8,98g
Bài 3: Có 2 lá sắt khối lượng bằng nhau và bằng 11,2g. Một lá cho tác dụng hết với khí clo, một lá ngâm trong dung dịch HCl dư. Tính khối lượng sắt clorua thu được.
Hướng dẫn giải:
PTHH:
2Fe+3Cl2 →2FeCl3(1)
Fe+2HCl →FeCl2+H2(2)
Theo phương trình (1,2) ta có:
Số mol muối thu được ở hai phản ứng trên bằng nhau nhưng khối lượng mol phân tử của FeCl3 lớn hơn nên khối lượng lớn hơn.
= 127 * 0,2 = 25,4g
= 162,5 * 0,2 = 32,5g
Bài 4: Hoà tan hỗn hợp 2 muối Cacbonnat kim loại hoá trị 2 và 3 bằng dung dịch HCl dư thu được dung dịch A và 0,672 lít khí (đktc).
Hỏi cô cạn dung dịch A thu được bao nhiêu gam muối khác nhau?
Bài giải:
Bài 1: Gọi 2 kim loại hoá trị II và III lần lượt là X và Y ta có phương trình phản ứng:
XCO3 + 2HCl -> XCl2 + CO2 + H2O (1)
Y2(CO3)3 + 6HCl -> 2YCl3 + 3CO2 + 3H2O (2).
Số mol CO2 thoát ra (đktc) ở phương trình 1 và 2 là:
Theo phương trình phản ứng 1 và 2 ta thấy số mol CO2 bằng số mol H2O.
Như vậy khối lượng HCl đã phản ứng là:
mHCl = 0,06 . 36,5 = 2,19 gam
Gọi x là khối lượng muối khan ()
Theo định luật bảo toàn khối lượng ta có:
10 + 2,19 = x + 44 . 0,03 + 18. 0,03
=> x = 10,33 gam
Bài toán 2: Cho 7,8 gam hỗn hợp kimloại Al và Mg tác dụng với HCl thu được 8,96 lít H2 (ở đktc). Hỏi khi cô cạn dung dịch thu được bao nhiêu gam muối khan.
Bài giải:Ta có phương trình phản ứng như sau:
Mg + 2HCl -> MgCl2 + H2↑
2Al + 6HCl -> 2AlCl3 + 3H2↑
Số mol H2 thu được là:
Theo (1, 2) ta thấy số mol HCL gấp 2 lần số mol H2
Nên: Số moltham gia phản ứng là:
n HCl= 2 . 0,4 = 0,8 mol
Số mol (số mol nguyên tử) tạo ra muối cũng chính bằng số mol HCl bằng 0,8 mol. Vậy khối lượng Clo tham gia phản ứng:
mCl = 35,5 . 0,8 = 28,4 gam
Vậy khối lượng muối khan thu được là:
7,8 + 28,4 = 36,2 gam
................................
................................
................................







 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

