Đề kiểm tra 15 phút Hóa 12 Học kì 2 trắc nghiệm - tự luận có đáp án (Bài số 2 - 3 đề)
Dưới đây là danh sách Đề kiểm tra 15 phút Hóa 12 Học kì 2 trắc nghiệm - tự luận có đáp án (Bài số 2 - 3 đề). Hi vọng bộ đề thi này sẽ giúp bạn ôn luyện để đạt điểm cao trong bài thi Hóa học 12.
Bộ Đề thi 15 phút Hóa học 12
Trắc nghiệm + Tự luận
- Đề kiểm tra 15 phút Hóa 12 Học kì 2 có đáp án (Trắc nghiệm - Tự luận - Bài số 2 - Đề 1)
- Đề kiểm tra 15 phút Hóa 12 Học kì 2 có đáp án (Trắc nghiệm - Tự luận - Bài số 2 - Đề 2)
- Đề kiểm tra 15 phút Hóa 12 Học kì 2 có đáp án (Trắc nghiệm - Tự luận - Bài số 2 - Đề 3)
- Đề kiểm tra 15 phút Hóa 12 Học kì 2 có đáp án (Trắc nghiệm - Tự luận - Bài số 2 - Đề 4)
Sở Giáo dục và Đào tạo .....
Đề kiểm tra 15 phút học kì 2
Môn: Hóa Học 12
Thời gian làm bài: 15 phút
(Đề 1)
Cho nguyên tử khối của các nguyên tố: O = 16, H = 1, Na = 23, Al = 27, Fe = 56.
I. Phần trắc nghiệm
Câu 1: Xét 2 phương trình phản ứng theo sơ đồ sau: 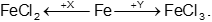
Hai chất X, Y theo thứ tự lần lượt là
A. HCl, FeCl3.
B. Cl2 , HCl.
C. CuCl2, Cl2.
D. Cl2 , FeCl3.
Câu 2: Cho dãy các chất: NaOH, HCl, Na2SO4, MgCl2; CuSO4. Số chất trong dãy phản ứng với Al là
A. 5.
B. 4.
C. 3.
D. 2.
Câu 3: Phản ứng nào sau đây tạo ra muối sắt(II)?
A. FeO tác dụng với dung dịch H2SO4 đặc, nóng (dư).
B. FeO tác dụng với dung dịch HNO3 loãng (dư).
C. Fe tác dụng với Cl2.
D. Fe tác dụng với dung dịch CuSO4.
Câu 4: Kim loại vừa tác dụng được với dung dịch NaOH, vừa tác dụng được với dung dịch HCl là
A. Mg.
B. Fe.
C. Cu.
D. Al.
Câu 5: Cho các khẳng định sau:
(1) Al là kim loại nặng hơn Ba.
(2) Al là kim loại dẫn điện bằng 2/3 Cu và nhẹ bằng 1/3 Cu.
(3) Al là kim loại dẻo nhất trong các kim loại.
(4) Trong điện phân Al2O3 nóng chảy, Al sinh ra ở trạng thái lỏng.
Khẳng định đúng là
A. (2) và (4).
B. (1) và (4).
C. (2) và (3).
D. (1), (3) và (4).
Câu 6: Nung hỗn hợp bột gồm Al và Fe3O4 trong bình kín (không có không khí) đến khi phản ứng hoàn toàn, thu được hỗn hợp X. Cho X vào nước vôi trong dư, thấy không có khí thoát ra. Vậy hỗn hợp X gồm
A. Al2O3, Fe2O3, Fe.
B. Al2O3, Fe.
C. Al2O3, Fe3O4, Al.
D. Al2O3, Fe, Al.
Câu 7: Cho dãy các chất: FeO, Fe(OH)2, FeSO4, Fe2(SO4)3, Fe3O4 , Fe2O3. Số chất trong dãy tác dụng được với dung dịch HNO3 đặc, nóng là
A. 3.
B. 5.
C. 4
D. 6.
Câu 8: Sắt là kim loại phổ biến thứ hai (sau nhôm) trên vỏ Trái Đất. Số proton và số nơtron có trong một nguyên tử sắt lần lượt là
A. 26 và 30.
B. 30 và 56.
C. 26 và 28.
D. 26 và 56.
Câu 9: Hỗn hợp X gồm: Al, Al2O3, Al(OH)3. X tan hoàn toàn trong
A. H2SO4 đặc, nguội, dư.
B. dd KOH dư.
C. dd FeCl2 dư.
D. HNO3 đặc, nguội
Câu 10: Trong quá trình luyện gang, nhiên liệu X (không có sẵn trong tự nhiên, phải điều chế từ than mỡ) có vai trò cung cấp nhiệt khi cháy và tạo ra chất khử CO để khử oxit sắt thành gang. Nhiên liệu X là
A. Than gỗ.
B. Than đá.
C. Than cốc.
D. Than chì.
II. Phần tự luận
Câu 1 (2 điểm): Khử hoàn toàn 11,6 gam oxit sắt bằng CO ở nhiệt độ cao. Sản phẩm khí dẫn vào dung dịch Ca(OH)2 dư, tạo ra 20 gam kết tủa. Viết các PTHH xảy ra và xác định công thức của oxit sắt.
Câu 2 (3 điểm): Cho m gam hỗn hợp G gồm: Na, Al, Fe vào nước dư thu được 4,48 lít khí (ở đktc).
Mặt khác cho m gam G ở trên vào dung dịch KOH dư thu được 7,84 lít khí (ở đktc) và dung dịch X, chất rắn Y. Hòa tan hoàn toàn Y vào H2SO4 đặc thu được 5,04 lít khí (ở đktc).
Tính giá trị của m.
Đáp án & Thang điểm
1. Phần trắc nghiệm (0,5 điểm/ 1 câu)
| Câu | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| Đ/a | C | C | D | D | A | B | B | A | B | C |
Câu 1 : Fe + CuCl2 → FeCl2 + Cu
2Fe + 3Cl2 → 2FeCl3. Chọn đáp án C.
Câu 2: Chất trong dãy phản ứng với Al là NaOH, HCl, CuSO4. Chọn đáp án C.
Câu 3: Fe + CuSO4 → FeSO4 + Cu. Chọn đáp án D.
Câu 4: Al vừa tác dụng được với dung dịch NaOH, vừa tác dụng được với dung dịch HCl. Chọn đáp án D.
Câu 5: Khẳng định đúng là
(2) Al là kim loại dẫn điện bằng 2/3 Cu và nhẹ bằng 1/3 Cu.
(4) Trong điện phân Al2O3 nóng chảy, Al sinh ra ở trạng thái lỏng. Chọn đáp án A.
Câu 6: X gồm Al2O3 và Fe. Chọn đáp án B.
Câu 7: Chất trong dãy tác dụng được với dung dịch HNO3 đặc, nóng là FeO, Fe(OH)2, FeSO4, Fe3O4 , Fe2O3. Chọn đáp án B.
Câu 8: Số proton và số nơtron có trong một nguyên tử sắt lần lượt là 26 và 30. Chọn đáp án A.
Câu 9: Hỗn hợp X gồm: Al, Al2O3, Al(OH)3 tan hoàn toàn trong dd KOH dư. Chọn đáp án B.
Câu 10: X là than cốc. Chọn đáp án C.
2. Phần tự luận
Câu 1 (2điểm):
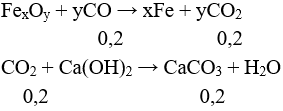
Ta có: nO (FexOy) = nCO = 0,2 mol
mFe (FexOy) = 11,6 – 0,2.16 = 8,4 gam → nFe (FexOy) = 0,15 mol
x : y = nFe (oxit) : nO (oxit) = 0,15 : 0,2 = 3 : 4.
Vậy oxit sắt là Fe3O4.
Câu 2 (3điểm): Gọi số mol Na, Al, Fe lần lượt là x, y và z (mol)
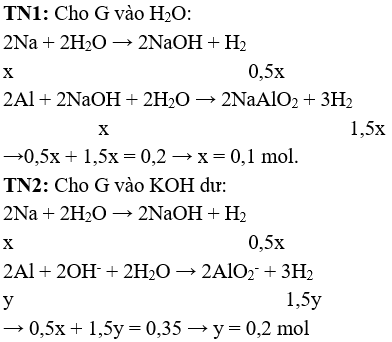
Y là Fe. Bảo toàn e: 3.nFe = 2.nkhí → 3z = 2.0,225 → z = 0,15.
m = 0,1.23 + 0,2.27 + 0,15.56 = 16,1 gam.
Chú ý: HS làm theo cách khác đúng vẫn cho điểm tối đa.
Sở Giáo dục và Đào tạo .....
Đề kiểm tra 15 phút học kì 2
Môn: Hóa Học 12
Thời gian làm bài: 15 phút
(Đề 2)
Cho nguyên tử khối của các nguyên tố: O = 16, H = 1, Cu = 64, Fe = 56, Na = 23.
I. Phần trắc nghiệm
Câu 1: Cho các nhận xét sau:
(1) Fe3O4 là quặng giàu sắt nhất để luyện gang
(2) Hợp chất sắt (II) chỉ có tính khử.
(3) Hàm lượng cacbon trong gang nhiều hơn trong thép (4) Fe tác dụng được với hơi nước ở nhiệt độ cao
(5) Fe (Z=26) thuộc chu kì 4, nhóm VIIIB
(6) Fe2O3 có tính oxi hóa
Số nhận xét đúng là
A. 5
B. 4.
C. 3.
D. 6
Câu 2: Quá trình sản xuất Al trong công nghiệp bằng phương pháp điện phân quặng boxit cần dùng criolit (hay băng thạch). Công thức của criolit là
A. Cả B và D đều đúng.
B. Na3AlF6.
C. KAl(SO4)2.12H2O.
D. 3NaF.AlF3.
Câu 3: Phản ứng hóa học xảy ra trong trường hợp nào dưới đây không thuộc loại phản ứng nhiệt nhôm?
A. Al tác dụng với CuO nung nóng.
B. Al tác dụng với Fe3O4 nung nóng
C. Al tác dụng với Fe2O3 nung nóng
D. Al tác dụng với axit H2SO4 đặc nóng
Câu 4: Số electron lớp ngoài cùng của nguyên tử Al là
A. 3.
B. 4.
C. 2.
D. 1.
Câu 5: Cho sơ đồ chuyển hoá: 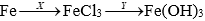
A. HCl, NaOH.
B. NaCl, Cu(OH)2.
C. Cl2, NaOH.
D. HCl, Al(OH)3.
Câu 6: Kim loại phản ứng được với dung dịch NaOH là
A. Cu.
B. Fe.
C. Al.
D. Ag.
Câu 7: Nguyên liệu sản xuất thép là:
A. quặng manhetit
B. quặng pirit
C. quặng hematit
D. gang
Câu 8: Hợp chất sắt (II) sunfat có công thức là
A. Fe(OH)3.
B. Fe2O3.
C. Fe2(SO4)3.
D. FeSO4.
Câu 9: Trộn bột kim loại Al với chất X (gọi là hỗn hợp tecmit) để thực hiện phản ứng nhiệt nhôm dùng để hàn đường ray tàu hỏa. Chất X là
A. FeCO3.
B. Fe3O4.
C. Fe.
D. Al.
Câu 10: Cấu hình electron nào sau đây là của Fe( Z = 26)?
A. [Ar]3d8.
B. [Ar]3d74s1.
C. [Ar]3d64s2.
D. [Ar] 4s23d6.
II. Phần tự luận
Câu 1 (2 điểm): Hỗn hợp X gồm Na và Al. Cho m gam X vào một lượng dư nước thì thoát ra V lít khí. Nếu cũng cho m gam X vào dung dịch NaOH (dư) thì được 1,75V lít khí. Tính thành phần phần trăm theo khối lượng của Na trong X.
Câu 2 (3 điểm): Cho 61,2 gam hỗn hợp X gồm Cu và Fe3O4 tác dụng với dung dịch HNO3 loãng, đun nóng và khuấy đều. Sau khi các phản ứng xảy ra hoàn toàn, thu được 3,36 lít khí NO (sản phẩm khử duy nhất, ở đktc), dung dịch Y và còn lại 2,4 gam kim loại. Cô cạn dung dịch Y, thu được m gam muối khan. Tính giá trị của m.
Đáp án & Thang điểm
1. Phần trắc nghiệm (0,5 điểm/ 1 câu)
| Câu | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| Đ/a | B | A | D | A | C | C | D | D | B | C |
Câu 1: Nhận xét đúng là:
(3) Hàm lượng cacbon trong gang nhiều hơn trong thép
(4) Fe tác dụng được với hơi nước ở nhiệt độ cao
(5) Fe (Z=26) thuộc chu kì 4, nhóm VIIIB
(6) Fe2O3 có tính oxi hóa
Chọn đáp án B.
Câu 2: Công thức của criolit là Na3AlF6 hay 3NaF.AlF3. Chọn đáp án A.
Câu 3: Al tác dụng với axit H2SO4 đặc nóng không thuộc loại phản ứng nhiệt nhôm. Chọn đáp án D.
Câu 4: Al: [Ne]3s23p1. Số electron lớp ngoài cùng của nguyên tử Al là 3. Chọn đáp án A.
Câu 5: 2Fe + 3Cl2 → 2FeCl3
FeCl3 + 3NaOH → Fe(OH)3 + 3NaCl. Chọn đáp án C.
Câu 6: Al phản ứng được với dung dịch NaOH. Chọn đáp án C.
Câu 7: Nguyên liệu sản xuất thép là gang. Chọn đáp án D.
Câu 8: Hợp chất sắt (II) sunfat có công thức là FeSO4. Chọn đáp án D.
Câu 9: Trộn bột kim loại Al với chất X (gọi là hỗn hợp tecmit) để thực hiện phản ứng nhiệt nhôm dùng để hàn đường ray tàu hỏa. Chất X là Fe3O4. Chọn đáp án B.
Câu 10: Fe( Z = 26): [Ar]3d64s2. Chọn đáp án C.
2. Phần tự luận
Câu 1 (2điểm): Gọi số mol Na và Al trong hỗn hợp lần lượt là x và y (mol)
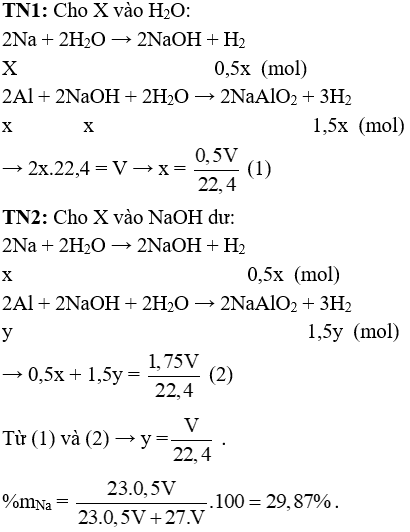
Câu 2 (3điểm):
Sau phản ứng còn kim loại dư → muối sau phản ứng là Cu(NO3)2 và Fe(NO3)2
mX phản ứng = 61,2 – 2,4 = 58,8 gam.
Gọi x và y lần lượt là số mol Cu và Fe3O4 đã phản ứng.
→ 64x + 232y = 58,8 (1)

Giải hệ pt được: x = 0,375 và y = 0,15
mmuối = 0,375.188 + 0,45.180 = 151,5 gam.
Chú ý: HS làm theo cách khác đúng vẫn cho điểm tối đa.
Sở Giáo dục và Đào tạo .....
Đề kiểm tra 15 phút học kì 2
Môn: Hóa Học 12
Thời gian làm bài: 15 phút
(Đề 3)
Cho nguyên tử khối của các nguyên tố: O = 16, H = 1, Fe = 56, Al = 27, S = 32.
I. Phần trắc nghiệm
Câu 1: Sắt tây là hợp kim của sắt và kim loại nào sau đây?
A. Cr.
B. Ag.
C. Sn.
D. Zn.
Câu 2: Al thể hiện tính chất nào sau đây:
1) Nhôm có cấu tạo mạng tinh thể lập phương tâm diện.
2) Là kim loại màu trắng bạc, mềm, dễ kéo sợi và dát mỏng.
3) Nhôm dẫn điện và dẫn nhiệt tốt.
4) Nhôm là kim loại nhẹ, nóng chảy ở nhiệt độ 660˚C.
5) Nhôm là nguyên tố s
A. 1, 2, 3, 4.
B. 1, 2, 3.
C. 1, 3, 4, 5.
D. 1, 2, 4, 5.
Câu 3: Hoà tan hoàn toàn 11,2 gam Fe bằng dd H2SO4 đặc nóng dư, thu được V lít khí SO2 (đktc, là sản phẩm khử duy nhất). Giá trị của V là
A. 4,48.
B. 3,36.
C. 2,24.
D. 6,72.
Câu 4: Nhúng một lá sắt nhỏ vào dung dịch chứa một trong các chất sau: FeCl3; HCl; H2SO4 đặc; HNO3 đặc; Cu(NO3)2; CaCl2; NaOH. Số trường hợp sinh ra muối sắt (II) là
A. 3.
B. 4.
C. 5.
D. 6.
Câu 5: Hợp chất nào sau đây không chứa nhôm?
A. Criolit.
B. Boxit.
C. Mica.
D. Xinvinit.
Câu 6: Sản phẩm tạo thành có chất kết tủa khi dung dịch Fe2(SO4)3 tác dụng với dung dịch nào sau đây?
A. NaOH.
B. CuSO4.
C. NaCl.
D. Na2SO4.
Câu 7: Cho sơ đồ chuyển hóa:
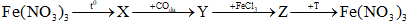
Các chất X và T lần lượt là
A. FeO và AgNO3.
B. Fe2O3 và AgNO3.
C. FeO và NaNO3.
D. Fe2O3 và Cu(NO3)2
Câu 8: Al2O3 phản ứng được với cả hai dung dịch:
A. Na2SO4, KOH.
B. NaOH, HCl.
C. KCl, NaNO3.
D. NaCl, H2SO4.
Câu 9: Sắt có thể tan trong dung dịch nào sau đây?
A. FeCl3.
B. MgCl2.
C. FeCl2.
D. AlCl3.
Câu 10: Cho 2,7 gam Al tác dụng hoàn toàn với dung dịch NaOH dư. Sau khi phản ứng kết thúc, thể tích khí H2 (ở đktc) thoát ra là
A. 2,24 lít.
B. 4,48 lít.
C. 3,36 lít.
D. 6,72 lít.
II. Phần tự luận
Câu 1 (2 điểm): Cho 200 ml dung dịch AlCl3 1,5M tác dụng với V lít dung dịch NaOH 0,5M, lượng kết tủa thu được là 15,6 gam. Xác định giá trị lớn nhất của V.
Câu 2 (3 điểm): Hòa tan hoàn toàn 2,44 gam hỗn hợp bột X gồm FexOy và Cu bằng dung dịch H2SO4 đặc nóng (dư). Sau phản ứng thu được 0,504 lít khí SO2 (sản phẩm khử duy nhất, ở đktc) và dung dịch chứa 6,6 gam hỗn hợp muối sunfat. Tính phần trăm khối lượng của Cu trong X.
Đáp án & Thang điểm
1. Phần trắc nghiệm (0,5 điểm/ 1 câu)
| Câu | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| Đ/a | C | A | D | A | D | A | B | B | A | C |
Câu 1: Sắt tây là hợp kim của sắt và kim loại Sn. Chọn đáp án C.
Câu 2: Al thể hiện các tính chất:
1) Nhôm có cấu tạo mạng tinh thể lập phương tâm diện.
2) Là kim loại màu trắng bạc, mềm, dễ kéo sợi và dát mỏng.
3) Nhôm dẫn điện và dẫn nhiệt tốt.
4) Nhôm là kim loại nhẹ, nóng chảy ở nhiệt độ 660˚C. Chọn đáp án A.
Câu 3: Bảo toàn e: 3.nFe = 2.nkhí → nkhí = 0,3 → V = 0,3.22,4 = 6,72 lít. Chọn đáp án D.
Câu 4: Fe + 2FeCl3 → 3FeCl2
Fe + 2HCl → FeCl2 + H2
Fe + Cu(NO3)2 → Fe(NO3)2 + Cu. Chọn đáp án A.
Câu 5: Hợp chất không chứa nhôm là Xinvinit. Chọn đáp án D.
Câu 6: Fe2(SO4)3 + 6NaOH → 2Fe(OH)3 ↓ + 3Na2SO4. Chọn đáp án A.
Câu 7:
4Fe(NO3)3 2Fe2O3 + 12NO2 + 3O2
Fe2O3 + 3CO dư 2Fe + 3CO2
Fe + 2FeCl3 → 3FeCl2
FeCl2 + 3AgNO3 → Fe(NO3)3 + Ag + 2AgCl
Chọn đáp án B.
Câu 8: Al2O3 phản ứng được với cả hai dung dịch NaOH và HCl. Chọn đáp án B.
Câu 9: Fe + 2FeCl3 → 3FeCl2. Chọn đáp án A.
Câu 10: Bảo toàn e: 3.nAl = 2.nkhí → nkhí = 0,15 mol → Vkhí = 0,15.22,4 = 3,36 lít. Chọn đáp án C.
2. Phần tự luận
Câu 1 (2điểm): Tính được số mol AlCl3 = 0,3 mol; số mol kết tủa = 0,2 mol
Có nAlCl3 > n↓. Để Vmax thì ban đầu tạo kết tủa max, sau đó kết tủa tan một phần.
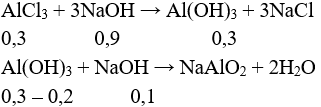
→ nNaOH = 0,9 + 0,1 = 1 mol → V = 1 : 0,5 = 2 lít.
Câu 2 (3điểm): Quy đổi hỗn hợp gồm: Fe (x mol), O (y mol) và Cu (z mol).
Ta có: mhh = 2,44 gam → 56x + 16y + 64z =2,44 (1)
Bảo toàn e: 3x – 2y + 2z = 0,045 (2)
Do H2SO4 dư, nên muối sunfat là Fe2(SO4)3: 0,5x mol và CuSO4 z mol
→ 200x + 160z = 6,6 (3)
Giải hệ được: x = y = 0,025; z = 0,01.
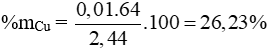
Chú ý: HS làm theo cách khác đúng vẫn cho điểm tối đa.
Sở Giáo dục và Đào tạo .....
Đề kiểm tra 15 phút học kì 2
Môn: Hóa Học 12
Thời gian làm bài: 15 phút
(Đề 4)
Cho nguyên tử khối của các nguyên tố: O = 16, H = 1, Al = 27, Fe = 56, Zn = 65.
I. Phần trắc nghiệm
Câu 1: Nhúng một lá sắt nhỏ vào dung dịch chứa lượng dư một trong những chất sau: FeCl3, AlCl3, CuSO4, Pb(NO3)2, NaCl, HCl, HNO3 loãng, H2SO4 đặc nóng, NH4NO3. Số trường hợp phản ứng tạo muối Fe(II) là
A. 3.
B. 4.
C. 5.
D. 6.
Câu 2: Khi cho hỗn hợp Fe3O4 và Cu vào dd H2SO4 loãng dư thu được chất rắn X và dd Y. Dãy nào dưới đây gồm các chất đều tác dụng được với dd Y?
A. KI, NH3, NH4Cl.
B. NaOH, Na2SO4,Cl2.
C. BaCl2, HCl, Cl2.
D. Br2, NaNO3, KMnO4.
Câu 3: Chất vừa có tính oxi hóa vừa có tính khử là
A. Fe2(SO4)3 .
B. NaCl.
C. Fe(OH)2.
D. Fe3O4.
Câu 4: Trong các chất: Al, Na, Al2O3, MgO. Số chất vừa tan được trong dung dịch NaOH, vừa tan được trong dung dịch HCl là
A. 3.
B. 2.
C. 1.
D. 4.
Câu 5: Dụng cụ bằng chất nào sau đây không nên dùng để chứa dung dịch kiềm?
A. Fe
B. Cu
C. Ag
D. Al
Câu 6: Dung dịch FeSO4 có lẫn tạp chất là CuSO4. Để loại bỏ CuSO4 có thể ngâm vào dung dịch trên kim loại nào sau đây?
A. Fe.
B. Cu.
C. Al.
D. Sn.
Câu 7: Quặng nào sau đây không chứa sắt ?
A. Manhetit.
B. Hemantit.
C. Xiđerit.
D. Apatit.
Câu 8: Để phân biệt các chất rắn riêng biệt: Al2O3; Mg; Al người ta có thể dùng một trong các hóa chất nào sau đây ?
A. Dung dịch HCl.
B. Dung dịch H2SO4 loãng.
C. Dung dịch NaOH.
D. Dung dịch HNO3 loãng.
Câu 9: Hòa tan 5,4 gam Al vào 100ml dung dịch NaOH 0,2M. Sau khi phản ứng xảy ra hoàn toàn thể tích khí H2 ở đktc thu được là
A. 4,48 lít.
B. 0,448 lít.
C. 6,72 lít.
D. 0,672 lít.
Câu 10: Trong các phát biểu sau:
(1) Trong lò cao, quá trình tạo gang xảy ra ở nồi lò.
(2) Thép là hợp kim của sắt với cacbon trong đó, %C cỡ 2-5% về khối lượng.
(3) Vonfam (W) là kim loại có nhiệt độ nóng chảy cao nhất.
(4) Kim cương là kim loại cứng nhất.
(5) Cấu hình electron lớp ngoài cùng của nguyên tử kim loại kiềm là ns1.
(6) Nước cứng là nước có chứa nhiều ion: Mg2+ và Ca2+.
Số phát biểu đúng là
A. 3
B. 4
C. 2
D. 5
II. Phần tự luận
Câu 1 (2 điểm): Cho 150 ml dung dịch KOH 1,2M tác dụng với 100 ml dung dịch AlCl3 nồng độ x mol/l, thu được dung dịch Y và 4,68 gam kết tủa. Loại bỏ kết tủa, thêm tiếp 175 ml dung dịch KOH 1,2M vào Y, thu được 2,34 gam kết tủa. Tính giá trị của x.
Câu 2 (3 điểm): Một hỗn hợp X gồm Fe và Zn khi tác dụng với dung dịch NaOH dư cho ra 3,136 lít khí (đktc) và để lại một chất rắn A. Hoà tan hết A trong dung dịch H2SO4 loãng, sau đó thêm NaOH dư được kết tủa B. Nung B ngoài không khí đến khối lượng không đổi được chất rắn nặng 12,8 gam . Viết các PTHH xảy ra và tính khối lượng của hỗn hợp X.
Đáp án & Thang điểm
1. Phần trắc nghiệm (0,5 điểm/ 1 câu)
| Câu | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| Đ/a | B | D | D | A | D | A | D | C | D | A |
Câu 1: Fe + 2FeCl3 → 3FeCl2
Fe + CuSO4 → FeSO4 + Cu
Fe + Pb(NO3)2 → Fe(NO3)2 + Pb
Fe + 2HCl → FeCl2 + H2
Chọn đáp án B.
Câu 2: Chất rắn X là Cu, vậy dd Y gồm CuSO4 và FeSO4, H2SO4 dư. Các chất tác dụng được với dung dịch Y là Br2, NaNO3, KMnO4. Chọn đáp án D.
Câu 3: Fe3O4 vừa có tính oxi hóa vừa có tính khử. Chọn đáp án D.
Câu 4: Al, Na, Al2O3 vừa tan được trong dung dịch NaOH, vừa tan được trong dung dịch HCl. Chọn đáp án A.
Câu 5: Dụng cụ bằng Al không nên dùng để chứa dung dịch kiềm. Chọn đáp án D.
Câu 6: Fe + CuSO4 → FeSO4 + Cu. Chọn đáp án A.
Câu 7: Quặng apatit không chứa sắt. Chọn đáp án D.
Câu 8: Dùng NaOH, hiện tượng:
- Chất rắn tan, có khí thoát ra → Al
2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2
- Chất rắn tan → Al2O3
Al2O3 + 2NaOH → 2NaAlO2 + H2O
- Không hiện tượng → MgO. Chọn đáp án C.
Câu 9:
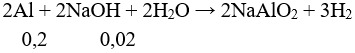
→ Al dư, NaOH hết → nkhí = 0,03 mol → Vkhí = 0,672 lít. Chọn đáp án D.
Câu 10: Phát biểu đúng là:
(3) Vonfam (W) là kim loại có nhiệt độ nóng chảy cao nhất.
(5) Cấu hình electron lớp ngoài cùng của nguyên tử kim loại kiềm là ns1.
(6) Nước cứng là nước có chứa nhiều ion: Mg2+ và Ca2+.
Chọn đáp án A.
2. Phần tự luận
Câu 1 (2 điểm):
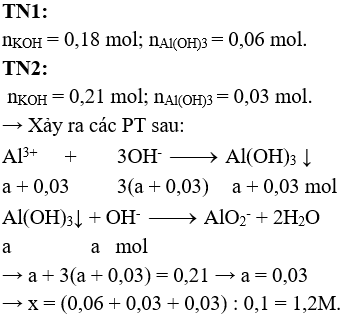
Câu 2 (3 điểm):
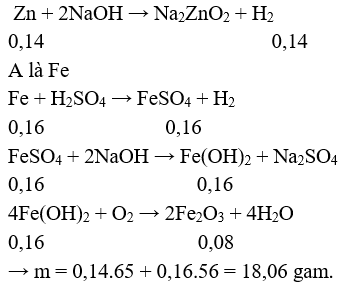
Chú ý: HS làm theo cách khác đúng vẫn cho điểm tối đa.
Xem thêm các đề thi Hóa học 12 chọn lọc, có đáp án hay khác:
- 12+ Đề kiểm tra 15 phút Hóa 12 Học kì 2 có đáp án (Bài số 1)
- Đề kiểm tra 15 phút Hóa 12 Học kì 2 trắc nghiệm có đáp án (Bài số 1)(8 đề)
- Đề kiểm tra 15 phút Hóa 12 Học kì 2 trắc nghiệm - tự luận có đáp án (Bài số 1)(3 đề)
- 12+ Đề kiểm tra 15 phút Hóa 12 Học kì 2 có đáp án (Bài số 2)
- Đề kiểm tra 15 phút Hóa 12 Học kì 2 trắc nghiệm có đáp án (Bài số 2)(8 đề)
- 9+ Đề thi Hóa học 12 Giữa kì 2 năm 2026 (cấu trúc mới, có đáp án)
- Đề thi Hóa học 12 Giữa kì 2 trắc nghiệm năm 2026 có đáp án (3 đề)
- Đề thi Hóa học 12 Giữa kì 2 trắc nghiệm - tự luận năm 2026 có đáp án (5 đề)
- 9+ Đề thi Hóa học 12 Giữa kì 2 năm 2026 (cấu trúc mới, có đáp án)
- Đề thi Hóa học 12 Giữa kì 2 trắc nghiệm năm 2026 có đáp án (3 đề)
- Đề thi Hóa học 12 Giữa kì 2 trắc nghiệm - tự luận năm 2026 có đáp án (5 đề)
- 9+ Đề thi Hóa học 12 Học kì 2 năm 2026 (cấu trúc mới, có đáp án)
- Đề thi Hóa học 12 Học kì 2 trắc nghiệm năm 2026 có đáp án (3 đề)
- Đề thi Hóa học 12 Học kì 2 trắc nghiệm - tự luận năm 2026 có đáp án (5 đề)
Để học tốt lớp 12 các môn học sách mới:
- Giải bài tập Lớp 12 Kết nối tri thức
- Giải bài tập Lớp 12 Chân trời sáng tạo
- Giải bài tập Lớp 12 Cánh diều
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Giáo án lớp 12 (các môn học)
- Giáo án điện tử lớp 12 (các môn học)
- Giáo án Toán 12
- Giáo án Ngữ văn 12
- Giáo án Vật Lí 12
- Giáo án Hóa học 12
- Giáo án Sinh học 12
- Giáo án Địa Lí 12
- Giáo án Lịch Sử 12
- Giáo án Lịch Sử 12 mới
- Giáo án GDCD 12
- Giáo án Kinh tế Pháp luật 12
- Giáo án Tin học 12
- Giáo án Công nghệ 12
- Giáo án GDQP 12
- Đề thi lớp 12 (các môn học)
- Đề thi Ngữ văn 12
- Đề thi Toán 12
- Đề thi Tiếng Anh 12 mới
- Đề thi Tiếng Anh 12
- Đề thi Vật Lí 12
- Đề thi Hóa học 12
- Đề thi Sinh học 12
- Đề thi Địa Lí 12
- Đề thi Lịch Sử 12
- Đề thi Giáo dục Kinh tế Pháp luật 12
- Đề thi Giáo dục quốc phòng 12
- Đề thi Tin học 12
- Đề thi Công nghệ 12






 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

