Cách giải bài tập oxit tác dụng với nước (cực hay, chi tiết)
Bài viết Cách giải bài tập oxit tác dụng với nước với phương pháp giải chi tiết giúp học sinh ôn tập, biết cách làm bài tập oxit tác dụng với nước.
Cách giải bài tập oxit tác dụng với nước (cực hay, chi tiết)
Thi online KHTN 8 KNTTThi online KHTN 8 CDThi online KHTN 8 CTST
A. Lý thuyết & Phương pháp giải
1. Nước tác dụng với basic oxide
+ Nước có thể tác dụng với một số basic oxide như K2O, Na2O, CaO, BaO… tạo ra dung dịch bazơ tương ứng.
+ Dung dịch bazơ làm đổi màu quỳ tím thành xanh.
Ví dụ:
CaO + H2O → Ca(OH)2
Lưu ý: phản ứng trên còn gọi là phản ứng tôi vôi, dung dịch Ca(OH)2 gọi là nước vôi trong.
2. Nước tác dụng với acidic oxide
+ Nước tác dụng với acidic oxide như SO2, P2O5,... tạo ra axit tương ứng
+ Dung dịch axit làm đổi màu quỳ tím thành đỏ.
Ví dụ: P2O5 + 3H2O → 2H3PO4
Các bước giải toán:
+ Tính số mol các chất đã cho
+ Viết phương trình hóa học
+ Xác định chất dư, chất hết (nếu có), tính toán theo chất hết
+ Tính khối lượng hoặc thể tích các chất theo yêu cầu đề bài
- Nắm vững kiến thức về lập phương trình hóa học, cân bằng hóa học và các công thức chuyển đổi khối lượng, thể tích
- Áp dụng định luật bảo toàn khối lượng: mtham gia = msản phẩm
- Nếu bài cho số liệu số mol cả chất tham gia phản ứng và chất sản phẩm thì tính toán theo chất sản phẩm.
B. Ví dụ minh họa
Ví dụ 1: Lập phương trình hóa học của các phản ứng sau:
(1) carbon dioxide + nước → carbonic acid (H2CO3)
(2) sulfur dioxide +nước → sulfurous acid (H2SO3)
(3) sodium oxide + nước → sodium hydroxide (NaOH)
(4) barium oxide + nước → bari hiđroxit (Ba(OH)2)
Lời giải:
(1) CO2 + H2O → H2CO3
(2) SO2 + H2O → H2SO3
(3) Na2O + H2O → 2NaOH
(4) BaO + H2O → Ba(OH)2
Ví dụ 2: Cho 12,4 gam sodium oxide tác dụng hết với nước.
a) Viết phương trình hóa học.
b) Tính khối lượng sodium hydroxide có trong dung dịch thu được.
Lời giải:
a) Phương trình hóa học: Na2O + H2O → 2NaOH
b) Số mol Na là: nNa2O = 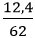
Na2O + H2O → 2NaOH
0,2 → 0,4 (mol)
Theo phương trình: nNaOH = 2nNa2O = 0,4 mol
Khối lượng sodium hydroxide có trong dung dịch thu được là:
mNaOH = nNaOH.MNaOH = 0,4.40 = 16 gam
Ví dụ 3: Hòa tan hỗn hợp gồm (28,4 gam P2O5 và 12 gam SO3) vào nước dư, thu được dung dịch chứa bao nhiêu gam chất tan?
Lời giải:
Số mol P2O5 là: nP2O5 = 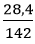
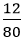
Phương trình hóa học:
P2O5 + 3H2O → 2H3PO4
0,2 → 0,4 (mol)
Khối lượng H3PO4 là: mH3PO4 = nH3PO4.MH3PO4 = 0,4.98 = 39,2 gam
SO3 + H2O → H2SO4
0,15 → 0,15 (mol)
Khối lượng H2SO4 là: mH2SO4 = nH2SO4.MH2SO4 = 0,15.98 = 14,7 gam
Tổng khối lượng H3PO4 và H2SO4 có trong dung dịch thu được là:
mhh = 39,2 + 14,7 = 53,9 gam.
C. Bài tập vận dụng
Câu 1: basic oxide nào sau đây không tác dụng với nước:
A. BaO
B. Na2O
C. CaO
D. Al2O3
Lời giải:
Đáp án D
Nước có thể tác dụng với một số basic oxide như K2O, Na2O, CaO, BaO … tạo ra bazơ ⇒ basic oxide không tác dụng với nước là: Al2O3.
Câu 2: Cho CaO tác dụng với nước thu được dung dịch nước vôi trong. Cho quỳ tím vào nước vôi trong, hiện tượng xảy ra là:
A. Quỳ tím chuyển màu đỏ
B. Quỳ tím không đổi màu
C. Quỳ tím chuyển màu xanh
D. Không có hiện tượng
Lời giải:
Đáp án C
Nước vôi trong là dung dịch Ca(OH)2: dung dịch bazơ
⇒ làm quỳ tím chuyển sang màu xanh.
Câu 3: Oxit tác dụng với nước tạo ra dung dịch làm quỳ tím hóa xanh là:
A. CO2
B. P2O5
C. Na2O
D. CuO
Lời giải:
Đáp án C
Na2O + H2O → 2NaOH
Dung dịch NaOH là dung dịch bazơ nên có thể làm quỳ tím chuyển xanh
Câu 4: Cho oxit A tác dụng với nước tạo nitric acid. Xác định A, biết MA = 108 g/mol, trong A có 2 nguyên tử nitơ.
A. NO2
B. N2O3
C. N2O
D. N2O5
Lời giải:
Đáp án D
Trong A có 2 nguyên tử nitơ ⇒ gọi công thức của A có dạng N2On
Theo đầu bài: MA = 108 g/mol ⇒ 14.2 + 16.n = 108 ⇒ n = 5.
Vậy công thức hóa học của A là: N2O5
N2O5 + H2O → 2HNO3
Câu 5: Cho nước tác dụng với SO3 thu được dung dịch A. Khi cho quỳ tím vào dung dịch A, quỳ tím chuyển sang màu gì?
A. Đỏ
B. Xanh
C. Tím
D. Không màu
Lời giải:
Đáp án A
SO3 + H2O → H2SO4
Sau phản ứng thu được dung dịch axit. Khi cho quỳ tím vào dung dịch axit, quỳ tím chuyển màu đỏ
Câu 6: Hòa tan 21,3 gam P2O5 vào nước dư, thu được dung dịch chứa bao nhiêu gam chất tan?
A. 14,7 gam.
B. 29,4 gam.
C. 44,1 gam.
D. 19,6 gam.
Lời giải:
Đáp án B
Số mol P2O5 là: nP2O5 = 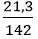
Phương trình hóa học:
P2O5 + 3H2O → 2H3PO4
0,15 → 0,3 (mol)
Khối lượng H2PO4 thu được là:
mH3PO4 = nH3PO4.MH3PO4 = 0,3.98 = 29,4gam
Câu 7: Cho các oxit sau: CuO, K2O, CaO, SiO2, SO2. Số oxit không tác dụng được với nước là
A. 1.
B. 2.
C. 3.
D. 4.
Lời giải:
Chọn B
Hai oxit không tác dụng với nước là CuO và SiO2.
Câu 8: Hòa tan 11,28 gam K2O vào nước dư, thu được dung dịch chứa m gam KOH. Tính m ?
A. 6,72 gam.
B. 13,44 gam.
C. 8,40 gam.
D. 8,96 gam.
Lời giải:
Đáp án B
Số mol K2O là: nK2O = 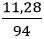
K2O + H2O → 2KOH
0,12 → 0,24 (mol)
Khối lượng KOH có trong dung dịch thu được là:
mKOH = nKOH.MKOH = 0,24.56 = 13,44 gam.
Câu 9: Hòa tan một lượng BaO vào nước dư thu được dung dịch chứa 17,1 gam Ba(OH)2. Tính khối lượng BaO đã phản ứng?
A. 30,6 gam.
B. 15,3 gam.
C. 20,4 gam.
D. 26,48 gam.
Lời giải:
Đáp án B
Số mol Ba(OH)2 là: nBa(OH)2 = 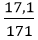
BaO + H2O → Ba(OH)2
0,1 ← 0,1 (mol)
Khối lượng BaO đã phản ứng là:
mBaO = nBaO.MBaO = 0,1.153 = 15,3 gam
Câu 10: Hòa tan hỗn hợp gồm (12,4 gam Na2O và 15,3 gam BaO) vào nước dư, thu được dung dịch chứa m gam hỗn hợp NaOH và Ba(OH)2. Tính m?
A. 33,1 gam.
B. 17,1 gam.
C. 49,65 gam.
D. 26,48 gam.
Lời giải:
Đáp án A
nNa2O = 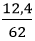
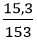
Na2O + H2O → 2NaOH
0,2 → 0,4 (mol)
Khối lượng NaOH có trong dung dịch thu được là: mNaOH = 0,4.40 = 16 gam
BaO + H2O → Ba(OH)2
0,1 → 0,1 (mol)
Khối lượng Ba(OH)2 có trong dung dịch là: mBa(OH)2 = 0,1.171 = 17,1 gam
Tổng khối lượng NaOH và Ba(OH)2 có trong dung dịch là:
m = 16 + 17,1 = 33,1 gam.
Thi online KHTN 8 KNTTThi online KHTN 8 CDThi online KHTN 8 CTST
Xem thêm các dạng bài tập Hóa học lớp 8 có đáp án hay khác:
- Cách phân biệt một số chất khí lớp 8 thường gặp (cực hay)
- Cách phân biệt axit, bazo, muối (cực hay, chi tiết)
- Bài tập xác định công thức hóa học và gọi tên axit (cực hay, chi tiết)
- Bài tập xác định công thức hóa học và gọi tên bazo (cực hay, chi tiết)
- Bài tập xác định công thức hóa học và gọi tên muối (cực hay, chi tiết)
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Loạt bài Lý thuyết - Bài tập Hóa học lớp 8 có đáp án được biên soạn bám sát nội dung chương trình sgk Hóa học 8.
Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Giải Tiếng Anh 8 Global Success
- Giải sgk Tiếng Anh 8 Smart World
- Giải sgk Tiếng Anh 8 Friends plus
- Lớp 8 - Kết nối tri thức
- Soạn văn 8 (hay nhất) - KNTT
- Soạn văn 8 (ngắn nhất) KNTT
- Giải sgk Toán 8 - KNTT
- Giải sgk Khoa học tự nhiên 8 - KNTT
- Giải sgk Lịch Sử 8 - KNTT
- Giải sgk Địa Lí 8 - KNTT
- Giải sgk Giáo dục công dân 8 - KNTT
- Giải sgk Tin học 8 - KNTT
- Giải sgk Công nghệ 8 - KNTT
- Giải sgk Hoạt động trải nghiệm 8 - KNTT
- Giải sgk Âm nhạc 8 - KNTT
- Lớp 8 - Chân trời sáng tạo
- Soạn văn 8 (hay nhất) - CTST
- Soạn văn 8 (ngắn nhất) - CTST
- Giải sgk Toán 8 - CTST
- Giải sgk Khoa học tự nhiên 8 - CTST
- Giải sgk Lịch Sử 8 - CTST
- Giải sgk Địa Lí 8 - CTST
- Giải sgk Giáo dục công dân 8 - CTST
- Giải sgk Tin học 8 - CTST
- Giải sgk Công nghệ 8 - CTST
- Giải sgk Hoạt động trải nghiệm 8 - CTST
- Giải sgk Âm nhạc 8 - CTST
- Lớp 8 - Cánh diều
- Soạn văn 8 Cánh diều (hay nhất)
- Soạn văn 8 Cánh diều (ngắn nhất)
- Giải sgk Toán 8 - Cánh diều
- Giải sgk Khoa học tự nhiên 8 - Cánh diều
- Giải sgk Lịch Sử 8 - Cánh diều
- Giải sgk Địa Lí 8 - Cánh diều
- Giải sgk Giáo dục công dân 8 - Cánh diều
- Giải sgk Tin học 8 - Cánh diều
- Giải sgk Công nghệ 8 - Cánh diều
- Giải sgk Hoạt động trải nghiệm 8 - Cánh diều
- Giải sgk Âm nhạc 8 - Cánh diều






 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

