Lý thuyết, Bài tập Hóa trị lớp 8 (có lời giải)
Bài viết tóm tắt lý thuyết trọng tâm và bài tập Hóa trị lớp 8 có lời giải giúp học sinh nắm vững kiến thức & ôn luyện để biết cách làm bài tập Hóa học 8.
Lý thuyết, Bài tập Hóa trị lớp 8 (có lời giải)
Thi online KHTN 8 KNTTThi online KHTN 8 CDThi online KHTN 8 CTST
A/ Lý thuyết Hóa trị
1. Cách xác định
- Hóa trị của nguyên tố (hay nhóm nguyên tử) là con số biểu thị khả năng liên kết của nguyên tử (hay nhóm nguyên tử)
- Quy ước : hóa trị của H là I ⇒ lấy làm đơn vị, hóa trị của các nguyên tố (hay nhóm nguyên tử) được xác định bằng số nguyên tử H mà nguyên tố (hay nhóm nguyên tử) có thể liên kết
2. Quy tắc hóa trị:
AxaByb với x, y: chỉ số
a, b: hóa trị của nguyên tố A, B
Theo quy tắc hóa trị: x ×a=y×b
VD: Từ CTHH của hợp chất FeIII(OH)3I, ta có: 1 x III = 3 x I
3. Vận dụng
a. Tính hóa trị của một nguyên tố:
VD: tính hóa trị của Cu trong Cu(OH)2, biết nhóm OH hóa trị I.
Gọi hóa trị của Cu là a, theo quy tắc hóa trị: a x 1 = I x 2, suy ra a = II
b. Lập công thức hóa học theo hóa trị
Cách làm:
Lập công thức chung dạng AxBy
Áp dụng quy tắc hóa trị, lập tỉ lệ
Nếu tỷ lệ này là phân số tối giản thì lấy x = b ; y = a
VD: lập CTHH của hợp chất tạo bởi sắt hóa trị III và oxi.
Viết CT dạng chung: FexOy
Theo quy tắc hóa trị: x×III=y×II
Chuyển thành tỷ lệ: 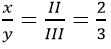
Vì vậy, lấy x = 2 ; y = 3
CTHH của hợp chất: Fe2O3
VD: lập CTHH của hợp chất tạo bởi đồng hóa trị II và nhóm SO4 hóa trị II
Viết CT chung dạng: Cux(SO4)y
Theo quy tắc hóa trị: x×II=y×II
Chuyển thành tỉ lệ:
CTHH của hợp chất CuSO4
B/ Bài tập vận dụng
Câu 1: Hoá trị của Al trong các hợp chất AlCl3 (biết Cl có hoá trị I) là
A. I
B. II
C. III
D. IV
Lời giải
- Gọi hoá trị của nhôm là a: ![]()
Theo quy tắc hóa trị => 1 . a = 3 . I => a = III
Đáp án cần chọn là: C
Câu 2: Xđ hóa trị của mỗi nguyên tố có trong các hợp chất sau đây, biết trong các hợp chất H có hóa trị I còn O có hóa trị II.
a/ KH, H2S, CH4
b/ FeO, Ag2O, SiO2
A. a/ KI, SII, CIV b) FeII, AgII, SiIV
B. a/ KI, SII, CIV b) FeIII, AgII, SiIV
C. a/ KI, SII ,CIV b) FeII, AgI, SiIV
D. a/ KI, SII, CIV b) FeIII, AgI, SiIV
Lời giải
![]() ⇒ a.1
⇒ a.1
=I.1
⇒a=I
![]()
⇒I×2=b×1
⇒b=II
![]()
⇒a×1=I×4
⇒a=IV
Vậy hóa trị của các nguyên tố có trong hợp chất lần lượt là:,,
b/ Làm tương tự câu a
FeII, AgI, SiIV
Đáp án cần chọn là: C
Câu 3: Hóa trị của nguyên tố Fe trong hợp chất FeCl2 là: (Biết Cl có hóa trị I)
A. a/ KI, SII, CIV b) FeII, AgII, SiIV
B. a/ KI, SII, CIV b) FeIII, AgII, SiIV
C. a/ KI, SII ,CIV b) FeII, AgI, SiIV
D. a/ KI, SII, CIV b) FeIII, AgI, SiIV
Lời giải
Đặt hóa trị của Fe trong hợp chất là x: 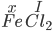
Theo quy tắc hóa trị có: x×1= I×2 ⇒ ![]() => chọn x = II thỏa mãn
=> chọn x = II thỏa mãn
Vậy hóa trị của Fe trong FeCl2 là 2
Đáp án cần chọn là: B
Câu 4 : Biết Ba có hóa trị II và gốc PO4 có hóa trị III. Vậy công thức hóa học của hợp chất tạo bởi nguyên tố Ba và gốc PO4 là
A. BaPO4
B. Ba2PO4
C. Ba3PO4
D. Ba3(PO4)
Lời giải
Công thức dạng: Bax(PO4)y
Ta có:
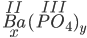
Áp dụng quy tắc hóa trị: II . x = III . y
=> rút ra tỉ lệ: ![]()
=> lấy x = 3 và y = 2
Đáp án cần chọn là: D
Câu 5: Một oxit có công thức Al2Ox có phân tử khối là 102. Hóa trị của Al trong hợp chất oxit này là
A. I
B. III
C. II
D. IV
Lời giải
+) Phân tử khối của Al2Ox là: 2 . 27 + 16 . x = 102 => x = 3
=> công thức hóa học của hợp chất Al2O3
+) Gọi hóa trị của Al trong hợp chất là a => ![]()
Theo quy tắc hóa trị: a . 2 = II . 3 => a = III
Vậy hóa trị của Al trong hợp chất này là III
Đáp án cần chọn là: B
Câu 6: Hợp chất Ba(NO3)y có PTK là 261. bari có NTK là 137, hóa trị II. Hãy xác định hóa trị của nhóm NO3
A. Hóa trị II
B. Hóa trị I
C. Hóa III
D. Hóa trị IV
Lời giải
Phân tử khối của Ba(NO3)y = 261
=> 137 + 62y = 261
=> y = 2
Công thức hóa học được lập là Ba(NO3)2
Gọi hóa trị của cả nhóm NO3 là a ta có:
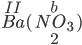
⇒II×1
=b×2
⇒b=1
Vậy nhóm NO3 có hóa trị I
Đáp án cần chọn là: B
Câu 7: Nguyên tố X có hóa trị III, công thức hợp chất của X với nhóm SO4 (II) là
A. XSO4
B. X(SO4)3
C. X2(SO4)3
D. X3SO4
Lời giải
Công thức dạng: Xx(SO4)y
Ta có:
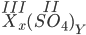
Áp dụng quy tắc hóa trị: III . x = II . y
=> rút ra tỉ lệ: ![]() => lấy x = 2 và y = 3
=> lấy x = 2 và y = 3
Công thức hợp chất là: X2(SO4)3
Đáp án cần chọn là: C
Câu 8: Lập CTHH và tính PTK của các hợp chất gồm:
a/ Fe (III) và nhóm OH
b/ Zn (II) và nhóm PO4 (III)
A. a/ Fe(OH)3 = 107 amu ; b/ Zn3(PO4)2 = 385 amu
B. a/ Fe(OH)2 = 90 amu ; b/ Zn3(PO4)2 = 365 amu
C. a/ Fe(OH)3 = 107 amu ; b/ Zn3(PO4)2 = 375 amu
D. a/ Fe(OH)2 = 90 amu ; b/ Zn3(PO4)2 = 385 amu
Lời giải
- Gọi công thức có dạng :
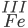
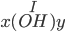
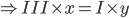
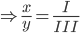
=> chọn x = 1 và y = 3
=> CTHH : Fe(OH)3
Tra SGK hóa 8 bảng 1- trang 42 có : PTK Fe(OH)3 = 56 + (16+1).3 = 107 amu
b/ Gọi công thức có dạng : ![]()
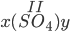
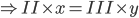
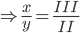
=> chọn x = 3 và y = 2
=> CTHH : Zn3(PO4)2
Tra SGK hóa 8 bảng 1- trang 42 có : PTK Zn3(PO4)2 = 65 + (31+16.4).3 = 385 amu
Đáp án cần chọn là: A
Câu 9: Biết S có hóa trị IV, hãy chọn công thức hóa học phù hợp với quy tắc hóa trị trong các công thức sau:
A. S2O2
B. S2O3
C. SO2
D. SO3
Lời giải
Xét đáp án A: ![]()
Theo quy tắc hóa trị ta có: a . 2 = II . 2 => a = II (loại vì đầu bài cho S hóa trị IV)
Xét đáp án B: ![]()
Theo quy tắc hóa trị ta có: a . 2 = II . 3 => a = III (loại)
Xét đáp án C: ![]()
Theo quy tắc hóa trị: a . 1 = II . 2 => a = IV (thỏa mãn)
Xét đáp án D: ![]()
Theo quy tắc hóa trị: a . 1 = II . 3 => a = VI (loại)
Đáp án cần chọn là: C
Câu 10: CTHH một số hợp chất của nhôm viết như sau: AlCl4, AlNO3, Al2O3, AlS, Al3(SO4)2, Al(OH)2, Al2(PO4)3. CTHH nào viết sai, hãy sửa lại cho đúng.
A. Các công thức viết sai: AlCl4, AlNO3, AlS
Sửa lại: AlCl3, Al(NO3)3, Al2S3.
B. Các công thức viết sai: AlCl4, AlNO3, AlS, Al3(SO4)2,
Sửa lại: AlCl3, Al(NO3)3, Al2S3, Al2(SO4)3,
C.Các công thức viết sai: AlCl4, AlNO3, AlS, Al3(SO4)2, Al(OH)2,
Sửa lại: AlCl3, Al(NO3)3, Al2S3, Al2(SO4)3, Al(OH)3.
D. Các công thức viết sai: AlCl4, AlNO3, AlS, Al3(SO4)2, Al(OH)2, Al2(PO4)3
Sửa lại: AlCl3, Al(NO3)3, Al2S3, Al2(SO4)3, Al(OH)3, AlPO4
Lời giải
Các công thức sai là: AlCl4, AlNO3, AlS, Al3(SO4)2, Al(OH)2, Al2(PO4)3
Sửa lại: AlCl3, Al(NO3)3, Al2S3, Al2(SO4)3, Al(OH)3, AlPO4
Đáp án cần chọn là: D
Thi online KHTN 8 KNTTThi online KHTN 8 CDThi online KHTN 8 CTST
Xem thêm Lý thuyết và các dạng bài tập Hóa học lớp 8 có đáp án khác:
- Lý thuyết & bài tập Công thức hóa học; Hóa trị
- Lý thuyết & bài tập Sự biến đổi chất
- Lý thuyết & bài tập Phản ứng hóa học
- Lý thuyết & bài tập Định luật bảo toàn khối lượng
- Lý thuyết & bài tập Phương trình hóa học
- Lý thuyết & bài tập Phản ứng hóa học
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Loạt bài Lý thuyết - Bài tập Hóa học lớp 8 có đáp án được biên soạn bám sát nội dung chương trình sgk Hóa học 8.
Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Giải Tiếng Anh 8 Global Success
- Giải sgk Tiếng Anh 8 Smart World
- Giải sgk Tiếng Anh 8 Friends plus
- Lớp 8 - Kết nối tri thức
- Soạn văn 8 (hay nhất) - KNTT
- Soạn văn 8 (ngắn nhất) KNTT
- Giải sgk Toán 8 - KNTT
- Giải sgk Khoa học tự nhiên 8 - KNTT
- Giải sgk Lịch Sử 8 - KNTT
- Giải sgk Địa Lí 8 - KNTT
- Giải sgk Giáo dục công dân 8 - KNTT
- Giải sgk Tin học 8 - KNTT
- Giải sgk Công nghệ 8 - KNTT
- Giải sgk Hoạt động trải nghiệm 8 - KNTT
- Giải sgk Âm nhạc 8 - KNTT
- Lớp 8 - Chân trời sáng tạo
- Soạn văn 8 (hay nhất) - CTST
- Soạn văn 8 (ngắn nhất) - CTST
- Giải sgk Toán 8 - CTST
- Giải sgk Khoa học tự nhiên 8 - CTST
- Giải sgk Lịch Sử 8 - CTST
- Giải sgk Địa Lí 8 - CTST
- Giải sgk Giáo dục công dân 8 - CTST
- Giải sgk Tin học 8 - CTST
- Giải sgk Công nghệ 8 - CTST
- Giải sgk Hoạt động trải nghiệm 8 - CTST
- Giải sgk Âm nhạc 8 - CTST
- Lớp 8 - Cánh diều
- Soạn văn 8 Cánh diều (hay nhất)
- Soạn văn 8 Cánh diều (ngắn nhất)
- Giải sgk Toán 8 - Cánh diều
- Giải sgk Khoa học tự nhiên 8 - Cánh diều
- Giải sgk Lịch Sử 8 - Cánh diều
- Giải sgk Địa Lí 8 - Cánh diều
- Giải sgk Giáo dục công dân 8 - Cánh diều
- Giải sgk Tin học 8 - Cánh diều
- Giải sgk Công nghệ 8 - Cánh diều
- Giải sgk Hoạt động trải nghiệm 8 - Cánh diều
- Giải sgk Âm nhạc 8 - Cánh diều

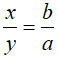
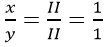





 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

